Clear Sky Science · ar
علامة حيوية كمِّية لإنزيم DOPA decarboxylase للتشخيص في اضطرابات أجسام ليوي
لماذا تكتسب التشخيصات الدماغية الأفضل أهمية
قد تبدو حالة الخرف المصحوب بأجسام ليوي ومرض باركنسون مشابهة كثيرًا لمرض ألزهايمر أو للشيخوخة الطبيعية، خصوصًا في المراحل المبكرة. ومع ذلك يمكن أن يؤدي التشخيص الخاطئ إلى علاجات خطيرة وفقدان فرص التخطيط للرعاية أو الانضمام إلى تجارب سريرية. تقدم هذه الدراسة اختبارًا مخبريًا واعدًا يعتمد على جزيء يسمى إنزيم DOPA decarboxylase (DDC) الموجود في السائل الذي يحيط بالدماغ والحبل الشوكي. وتشير النتائج إلى أن قياس هذا المكوّن في السائل قد يساعد الأطباء على التمييز بين الأمراض المرتبطة بأجسام ليوي وألزهايمر أو الشيخوخة الصحية بثقة أكبر بكثير.
بصمة خفية في سائل الدماغ
تُسبِّب اضطرابات أجسام ليوي، والتي تشمل الخرف المصحوب بأجسام ليوي ومرض باركنسون، تكتلات لبروتين يسمى ألفا‑سينوكلين تُلحق الضرر بالخلايا العصبية، لا سيما تلك التي تستخدم الناقل العصبي الدوبامين. إنزيم DDC يشارك في صنع الدوبامين والسيروتونين. أشارت مسوح بروتينية أوسع سابقة إلى أن مستويات DDC غالبًا ما تكون أعلى في السائل الدماغي الشوكي الشفاف لدى المصابين باضطرابات أجسام ليوي، لكن تلك النتائج اعتمدت على أساليب بحثية غير جاهزة للاستخدام الروتيني في مختبرات المستشفيات. سعى المؤلفون إلى بناء اختبارات دقيقة وقابلة للتوسيع لقياس تركيز DDC الفعلي في السائل الدماغي الشوكي والدم، ثم فحص مدى ارتباط هذه القياسات بالتشخيص والأعراض والتصوير الدماغي وفي بعض المرضى بالتغيرات التي لوحظت في التشريح المرضي بعد الوفاة.
بناء اختبار موثوق
طوّر الفريق اثنين من اختبارات المناعة الحساسة لـ DDC—أحدهما يعمل على منصة تُدعى Ella والآخر على نظام معروف باسم Simoa. كل منهما يستخدم زوجًا من الأجسام المضادة لالتقاط جزيئات DDC وإنتاج إشارة قابلة للقياس، وقد تم التحقق من دقتهما واتساقهما واستقرارهما تحت ظروف تخزين ومناولة مختلفة. كانت الاختبارات قادرة على اكتشاف DDC في كل عينة سائل دماغي شوكي تم فحصها، وكانت النتائج بين المنصتين وكذلك مقارنةً باختبار القرب السابق (proximity extension assay) متقاربة للغاية. كما تم تعديل أحد إصدارات اختبار Simoa للعمل في بلازما الدم ومصله، على الرغم من أن تركيز الدراسة ظل على السائل الدماغي الشوكي الذي يعكس التغيرات الدماغية بشكل مباشر أكثر.
فصل واضح بين الأمراض
باستخدام هذه الأدوات، قاس الباحثون DDC في السائل الدماغي الشوكي لأكثر من 700 شخص عبر ست مجموعات مستقلة من عدة دول. في كل مجموعة، كانت مستويات DDC لدى الأشخاص المصابين بالخرف المصحوب بأجسام ليوي أو بمرض باركنسون أعلى بكثير في السائل الدماغي الشوكي—حتى بمقدار حوالى مرتين ونصف مقارنةً بالمراقبين الأصحاء وكانت أعلى بوضوح من مستويات ألزهايمر. عند دمج قيمة DDC مع عمر الشخص وجنسه في نماذج تشخيصية معيارية، مكن الاختبار من تمييز اضطرابات أجسام ليوي عن الأصحاء بمساحات تحت المنحنى تقارب أو تتجاوز 0.9، مما يدل على دقة ممتازة. كما فصل بينهم وبين مرض ألزهايمر بأداء عالٍ، بما في ذلك في مجموعة من المرضى تم تأكيد تشخيصهم إما بواسطة اختبار "بذرة" ألفا‑سينوكلين عالي الخصوصية أو بفحص الدماغ بعد الوفاة. بالمقابل، لم تختلف مستويات DDC في الدم بين مجموعات التشخيص بشكل موثوق وكان تأثيرها قويًا من جراء الأدوية الدوبامينية، مما يجعل الدم أقل ملاءمة للتشخيص.
ربط الاختبار بالأعراض والتغيرات الدماغية
خارج نطاق التشخيص، استكشف الفريق ما الذي قد تعكسه مستويات DDC المرتفعة في السائل الدماغي الشوكي داخل الدماغ. داخل مجموعات أجسام ليوي وباركنسون، رُبط ارتفاع DDC بوجود—وليس بشدة—الأعراض الحركية وبالهلاوس البصرية، وهما سِمتان بارزتان في خرف أجسام ليوي. لم تتتبع مستويات DDC باستمرار درجات الذاكرة أو العلامات المعيارية لألزهايمر في السائل الدماغي الشوكي، مما يشير إلى أنها تحمل معلومات جزءًا منها مستقلة عن التغيرات الكلاسيكية لألزهايمر. في أشخاص أجروا تصويرًا تفصيليًا لناقل الدوبامين، ارتبطت مستويات DDC الأعلى بنمط أوسع من الضرر الدوباميني يشبه ذلك المرصود في خرف أجسام ليوي. وفي مجموعة تشريح مرضي، رافق ارتفاع DDC في السائل الدماغي الشوكي وجود مرض أجسام ليوي أوسع، لا سيما في المادة السوداء (substantia nigra)، وهي منطقة في منتصف الدماغ حاسمة للحركة.
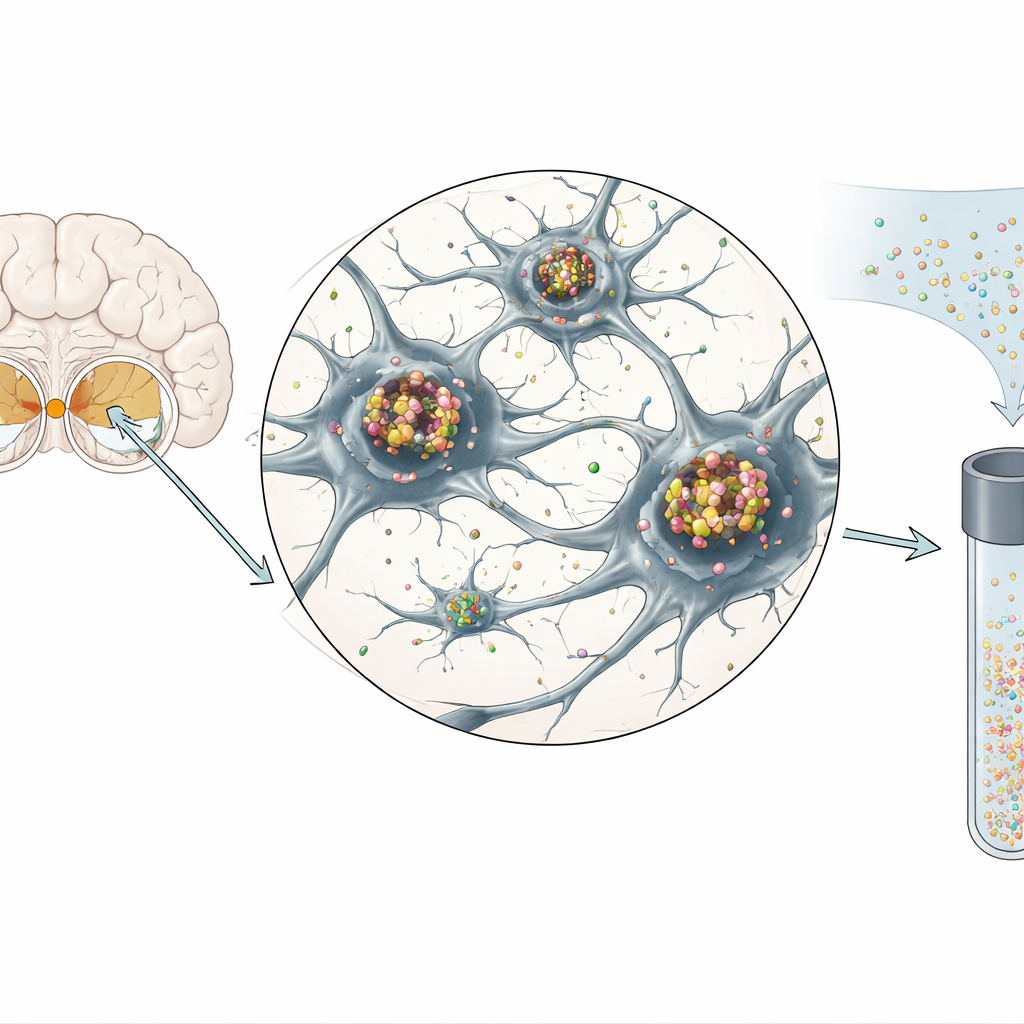
رؤية DDC داخل الخلايا العصبية المعرضة للخطر
لربط إشارة السائل بالنسيج الدماغي الفعلي، فحص الباحثون عينات بعد الوفاة لأشخاص مصابين بالخرف المصحوب بأجسام ليوي ومرض باركنسون المصحوب بالخرف، وأيضًا لمراقبين أصحاء عصبيًا. باستخدام نفس الجسم المضاد المستخدم في اختبارات السائل، أظهروا أن DDC وافر في الخلايا العصبية المنتجة للدوبامين في المادة السوداء وفي الخلايا المنتجة للسيروتونين في نوى الرابيه في جذع الدماغ. في مرضى اضطرابات أجسام ليوي، لم يكن DDC حاضرًا في الخلايا الناجية فحسب، بل تراكز أيضًا داخل أجسام ليوي والهياكل الشاذة ذات الصلة، وشغل نفس المساحات الخلوية مثل ألفا‑سينوكلين المرتبط بالمرض والمُفْرزَف (phosphorylated). بقي عدد أقل من الخلايا العصبية إجمالًا، لكن تلك المتبقية غالبًا ما أظهرت إشارة DDC قوية، بما يتوافق مع تراكم تعويضي للإنزيم أو تسربه من خلايا تالفة إلى السائل المحيط.
ماذا يعني هذا للمرضى
باختصار، تُظهر الدراسة أن مستويات DDC في السائل الدماغي الشوكي مرتفعة بشكل متين ومحدّد في الخرف المصحوب بأجسام ليوي ومرض باركنسون، وترتبط بانتشار مرض أجسام ليوي في الدماغ، ويمكن قياسها بصورة موثوقة باستخدام منصات مخبرية شائعة بالفعل في الممارسات السريرية. بينما لا يحل الاختبار مكان التقييم السريري الدقيق أو التصوير، فقد يصبح أداة قيّمة لدعم التشخيص، والمساعدة في تمييز اضطرابات أجسام ليوي عن ألزهايمر، واختيار المرضى لتجارب سريرية بشكل أفضل. يقترح المؤلفون اعتماد DDC في السائل الدماغي الشوكي كعلامة حيوية عملية جديدة تقرّبنا من تشخيصات قائمة على البيولوجيا لبعض أصعب أشكال الخرف.
الاستشهاد: Bolsewig, K., Bellomo, G., Hok-A-Hin, Y.S. et al. A quantitative DOPA decarboxylase biomarker for diagnosis in Lewy body disorders. Nat Med 32, 1073–1084 (2026). https://doi.org/10.1038/s41591-026-04212-0
الكلمات المفتاحية: خرف أجسام ليوي, مرض باركنسون, علامة حيوية في السائل الدماغي الشوكي, DOPA decarboxylase, ألفا-سينوكلين