Clear Sky Science · ar
الهروب المستضدي متعدد الأشكال من محرضات الخلايا التائية المستهدفة لـ GPRC5D في المايلوما المتعددة
عندما يتفوق السرطان على المناعة الدقيقة
تحوّل أدوية مناعية قوية جديدة علاج المايلوما المتعددة، وهو سرطان دم يبقى غير قابل للشفاء لدى معظم المرضى. تعمل هذه العلاجات عن طريق توجيه خلايا T في الجسم للبحث عن الخلايا الورمية وتدميرها عندما تحمل علمًا محددًا على سطحها. من الأعلام الواعدة جزيء يسمى GPRC5D. ومع ذلك، كما هو الحال مع العديد من العلاجات المستهدفة، يمكن للأورام أن تتطور وتفلت من العلاج. تكشف هذه الدراسة بتفصيل غير معتاد كيف تغيّر خلايا المايلوما أو تخفي علم GPRC5D لتتمكن من الهروب من أدوية ربط الخلايا التائية شديدة الفعالية.
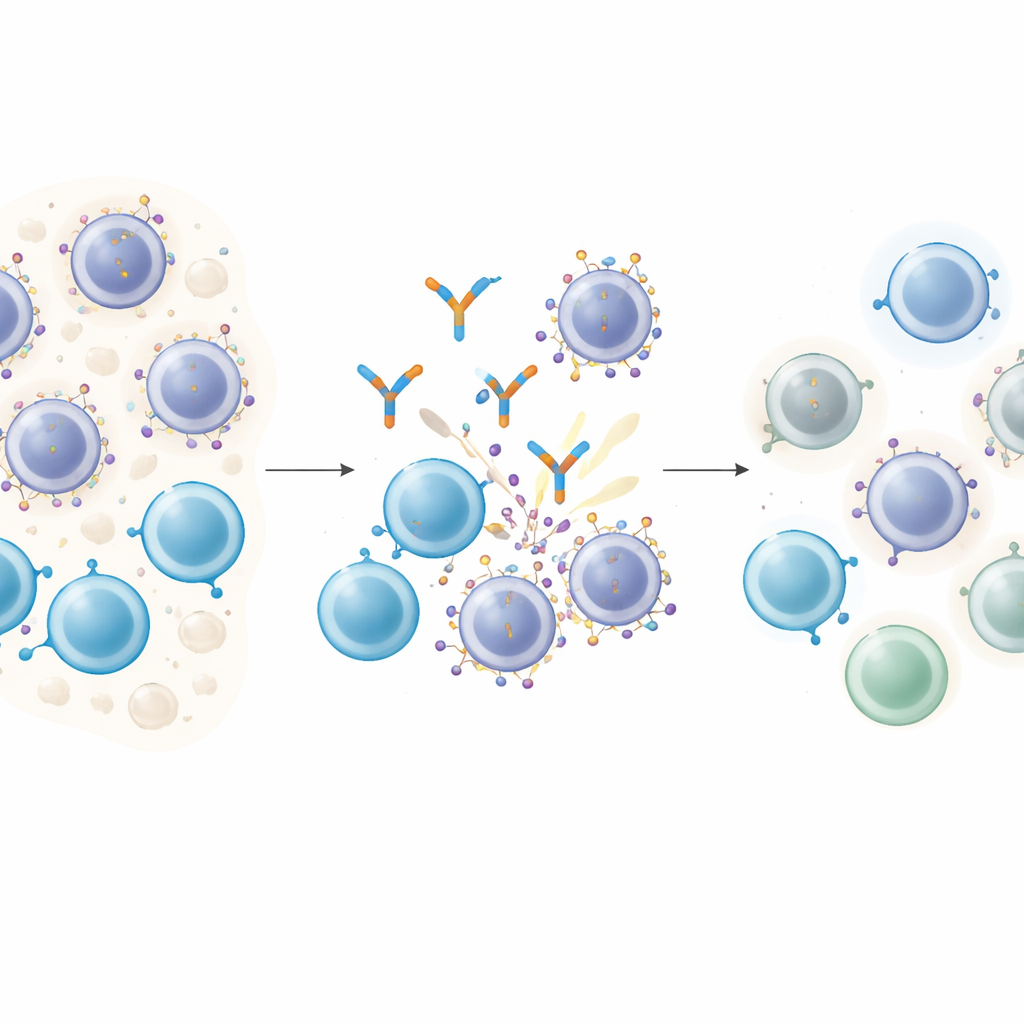
كيف تقبض الأدوية الذكية على خلايا السرطان
تعمل الأجسام المضادة المحرّكة للخلايا التائية كوساطات جزيئية: ينشُد طرف واحد خلية T، بينما يمسك الطرف الآخر بجزيء الهدف على خلية السرطان، جالبًا بينهما اتصالًا مباشرًا حتى تتمكن خلية T من قتل هدفها. في المايلوما المتعددة، يُعد GPRC5D هدفًا جذابًا لأنه وفير على الخلايا البلازمية الخبيثة ونادر في معظم الأنسجة الطبيعية. غالبًا ما يحقق المرضى المعالجون بعقار موجه إلى GPRC5D يُدعى تالكيتماب تراجعات عميقة في المرض. ومع ذلك، يتراجع معظم المرضى في نهاية المطاف، مما يثير سؤالًا حيويًا: هل تغيّر الخلايا السرطانية الهدف نفسه الذي تعتمد عليه هذه الأدوية؟
تتبع تطور الورم في الزمن الحقيقي
تبع الباحثون 21 شخصًا مصابًا بالمايلوما المقاومة للعلاج الذين تلقوا تالكيتماب. جمَعوا عينات نخاع العظم قبل العلاج لدى بعض المرضى ومرة أخرى عند عودة السرطان، ثم استخدموا طبقات متعددة من تحليل الحمض النووي، والحمض النووي الريبي، والكروماتين لفحص الخلايا الورمية. أظهر هذا العرض شديد التفصيل أنه في نحو ثلثي المرضى الذين انتكسوا، غيّر السرطان GPRC5D بطرق تقلل أو تمنع تأثير الدواء. لافت للنظر أن عدة نماذج فرعية مقاومة مختلفة—فروع ورمية متميزة وراثيًا—كثيرًا ما تعايشت في نفس المريض، مما يدل على أن التطور نحو الهروب يمكن أن يسلك عدة مسارات في آن واحد.
ثلاث طرق رئيسية تخفي بها الأورام الهدف
وجد الفريق ثلاثة أنماط متكررة تهرب بها خلايا المايلوما من التعرف. في بعض المرضى، حُذفت أجزاء من الكروموسوم الحامل لجين GPRC5D على النسختين، مما أزال العلم تمامًا من سطح الخلية. في حالات أخرى، أحدثت تغييرات أصغر—تبديلات حرفية في الحمض النووي أو إدخالات وحذفيات صغيرة—تشوه مناطق مهمة من بروتين GPRC5D. عطلت العديد من هذه التغيرات أجزاء من البروتين اللازمة للانتقال الصحيح من داخل الخلية إلى الغشاء الخارجي، مما جعل GPRC5D عالقًا في حجرة داخلية بدلًا من أن يُعرض حيث يمكن للدواء رؤيته. المسار الثالث شمل الصمت فوق الجيني: أصبح الحمض النووي المحيط بـ GPRC5D مضغوطًا ومعنونًا كيميائيًا بحيث نُدرَس الجين بالكاد، على الرغم من أن التسلسل الجيني الأساسي ظل إلى حد كبير سليمًا. الخلايا الورمية التي استخدمت هذه الاستراتيجية أنتجت قليلًا أو لم تنتج GPRC5D على الإطلاق.
عندما يكون العلم موجودًا لكن القفل لم يعد يناسب المفتاح
لم تزيل كل سبل الهروب GPRC5D من سطح الخلية. في بعض الحالات بدا البروتين طبيعيًا للاختبارات المعملية القياسية لكنه لم يعد يناسب الدواء كما المفتاح في القفل. أعاد الفريق إنشاء طفرات محددة مأخوذة من مرضى في خطوط خلوية مخبرية واختبروا مدى قدرة أجسام مضادة مختلفة مستهدفة لـ GPRC5D على الارتباط بفاعلية وقتل هذه الخلايا. غيرت طفرة واحدة المكان الدقيق الذي يمسك فيه تالكيتماب بالمستقبل بشكل طفيف، مما قلّل بشدة قدرة الدواء على الارتباط وإحداث موت الخلية، على الرغم من أن المستقبل ظل مرئيًا بالتلوين الروتيني. ومن المثير للاهتمام أن دواءً آخر موجهًا إلى GPRC5D ويشد المستقبل في موضعين ظل فعالًا ضد عدة من هذه الطفرات، مما يبرز كيف يمكن لتصميم الدواء—مثل استخدام ارتباط متعدد التكافؤ أو متعدد المواقع—أن يؤثر على بقاء النماذج المقاومة.
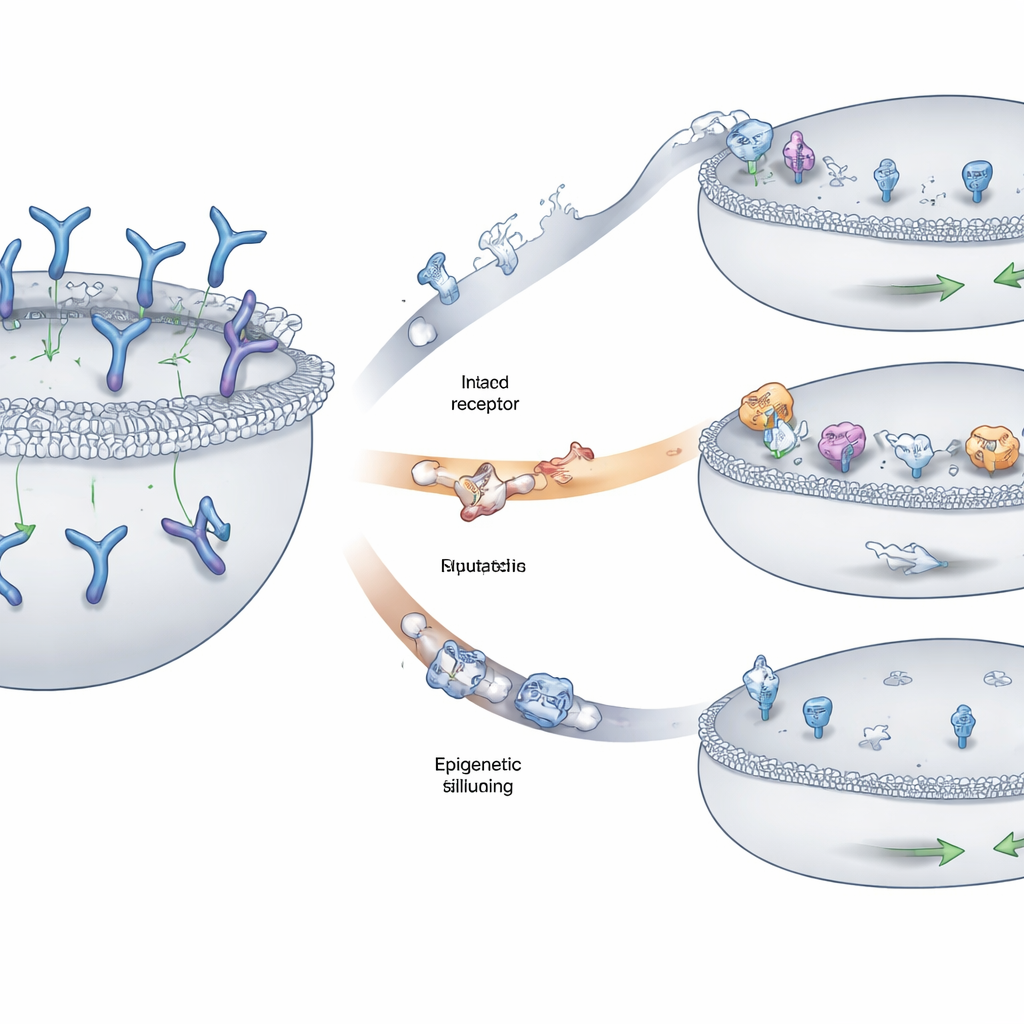
ما وراء الهدف: حدود أخرى للهجوم المناعي
بينما أظهرت غالبية حالات الانتكاس نوعًا من فقدان GPRC5D أو تغييره، انتكس أقلية من المرضى دون تغييرات واضحة في الهدف نفسه. في هذه الحالات بدا أن المشكلة تكمن في خلايا T: كانت أقل جاهزية وأقل قدرة على قتل الخلايا السرطانية في الاختبارات المخبرية، مما يوحي بأن التعرض المستمر طويل الأمد لعلاج المحرض قد يستنفد الجهاز المناعي. كشفت الدراسة أيضًا أن نوعًا وراثيًا معينًا من المايلوما (يشمل تبادلًا كروموسوميًا يُدعى t(11;14)) يحافظ طبيعيًا على جين GPRC5D في حالة كروماتين أكثر «إغلاقًا»، مع تعبير أساسي أقل. يطرح هذا احتمال أن بعض المرضى قد يكونون عُرضة لردود فعل ضعيفة لأن أورامهم تبدأ بمستويات مخففة من العلم المستهدف.
ماذا يعني هذا للمرضى والعلاجات المستقبلية
بالنسبة للمرضى والأطباء، يفسر هذا العمل لماذا ليست العلاجات الموجهة بقوة إلى GPRC5D علاجات شافية حتى الآن: يمكن لخلايا المايلوما حذف أو إعادة ترتيب أو توجيه بشكل خاطئ أو إيقاف تشغيل العلم الذي تعتمد عليه هذه الأدوية، وغالبًا ما تفعل ذلك بطرق متعددة في آن واحد. تشير النتائج إلى أن مراقبة حمض نووي الورم، بدلًا من قياس مستويات البروتين فحسب، ستكون مهمة لاكتشاف الطفرات الناشئة للهروب التي قد تفوتها الاختبارات الروتينية. كما تشير إلى استراتيجيات الجيل القادم—مثل أدوية ترتبط بـ GPRC5D بشدة في مواقع متعددة، أو تركيبات تهاجم أكثر من هدف في آن واحد، أو عوامل تعيد فتح الجينات المكمّمة—للمواكبة مع تطور الورم. في جوهرها، ترسم هذه الدراسة طرق الهروب التي تستخدمها المايلوما حتى يمكن تصميم العلاجات المستقبلية لسدّها، والحفاظ على فعالية علاجات الخلايا التائية لفترات أطول.
الاستشهاد: Lee, H., Ahn, S., Gonzales, G.A. et al. Multimodal antigenic escape to GPRC5D-targeted T cell engagers in multiple myeloma. Nat Med 32, 964–977 (2026). https://doi.org/10.1038/s41591-025-04175-8
الكلمات المفتاحية: المايلوما المتعددة, محرضات الخلايا التائية, GPRC5D, هروب المستضد, المناعة المضادة للسرطان