Clear Sky Science · ar
لينافونكيبارت وبيمبروليزوماب في الأورام الصلبة المتقدمة المقاومة لحجب نقاط التفتيش المناعية: تجربة مرحلة 1
لماذا تهمنا السرطانات العنيدة جميعًا
غيّرت أدوية المناعة التي «تزيل المكابح» عن الجهاز المناعي طريقة علاج العديد من السرطانات، لكن معظم المرضى إما لم يستفيدوا أبدًا أو عاودت أورامهم النمو في النهاية. تختبر هذه الدراسة دواءً جديدًا مناعيًا على شكل جسم مضاد، لينافونكيبارت، صُمم لتعطيل درع قوي تستخدمه الأورام للاختفاء من الهجوم المناعي، ويُدمج مع علاج مناعي موجود بالفعل هو بيمبروليزوماب. تقدم النتائج لمحة مبكرة تفيد أنه حتى لدى المرضى الذين توقفت سرطاناتهم عن الاستجابة لأدوية نقاط التفتيش، قد يكون من الممكن استعادة السيطرة المناعية مع الحفاظ على الآثار الجانبية تحت السيطرة.
درع خفي حول الأورام
تعمل العديد من أدوية المناعة الحديثة عن طريق حجب ما يُسمى جزيئات نقاط التفتيش، مثل PD‑1، التي تكبح عادة خلايا T. عند إزالة هذه المكابح، يمكن للخلايا المناعية أن تهاجم السرطان بشراسة أكبر. لكن الأورام غالبًا ما تتكيف ببناء حي عدائي حول نفسها يمنع خلايا T القاتلة من الوصول أو يضعفها بمجرد وصولها. مهندس رئيسي لهذه الفقاعة الواقية هو بروتين إشاري يُدعى TGFβ1، يُنتَج بواسطة خلايا السرطان والخلايا الداعمة المجاورة. أظهرت المحاولات السابقة لحجب عائلة TGFβ بأكملها وعودًا لكنها واجهت مشاكل خطيرة في القلب والنزف، لأن أفراد العائلة الآخرين مهمون للأنسجة السليمة. صُمم لينافونكيبارت ليخترق هذه الفجوة عن طريق تحييد الشكل الكامن وغير النشط من TGFβ1 بشكل انتقائي قبل تفعيله، مع ترك الجزيئات القريبة المرتبطة التي يحتاجها الجسم دون المساس بها.
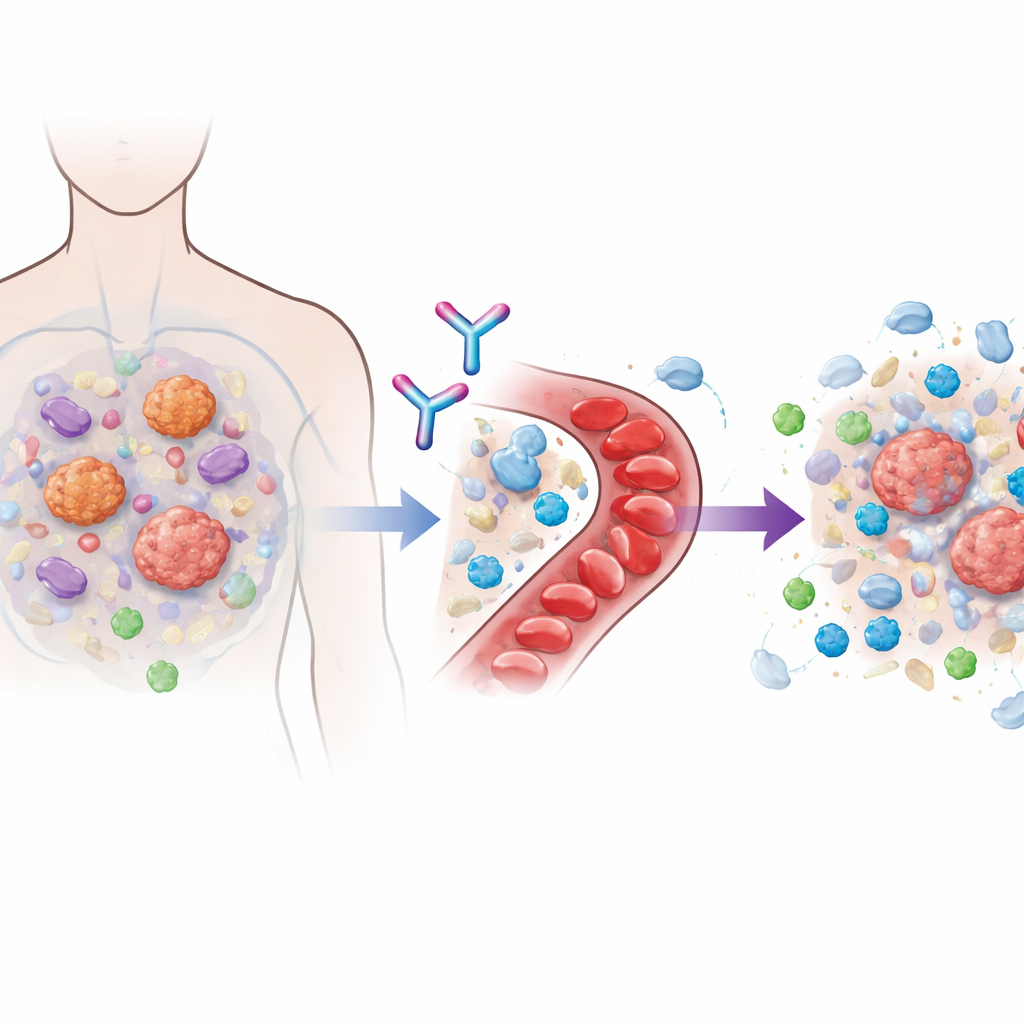
تصميم اختبار إنساني أولي بحذر
كانت تجربة DRAGON دراسة متعددة المراكز من المرحلة الأولى أُجريت في 22 مستشفى في الولايات المتحدة وكوريا الجنوبية. شملت 112 بالغًا مصابين بأورام صلبة متقدمة، وجميعهم لم تكن أمامهم خيارات علاجية كثيرة. في الجزء الأول من الدراسة، أُعطي لينافونكيبارت منفردًا بجرعات متزايدة تدريجيًا لمجموعات صغيرة من المرضى، أو مدموجًا مع دواءهم السابق المعتمد على PD‑1. استُخدم هذا النهج المرحلي لرسم خريطة السلامة، وكيفية تحرك الدواء وبقائه في مجرى الدم، ولتحديد جرعة للاختبار الأوسع. في الجزء الثاني، تلقى 78 مريضًا كانت سرطاناتهم قد قاومت بالفعل جرعة واحدة على الأقل من علاج PD‑1 جرعة ثابتة من لينافونكيبارت مع بيمبروليزوماب. كان لدى هؤلاء المرضى سرطانات يصعب علاجها، بما في ذلك سرطان الكلية ذو الخلايا الصافية، الميلانوما، سرطانات الرأس والعنق، سرطان المثانة (البولي) وسرطان الرئة، وأغلبهم خضعوا لعدة علاجات سابقة.
السلامة أولًا: ماذا حدث للمرضى
كان الهدف الرئيسي من هذه الدراسة المبكرة هو السلامة، وأظهر لينافونكيبارت أداءً مشجعًا في هذا الجانب. عبر جميع مستويات الجرعة، لم يُحدَّد جرعة تحمل قصوى، ولم تُسجل آثار جانبية مميتة أو محددة الجرعة مرتبطة بالدواء. عندما دمِج لينافونكيبارت مع بيمبروليزوماب عند جرعة المرحلة الثانية، عانى نحو ثلاثة أرباع المرضى من بعض الآثار الجانبية المرتبطة بالعلاج، وهو معدل مشابه لما يُرى غالبًا مع العلاج المناعي وحده. كانت الطفحات والحكة أكثر المشكلات الإضافية شيوعًا، وطور عدد صغير من المرضى التهابات جلدية أو رئوية أكثر خطورة. ومن المهم أن رد الفعل المناعي المفرط الخطير المعروف بمتلازمة تحرير السيتوكين، والذي يمكن أن يحدث مع بعض علاجات الأجسام المضادة، لم يُرَ، وكان نمط السلامة العام في الغالب يشبه أثر بيمبروليزوماب وحده.
دلائل على أن الجهاز المناعي يمكن إيقاظه مجددًا
على الرغم من أن هذه لم تكن تجربة فاعلية كبيرة وحاسمة، أشرَت عدة إشارات إلى أن إيقاف TGFβ1 قد يساعد في إحياء الاستجابات لحجب PD‑1. في مرحلة التوسعة، ضمّت تركيبة لينافونكيبارت–بيمبروليزوماب تقليصًا مرئيًا للأورام في نسبة ملحوظة من المرضى الذين توقفوا سابقًا عن الاستفادة من أدوية PD‑1. كانت معدلات الاستجابة المؤكدة 20% في سرطان الكلية ذو الخلايا الصافية، و18.2% في الميلانوما، وفقط أكثر من 9% في سرطانات الرأس والعنق والمثانة، مع تحقيق مريض واحد بسرطان الكلية اختفاءً تامًا للأمراض المرئية. استمرت العديد من هذه الاستجابات لأشهر عديدة، وبقي المرضى الذين استجابوا عادة على التركيبة لفترة أطول بكثير مقارنة بفترة علاجهم السابقة المعتمدة على PD‑1. قدمت الخزعات المأخوذة قبل وبعد العلاج تفسيرًا بيولوجيًا: أظهرت الأورام اختراقًا أكبر لخلايا CD8 «القاتلة»، ومستويات أعلى من الخلايا التائية المنشطة، وعددًا أقل من الخلايا التائية المنظمة القامعة والخلايا النقيية، وتحولًا عامًا نحو بيئة ميكروية أكثر التهابًا وجهوزية للهجوم.
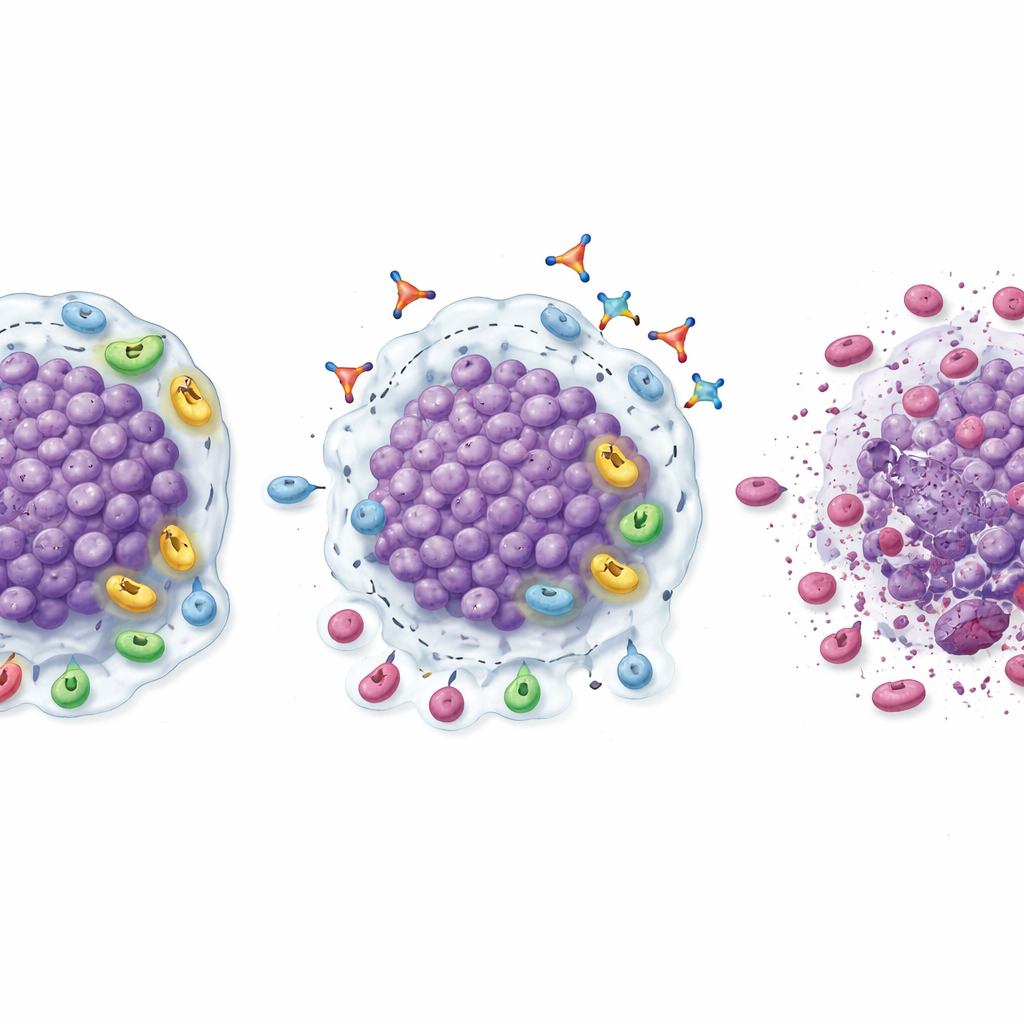
تحديد من قد يستفيد أكثر
استكشف الباحثون أيضًا أي المرضى قد يكونون أكثر احتمالًا للاستجابة. في سرطان الكلية ذو الخلايا الصافية، كانت الأورام التي احتوت بالفعل على عدد كبير من خلايا CD8 عند الأساس—ولكن كانت أيضًا غنية بالخلايا التائية المنظمة وتعبر عن مستويات عالية من TGFβ1—أكثر ميلًا للانكماش عند استخدام العلاج المركب. في هؤلاء المرضى، كانت معدلات الاستجابة والبقاء دون تقدم المرض أعلى بكثير من المجموعة الأوسع لسرطان الكلية. يوحي هذا النمط بوجود «نقطة مناسبة»: الأورام التي تتوفر فيها العديد من الجنود المناعيين لكنها مقيدة بقمع مدفوع بـ TGFβ1 قد تكون مرشحة مثالية للينافونكيبارت مضافًا إلى حجب PD‑1. إذا تم التحقق من ذلك في دراسات أكبر، فاختبارات نسيجية بسيطة لهذه العلامات قد تساعد الأطباء في اختيار المرضى الأكثر احتمالًا للاستفادة.
ما يعنيه هذا العمل للمستقبل
بالنسبة للأشخاص المصابين بسرطانات متقدمة قد قاومت بالفعل العلاج المناعي، فإن إمكانية إعادة تنشيط جهازهم المناعي دون إضافة سمية شديدة أمر جذاب. توفر هذه التجربة الإنسانية الأولى دليلًا مبكرًا على أن تعطيل درع TGFβ1 بشكل انتقائي باستخدام لينافونكيبارت قابل للقيام به بأمان وقد يعيد سيطرة ملموسة على الورم عند اقترانه بمثبط PD‑1، خصوصًا في بعض سرطانات الكلية. وبينما كانت الدراسة صغيرة وليست عشوائية، فإن سجل السلامة، والقراءات البيولوجية والاستجابات المستديمة معًا تبني حجة قوية لإجراء تجارب أكبر من المرحلة الثانية. إذا أكدت الدراسات المستقبلية هذه النتائج، فقد يوسع هذا النهج دائرة المرضى الذين يمكنهم الاستفادة من العلاج المناعي، محولًا بعض السرطانات العنيدة حاليًا إلى حالات تصبح مرة أخرى عرضة ل دفاعات الجسم الخاصة.
الاستشهاد: Yap, T.A., Sweis, R.F., Vaishampayan, U. et al. Linavonkibart and pembrolizumab in immune checkpoint blockade-resistant advanced solid tumors: a phase 1 trial. Nat Med 32, 992–1001 (2026). https://doi.org/10.1038/s41591-025-04157-w
الكلمات المفتاحية: العلاج المناعي للسرطان, ثبط TGFβ1, مقاومة نقاط التفتيش المناعية, سرطان الكلية ذو الخلايا الصافية, البيئة الميكروية للورم