Clear Sky Science · ar
خريطة قابلة للتفسير للالتهاب في الخلايا المناعية المتداولة
لماذا يهمك الالتهاب في الدم
الالتهاب يكمن في قلب العديد من الأمراض، من التهاب المفاصل والربو إلى كوفيد-19 والسرطان. ومع ذلك لا يزال الأطباء يواجهون صعوبة في قراءة إشارات الالتهاب في الجسم بطريقة تشرح بوضوح ما الذي يسير على غير ما يرام وأي علاج سيكون الأفضل. يبني هذا البحث "خريطة" ضخمة للخلايا المناعية المتداولة في الدم ويظهر كيف يمكن أن تعمل هذه الخلايا كمؤشرات حيوية حية وسهلة العينة لتصنيف مجموعة واسعة من الأمراض الالتهابية.
بناء خريطة عملاقة للخلايا المناعية
لرسم هذا المشهد، حلل الباحثون أكثر من 6.5 مليون خلية مناعية مأخوذة من دم 1,047 شخصًا. شمل هؤلاء المتطوعون 19 حالة، بما في ذلك أمراض مناعية ذاتية مثل الذئبة والتهاب المفاصل الروماتويدي، وأمراض رئوية مزمنة مثل الربو وCOPD، وعدوى مثل كوفيد-19 وHIV، وعددًا من السرطانات، إلى جانب متبرعين أصحاء. باستخدام تسلسل الحمض النووي الريبي أحادي الخلية، قاسوا أي الجينات كانت مُفعّلة في كل خلية على حدة، ثم استخدموا طرقًا إحصائية متقدمة لتصحيح الفروق الفنية بين الدراسات ولتجميع الخلايا إلى 64 حالة مناعية مميزة. تلتقط هذه "خريطة الالتهاب" كلًا من اللاعبين المعروفين—مثل الخلايا التائية، والخلايا البائية، والوحيدات—وأنواعًا فرعية متخصصة تتغير مع المرض.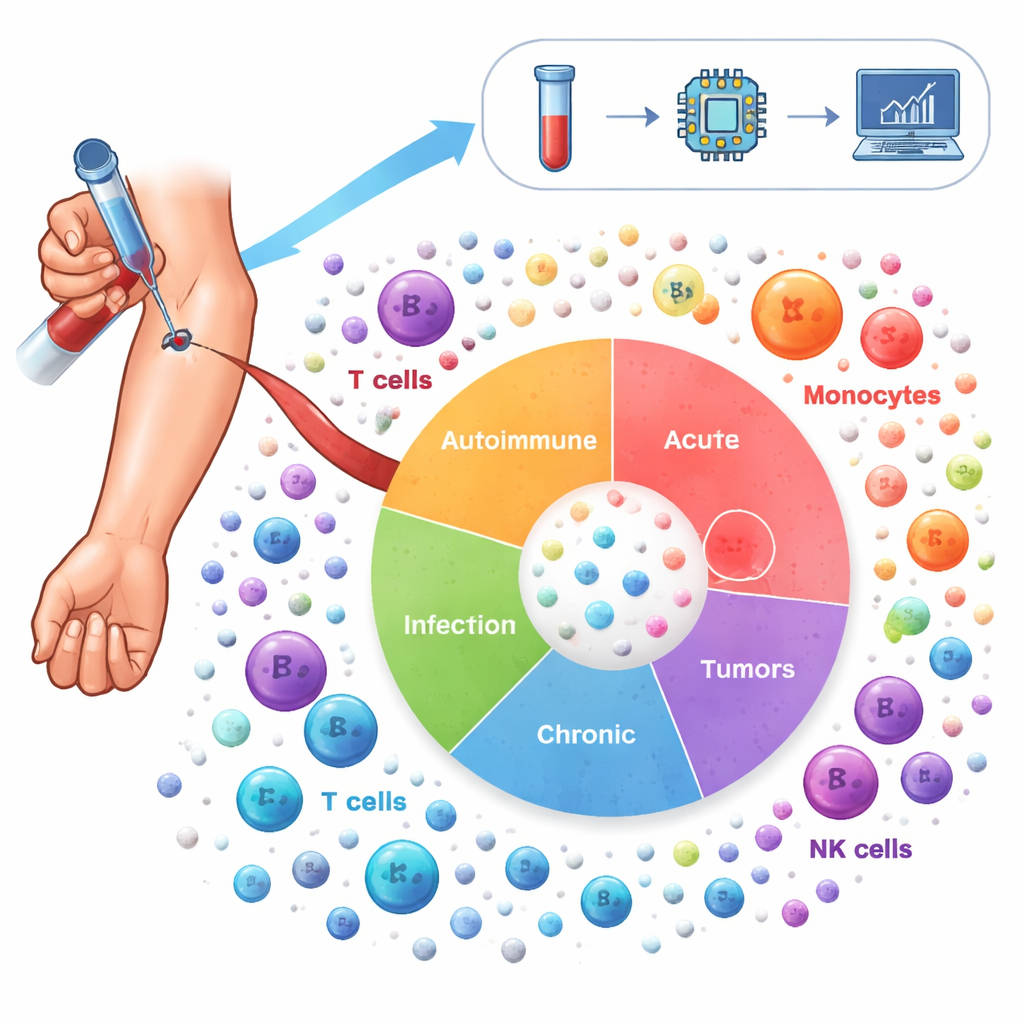
قراءة بصمات الالتهاب في الجسم
ركز الفريق بعد ذلك على الجينات التي تتحكم في كيفية تنشيط الخلايا المناعية وتحركها في الجسم وعرض المستضدات واستجابتها لجزيئات الإشارة مثل الإنترفيرونات وعامل نخر الورم. جمعوا هذه الجينات في 21 «بصمة» بيولوجية وصغّلوها لكل نوع خلية رئيسي. بمقارنة المرضى بالمتبرعين الأصحاء، تمكنوا من رؤية أي البصمات كانت مرتفعة أو منخفضة في أمراض مختلفة. على سبيل المثال، أظهرت العديد من الأمراض الالتهابية المناعية نشاطًا أقوى لجزيئات الالتصاق وآليات عرض المستضدات، بينما كانت استجابات الإنترفيرون منخفضة في معظم أنواع الخلايا لكنها مرتفعة في بعض الخلايا التائية CD8. العدوى الفيروسية مثل الإنفلونزا وكوفيد-19 عززت برامج مستحثة بالإنترفيرون، في حين أضعفتها الإصابات المزمنة مثل فيروس HIV والتهاب الكبد B.
التعمق في الجينات الرئيسية ومفاتيح التحكم
لأن البصمات العامة تخفي تفاصيل مهمة، نزل الباحثون إلى مستوى الجينات الفردية ومنظميها. في الخلايا التائية CD8 غير الساذجة، وجدوا أن جينين، FGFBP2 وGZMB، كانا نشيطين بشكل خاص في أنواع فرعية معينة من ذاكرة المؤثرات، خصوصًا في التهاب القولون التقرحي. ارتبطت هذه الجينات بإحداث تلف على السطوح الظهارية، وإشارة قوتها في الدم توحي بأن هذه الخلايا العدوانية تكون مهيأة بالفعل قبل دخولها إلى الأنسجة. تحليل منفصل لشبكات تنظيم الجينات أبرز عاملين نسخين، STAT1 وSP1، كمتحكمين مركزيين في برامج مستحثة بالإنترفيرون. اختلفت أنماط نشاطهما بين الأمراض وأنواع الخلايا—على سبيل المثال، سلوك متعاكس في الوحيدات مقابل الخلايا التائية CD8 في الذئبة، وتغيرات بين مراحل التفجر وعدم التفجر—مشيرًا إلى كيف يمكن لنفس المسارات أن تكون وقائية في سياق وضارة في آخر.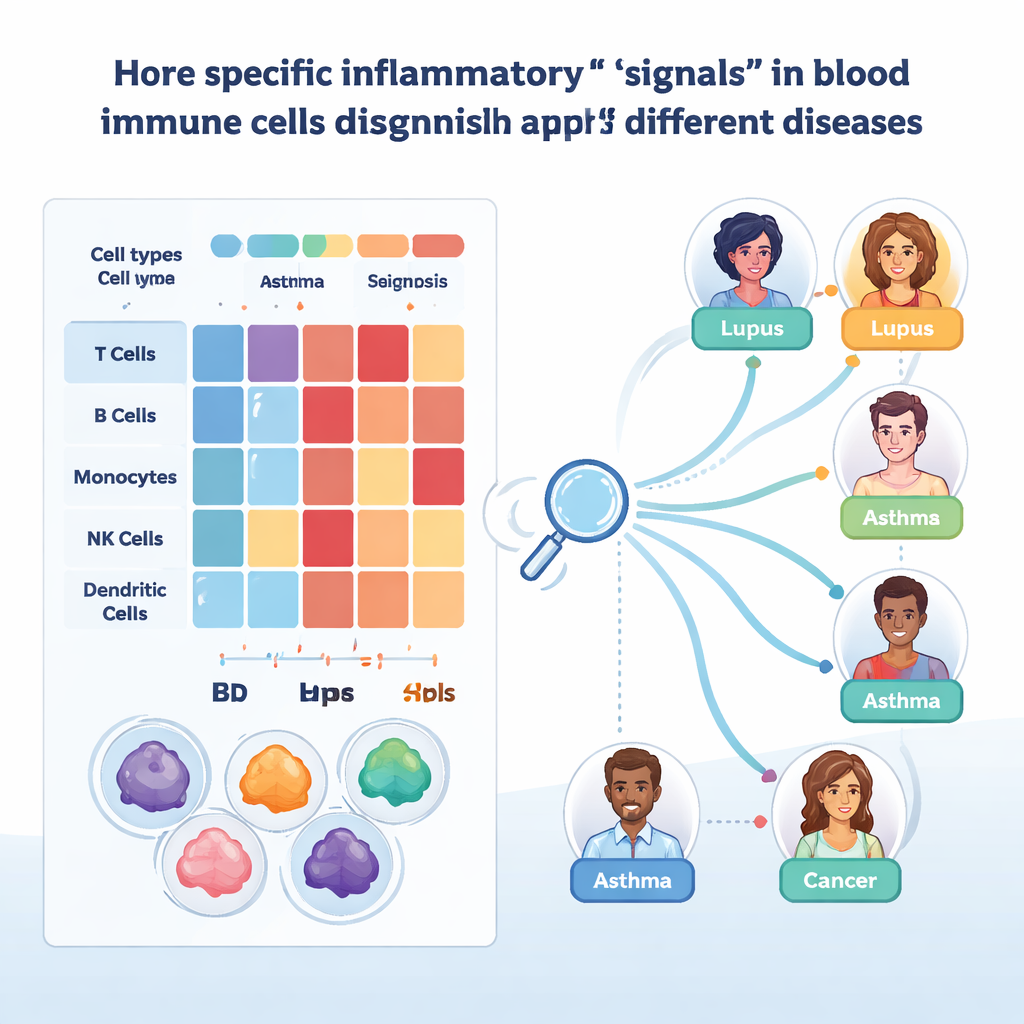
تدريب الآلات لتمييز المرض من خلايا الدم
لتحويل هذه الخريطة إلى أداة عملية، طبق الفريق تعلم آلة قابل للتفسير. دربوا نماذج أشجار قرار معززة تدريجيًا بشكل منفصل لكل نوع خلية رئيسي، طالبين من الخوارزميات تسمية الخلايا الفردية بالمرض الصحيح بناءً على تعبيرها الجيني. حققت هذه النماذج دقة عالية عند اختبارها على عينات محفوظة جانبًا، خاصة بعد تصحيح الفروق الفنية. باستخدام SHAP، وهي طريقة تشرح أي الجينات تقود كل قرار، تمكن الباحثون من تحديد مؤشرات حيوية مرشحة. مثال على ذلك هو CYBA في الوحيدات، حيث ساعدت مستوياته على التمييز بين أمراض الجلد مثل الصدفية والالتهاب المعوي في داء كرون والتهاب القولون التقرحي. ومثال آخر هو IFITM1 في بعض الخلايا التائية والخلايا اللمفاوية الخلقية، ففرّق بين الربو وCOPD مما يشير إلى أنماط مختلفة من الدفاع الفيروسي المزمن.
نحو بوصلة تشخيصية قائمة على الدم
أخيرًا، تساءل المؤلفون عما إذا كان يمكن تصنيف المرضى بأكملهم—وليس الخلايا الفردية فحسب—انطلاقًا من ملفاتهم المناعية المتداولة. سلطوا بيانات كل خلية في فضاء مُضمَّن مضغوط، وحسبوا متوسطات هذه المتضمّنات بحسب نوع الخلية لكل مريض، ودربوا مصنفات للتنبؤ بالمرض. عندما شابه المرضى الجدد من بيانات التدريب، كان الأداء ممتازًا. لكن عندما جاءت العينات من دراسات مستقلة تمامًا باستخدام طرق مخبرية مختلفة، انخفضت الدقة بشكل حاد، كاشفةً عن مدى حساسية مثل هذه الأدوات للتباينات الفنية. أعاد مجموعة بيانات "مركزية" أكثر تحكمًا، تم توليدها في مركز واحد بكيمياء تسلسل موحدة، كثيرًا من الأداء، مما يشير إلى الحاجة إلى بروتوكولات موحدة أو مجموعات تدريب ضخمة ومتنوعة للغاية.
ما يعنيه هذا للتشخيص والعلاج في المستقبل
بالنسبة للقارئ العام، الرسالة الأساسية هي أن خلاياك المناعية المتداولة تحمل بصمة غنية عن حالة الالتهاب في جسمك. بقراءة هذه البصمات خلية بخلة، يظهر هذا العمل أنه من الممكن التمييز بين العديد من الأمراض، واكتشاف جينات قد تسبّب أعراضًا محددة، والبدء في بناء اختبارات دم عالمية تصنف الأمراض الالتهابية. الدراسة ليست بعد اختبارًا سريريًا جاهزًا—فالفروق الفنية بين الدراسات لا تزال تحدّ من الموثوقية—لكنها تضع الأساس لأدوات "الخزعة السائلة" المستقبلية التي قد تساعد الأطباء على تحديد التشخيص والعلاج المناسبين مبكرًا باستخدام عينة دم بسيطة.
الاستشهاد: Jiménez-Gracia, L., Maspero, D., Aguilar-Fernández, S. et al. Interpretable inflammation landscape of circulating immune cells. Nat Med 32, 633–644 (2026). https://doi.org/10.1038/s41591-025-04126-3
الكلمات المفتاحية: الالتهاب, الخلايا المناعية, تسلسل الحمض النووي الريبي أحادي الخلية, مؤشرات حيوية, تعلم الآلة