Clear Sky Science · ar
يعطي CD38 خلايا Treg المحلية الخاصة بالمستضد قدرة على مقاومة الإجهاد للتحكم في التهاب الجهاز العصبي المركزي المقسَّم
لماذا تهم خلايا المناعة الحامية للدماغ
تتصرف العديد من أمراض الدماغ المناعية الذاتية، مثل التصلب المتعدد، كحرائق متقدة: تشتعل موجة أولية من الالتهاب ثم تخبو، لكن التلف قد يعاود الاشتعال بعد سنوات. تطرح هذه الدراسة سؤالاً يبدو بسيطاً لكنه ذو تداعيات كبيرة: بعد هجمة في الجهاز العصبي المركزي، ما الذي يحافظ على السلم—وما الذي يعيد التوازن نحو المرض؟ يركز المؤلفون على مجموعة صغيرة من خلايا المناعة تسمى خلايا تي التنظيمية التي تستقر في الدماغ والحبل الشوكي بعد الالتهاب، ويكشفون كيف يمنحها مولد سطحي واحد قدرة على البقاء في بيئة قاسية ومنع الانتكاسات.
حافظو السلام الذين يبقون في المكان
باستخدام نموذج فأري يحاكي جوانب من التصلب المتعدد، تعقّب الباحثون أنواعاً مختلفة من خلايا T بينما تصاعد المرض إلى ذروته ثم دخل مرحلة الانتعاش. بينما تقلص عدد خلايا T المساعدة التقليدية التي تُحرِّك الالتهاب مع تحسُّن الأعراض، بقيت خلايا تي التنظيمية—الخلايا المتخصصة التي تقلل عادة الاستجابات المناعية—في الجهاز العصبي المركزي. في الواقع زاد نصيبها النسبي داخل مجموعة خلايا T المحلية، واجتمعت في مصافٍ مميزة حول مساحات سائل الدماغ والأغشية الواقية المكسوة للدماغ. من خلال وسم أماكن منشأ خلايا T القادمة، أظهر الفريق أنه بعد الانتعاش وصل عدد قليل جداً من خلايا تي التنظيمية الجديدة من العقد اللمفاوية. بدلاً من ذلك حافظت التجمعات في الجهاز العصبي المركزي على نفسها محلياً إلى حد كبير، مما يوحي بوجود قوة «حفظ سلام» مقيمة على المدى الطويل. 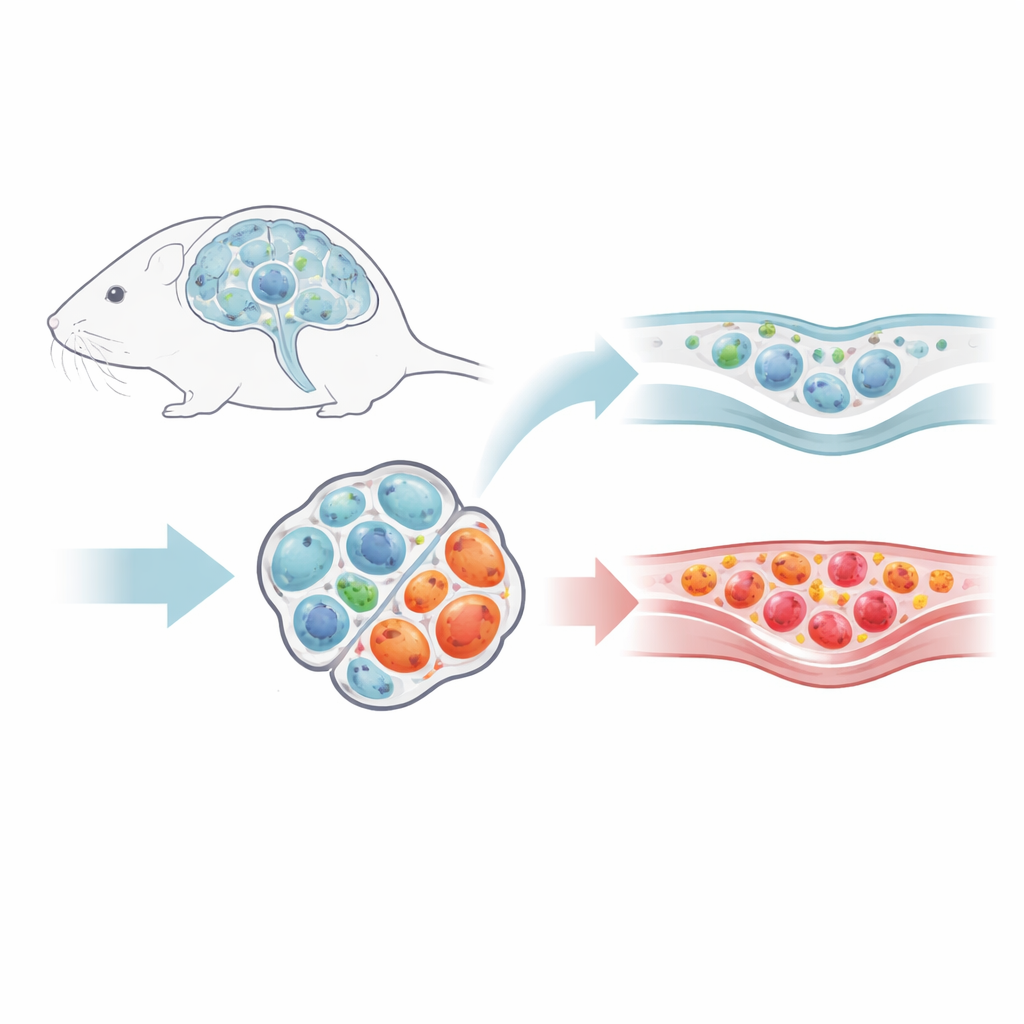
حراس متحملون للإجهاد في بيئة معادية
البيئة بعد الالتهاب في الجهاز العصبي المركزي بعيدة كل البعد عن الراحة لهذه الحماة. بعد موجة المرض الرئيسية، تنخفض مستويات إشارة النمو إنترلوكين-2 (IL-2)—التي تعتمد عليها خلايا تي التنظيمية بشكل كبير—لأن معظم الخلايا التائية التقليدية تراجعت. في الوقت نفسه، تكون الأنسجة غنية بجزيء أيضي هو NAD+، الذي يمكن أن يحفز موت الخلايا أو يثبط مستقبلات سطحية رئيسية عند تعديله بواسطة إنزيم محدد. من خلال وسم خلايا تي التنظيمية الفردية وتتبعها وراثياً، ميّز المؤلفون بين خلايا «مستقرة» حافظت على هويتها و«غير مستقرة» فقدت برنامج Foxp3 المميز لها. أظهرت الخلايا المستقرة بصمة قوية لإشارات IL-2 ومستويات أعلى من مستقبلات IL-2، مما يشير إلى أن القدرة على استشعار كميات قليلة من IL-2 أساسية للبقاء في هذه البيئة المضغوطة.
التحكم المحلي في الانتكاسات من داخل الدماغ
لاختبار ما إذا كانت خلايا تي التنظيمية المقيمة مهمة فعلاً للتحكم طويل الأمد في المرض، أزال الباحثون هذه الخلايا بشكل انتقائي من الجهاز العصبي المركزي باستخدام سم نُقل مباشرة إلى سائل الدماغ، مع ترك معظم خلايا تي التنظيمية الجهازية في أجزاء أخرى من الجسم سليمة. خلال أيام، طورت الفئران التي كانت في طور التعافي انتكاسات شديدة مع تجدد الشلل. بالمقابل، لم تُحدث إزالة خلايا تي التنظيمية في الجسم فقط—مع إبقاء تلك الموجودة في الجهاز العصبي المركزي—تفجُّرات. شملت الانتكاسة إعادة تنشيط سريعة وتوسعاً لخلايا T الفعالة التي كانت مستوطنة بالفعل في الجهاز العصبي المركزي، حتى عندما حُجب استقدامها من الدم. يوضح هذا أن خلايا تي التنظيمية المحلية، لا المتداولة، ضرورية لكبح الخلايا العدوانية المتبقية التي تبقى بعد مرور الهجمة الحادة.
كيف يحمي إنزيم واحد خلايا التنظيم
بالغوص أعمق، بحث المؤلفون عن جزيئات تميّز خلايا تي التنظيمية المتحملة للإجهاد في الجهاز العصبي المركزي. برز لاعب رئيسي: CD38، إنزيم على سطح الخلية يكسر NAD+ خارج الخلية. في الجهاز العصبي المركزي الملتهب، زادت خلايا تي التنظيمية بشكل قوي من CD38، بينما لم تُظهر خلايا T التقليدية هذا التغير الملحوظ. عندما نقل الفريق خلايا تي تنظيمية متفاعلة مع الميالين تفتقر إلى CD38 إلى الفئران، وصلت هذه الخلايا إلى الجهاز العصبي المركزي لكنها فشلت في السيطرة على المرض، على عكس نظائرها الطبيعية. في حيوانات خيمرية مختلطة، حيث كانت خلايا تي التنظيمية المقيمة فقط ناقصة CD38، كانت إزالة الجزء الكافي من الخلايا عالية CD38 كافية لإثارة انتكاسات، مما يبيّن أن CD38 يعمل بطريقة جوهرية داخل الخلية لتمكين السيطرة الفعالة.
حماية إشارة شريان الحياة
كشفت التجارب الآلية كيف يمنح CD38 هذه المقاومة. يمكن لمستويات NAD+ العالية في الجهاز العصبي المركزي أن تغذّي تعديلًا كيميائياً للبروتينات السطحية بواسطة إنزيم ARTC2.2. أحد الأهداف الحساسة هو الوحدة ذات التقارب العالي لمستقبل IL-2، التي تُعبَّر عنها خلايا تي التنظيمية بمستويات مرتفعة جداً، خاصة عند تعرفها على مستضدات الدماغ. في خلايا تي التنظيمية الناقصة CD38 المعرّضة لـ NAD+، أصبح معظم مستقبلات IL-2 معدّلاً، مما أدى إلى تفعيل أضعف للمرسال الأسفل STAT5 وتقليل الاستجابة لـ IL-2. في المقابل، خفّضت الخلايا المعبرة عن CD38 محلياً NAD+ حول نفسها، محدودة هذا التعديل الضار ومُحافظةً على إشارات IL-2 القوية. في فئران حية، أدى حقن NAD+ في الدماغ إلى قتل معظم خلايا تي التنظيمية عبر هذا المسار بشكل انتقائي، مع إبقاء خلايا T التقليدية على قيد الحياة، مما يؤكد هشاشة هذه المقيمة من دون هذا الإنزيم الوقائي. 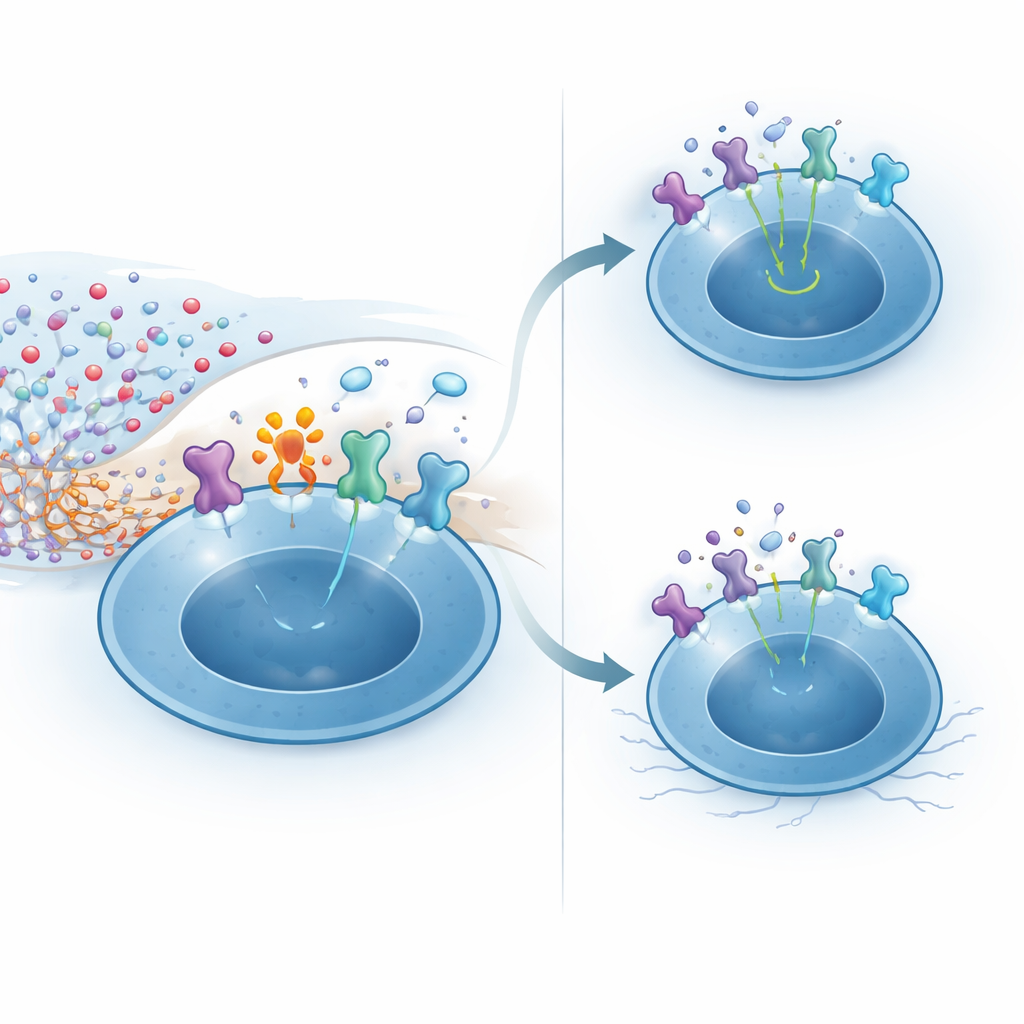
ماذا يعني هذا لالتهابات الدماغ المزمنة المناعية
ترسم هذه الدراسة صورة عن المناعة الذاتية المزمنة في الجهاز العصبي المركزي كميدان معركة مقسَّم: تجمعات صغيرة من خلايا T العدوانية المتبقية تقيم في الدماغ والحبل الشوكي، محبوسة بقوة من قبل خلايا تي تنظيمية محلية متخصصة بالمثل. هؤلاء الحماة «متحملون للإجهاد» لأن CD38 يسمح لهم بالبقاء لدى وجود NAD+ عالي ومواصلة استشعار كميات ضئيلة من IL-2، محافظين على هويتهم ووظيفتهم القمعية. للخلاصة العامة، النقطة الأساسية هي أن التحكم طويل الأمد بأمراض مثل التصلب المتعدد قد يعتمد بدرجة أقل على الجهاز المناعي المتداول وبدرجة أكبر على رعاية وحماية هؤلاء الحماة المقيمين داخل الدماغ نفسه—ومن الممكن أن يتم ذلك عبر استهداف مسارات تعزّز وظيفة CD38 أو حساسية IL-2 في خلايا تي التنظيمية.
الاستشهاد: Chen, HH., Tyystjärvi, S., Ruiz Navarro, D. et al. CD38 endows local antigen-specific Treg cells with stress resilience for control of compartmentalized CNS inflammation. Nat Immunol 27, 516–529 (2026). https://doi.org/10.1038/s41590-025-02416-z
الكلمات المفتاحية: خلايا تي التنظيمية, التصلب المتعدد, التهاب الجهاز العصبي المركزي, إنزيم CD38, التسامح المناعي