Clear Sky Science · ar
النمط المكاني لإشارة TGFβ في الأرومة الليفية يفسر مقاومة العلاج في التهاب المفاصل الروماتويدي
لماذا الألم المفصلي المستعصي مهم
يتناول العديد من الأشخاص المصابين بالتهاب المفاصل الروماتويدي أدوية حديثة تُهدئ الجهاز المناعي، ومع ذلك تظل مفاصلهم مؤلمة ومتصلبة. يسأل هذا البحث لماذا لا يتحسن بعض المرضى حتى عندما يبدو أن الالتهاب في المفصل يتلاشى. من خلال فحص مكان وكيفية تشغيل خلايا داعمة معينة في المفصل لبرامج التندب، يكشف الباحثون عن شكل خفي من الضرر قد يفسر استمرار الألم ويشير إلى استراتيجيات علاجية جديدة.
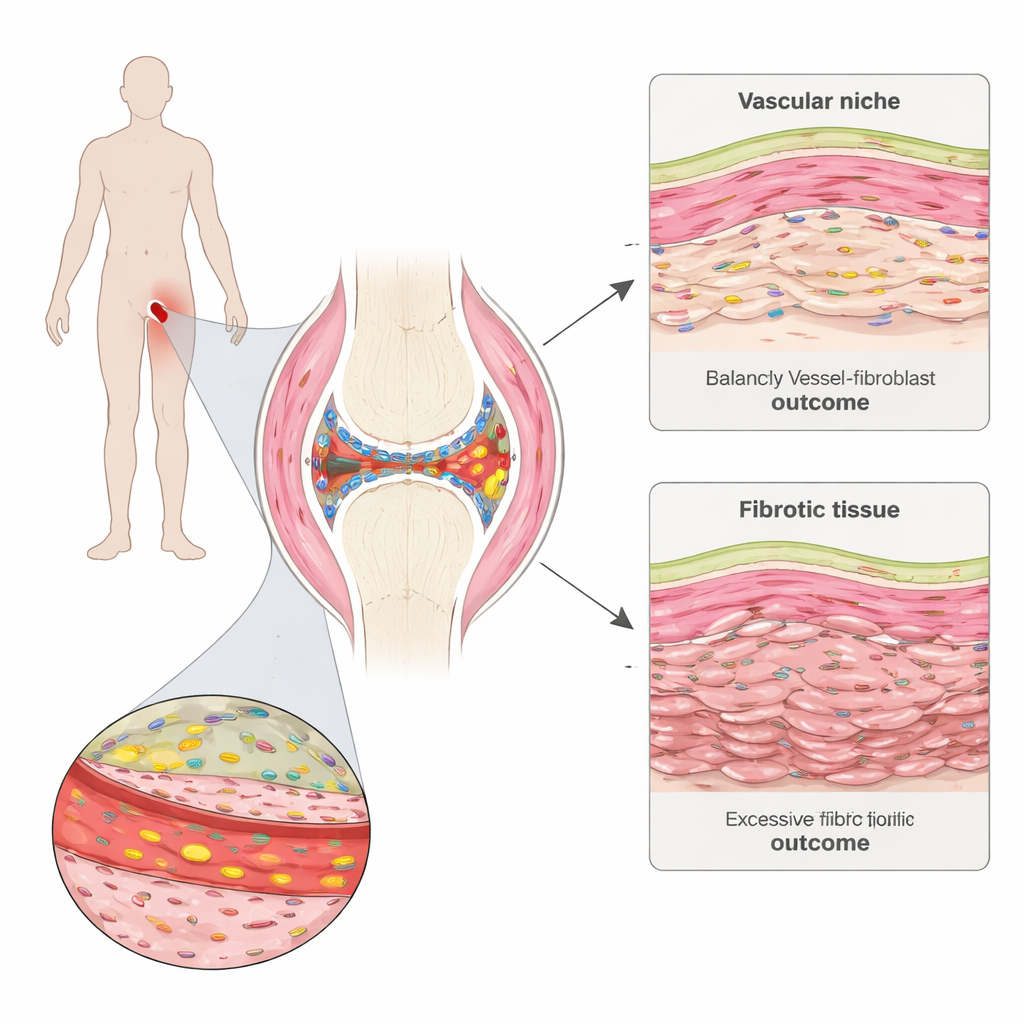
نظرة أقرب داخل المفصل المؤلم
يهاجم التهاب المفاصل الروماتويدي الغشاء الزلالي، نسيج رقيق يبطن المفاصل ويشحّمها. جمع الفريق خزعات زلالية صغيرة من أشخاص في مرحلة مبكرة من المرض قبل بدء العلاج ومرة أخرى بعد ستة أشهر. باستخدام خرائط جينية مكانية متقدمة، تمكنوا من رؤية الجينات النشطة في آلاف الخلايا الفردية مع الحفاظ على موضع تلك الخلايا في النسيج. حدّدوا «أحياء» مميزة في الغشاء الزلالي، بما في ذلك تجمعات الخلايا المناعية، ومناطق غنية بالدهون، والبطانة الداخلية الرقيقة، ومناطق مكتظة بالأوعية الدموية وخلايا تركيبية تُسمى الأرومات الليفية.
الخلايا المكوّنة للندبة ومقاومة العلاج
بالمقارنة بين المرضى الذين وصلوا لاحقًا إلى الهدأة والذين لم يصلوا، وجد الباحثون نمطًا بارزًا: قبل العلاج، كان لدى المرضى غير المتعافين إشارات أقوى للتليف النسيجي. ارتبط برنامج أرومة ليفية معين، ميزته إنتاج مرتفع لبروتين المصفوفة خارج الخلوية المسمى COMP، بالتوسع في هؤلاء المرضى. شاركت هذه الأرومات الغنية بـCOMP ميزات مع الخلايا المكوّنة للندبة المرصودة في تليف الرئة والجلد، وكانت مرتبطة بقوة بالاستجابة العلاجية الضعيفة. مع مرور الوقت، مالت المناطق المسيطر عليها من قبل هذه الخلايا إلى أن تصبح مكتظة بالنسيج الضام لكنها نسبياً فقيرة بالخلايا، ما يشير إلى أنها تودع مصفوفة صلبة قد تستمر حتى بعد زوال الالتهاب.
الأوعية الدموية كقادة خفيون
لم تكن الأرومات الليفية المولِّدة للتليف موزعة عشوائيًا. تجمعت حول الأوعية الدموية، مكونة نطاقات محيطة بالأوعية متعددة الطبقات. طبقة الأمام الأكثر تماسًا مع جدار الوعاء عبّرت عن جينات مختلفة عن الطبقة الخارجية. بيّن الفريق أن الخلايا الباطنة للأوعية تُرسِل إشارات نوتش إلى الأرومات الليفية المجاورة، والتي بدورها تشكل كيفية استجابة هذه الأرومات لعائلة من المؤثرات المروِّضة للتليف المعروفة باسم TGF‑beta. قرب الوعاء، تدفع إشارات نوتش الأرومات لإنتاج TGF‑beta لكنها في الوقت نفسه تقلّل عدد مستقبلات TGF‑beta على سطحها، مما يحد من حساسيتها. أبعد من ذلك، حيث يتلاشى تأثير نوتش، تحمل الأرومات مزيدًا من المستقبلات وتصبح شديدة الاستجابة، متحوِّلة إلى خلايا غنية بـCOMP تدفع التليف.
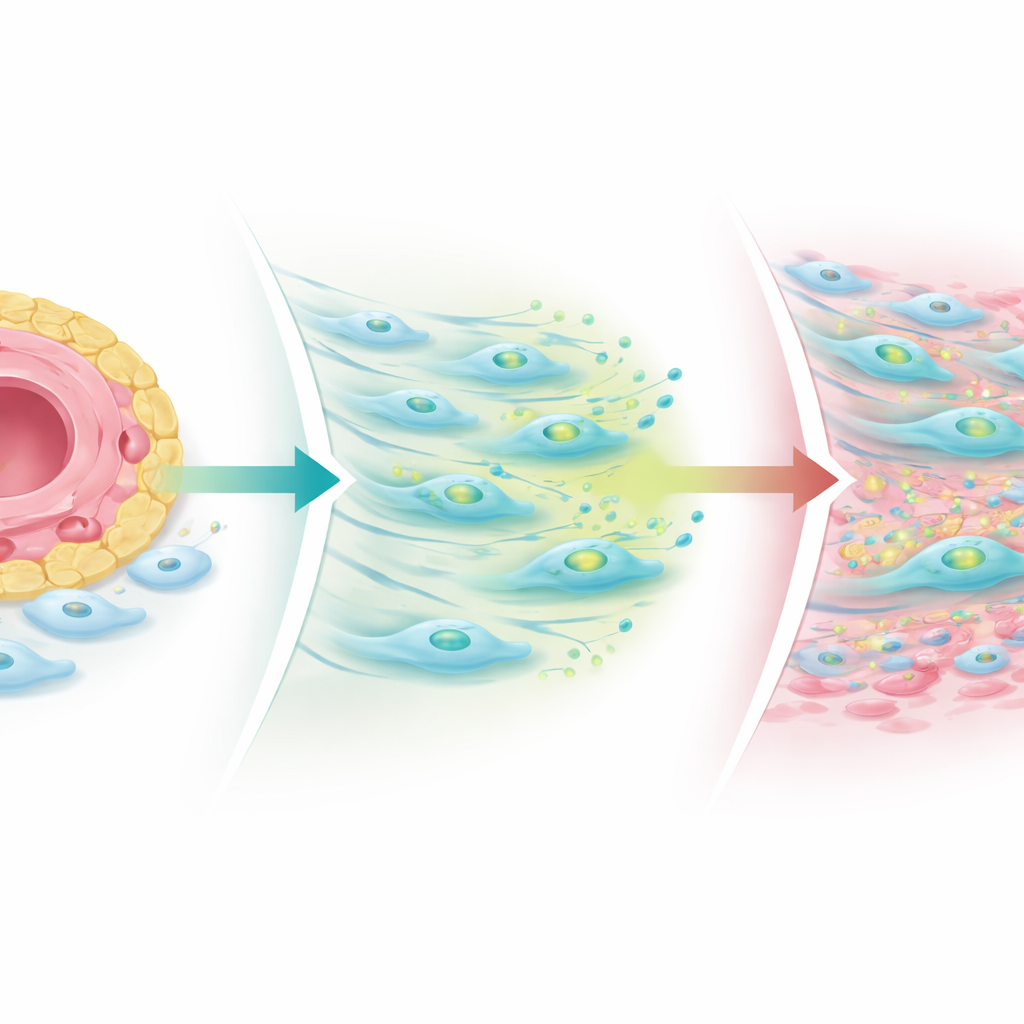
ماذا يحدث عندما ينكسر التوازن
بنى الباحثون نماذج مبسطة للمفصل في أطباق مخبرية وأورغانويدات ثلاثية الأبعاد مأخوذة من نسيج المرضى لاستقصاء هذه الآلية. عندما عززوا إشارات نوتش من الخلايا البطانية، زادت الأرومات من إنتاج TGF‑beta لكن خفّضت مستويات المستقبلات، مما حدّ من التندب. عندما أعاقوا نوتش أو أخلّوا بنمطه المستقر، استعادت الأرومات مستقبلات TGF‑beta—وخاصةً مستقبلًا مشاركًا يُدعى مستقبل TGF‑beta III—وتوسعت الخلايا الليفية المولِّدة للتليف الإيجابية لـCOMP بعيدًا عن الأوعية. في خزعات المرضى المأخوذة بعد العلاج، تقلصت تجمعات الخلايا المناعية لدى الجميع تقريبًا، لكن المواطن الليفية المولِّدة للتليف، لا سيما المناطق الغنية بـCOMP، غالبًا ما نمت، وخاصةً لدى من استمر ألم مفاصلهم. يشير هذا إلى أن الأدوية المضادة للالتهاب التقليدية يمكن أن تخمد «نار» المناعة بينما تترك وراءها أو تكشف عن عملية تليفية تحافظ على صلابة وألم المفاصل.
طرق جديدة لتهدئة المفاصل المستعصية
أخيرًا، اختبر الفريق ما إذا كان تعطيل هذه الدائرة المولِّدة للتليف قد يكون مفيدًا علاجيًا. في أورغانويدات مأخوذة من المرضى، قللت أدوية تُثبّط نوتش أو تحجب إشارة TGF‑beta من إنتاج COMP وبروتينات تندب أخرى وبعض الكولاجينات الرئيسية، وأعادت توصيل نشاط الجينات في المناطق المحيطة بالأوعية. للمتابع العام، الرسالة أن ليس كل الضرر في التهاب المفاصل الروماتويدي ناتج عن الالتهاب المرئي: بعضه «مُبرمج» في الخلايا الداعمة والأوعية الدموية داخل المفصل. باستهداف محادثة نوتش–TGF‑beta التي تتحكم في كيفية ترسيخ الأرومات الليفية لأنسجة الندبة، قد تمنع العلاجات المستقبلية أو تعكس شكلًا ليفيًا مستعصيًا من المرض يقاوم أدوية اليوم المركزة على المناعة.
الاستشهاد: Bhamidipati, K., McIntyre, A.B.R., Kazerounian, S. et al. Spatial patterning of fibroblast TGFβ signaling underlies treatment resistance in rheumatoid arthritis. Nat Immunol 27, 556–571 (2026). https://doi.org/10.1038/s41590-025-02386-2
الكلمات المفتاحية: التهاب المفاصل الروماتويدي, التليف, الأرومات الليفية, إشارة TGF-beta, مسار نوتش