Clear Sky Science · ar
هندسة الإنزيم زيلوزيل ترانسفيراز للتلاعب بالبروتيوغلِيكَانات في الخلايا الثديية
لماذا تغطية الخلايا مهمة
كل خلية في أجسامنا ترتدي «غطاء» جزيئي يساعدها على التواصل مع جيرانها واستشعار محيطها. جزء رئيسي من هذا الغطاء يتكوّن من بروتيوغلِيكَانات — بروتينات مزخرفة بسلاسل سكرية طويلة تعمل كأنتينات دقيقة لعوامل النمو والإشارات المناعية والإشارات البنائية. عندما يختلّ هذا التزيين السكري، قد تتعطّل عملية التطور وتتأثر أنسجة مثل العظام والعضلات بشدة. ومع ذلك، كافح العلماء لتحديد أي البروتينات تحمل هذه السلاسل بالضبط وكيف تؤثر مكونات الغطاء الفردية على سلوك الخلية. تقدم هذه الدراسة استراتيجية كيميائية دقيقة لوسم وإعادة بناء هذه السلاسل السكرية على خلايا ثديية حية، فاتحةً طريقًا لقراءة وإعادة كتابة المعلومات المشفرة على أسطحها. 
إعادة توصيل الخطوة الأولى لإرفاق السكر
يبدأ بناء البروتيوغلِيكَانات عندما يركّب طيف خاص من الإنزيمات، زيلوزيل ترانسفيرازات XT1 وXT2، السكر الأول على البروتين، محدِّدًا الموقع الذي ستنمو منه سلسلة طويلة. ونظرًا لأن كلا الإنزيمين قادران على أداء هذه الخطوة الأولى نفسها، فقد كان من الصعب معرفة أي البروتينات يعمل كل إنزيم عليها داخل الخلايا. استخدم المؤلفون تصميم «النتوء والثغرة» — شائع في الكيمياء الحيوية الحديثة — لحل هذه المشكلة. أعادوا تشكيل موقع الفعل في XT1 قليلًا، فخلقوا مساحة إضافية («الثغرة»)، وقدموا لبنة سكر مطابقة ولكن أكثر ضخامة قليلًا، 6AzGlc («النتوء»). يمكن الآن لـ XT1 المهندَسة أن تستخدم هذا السكر المعدَّل، بينما لا يستطيع الإنزيم الطبيعي ذلك، ما يتيح للباحثين وسم البروتينات التي تلامسها النسخة المعاد تصميمها فقط.
تهريب سكر مصمم إلى داخل الخلايا
لجعل هذه المقاربة تعمل في خلايا حية، اضطر الفريق إلى إيصال السكر المزخرف بصورة يتعرف عليها التمثيل الخلوي. بدلًا من الاعتماد على مسارات امتصاص السكر الطبيعية — التي لا تتعامل جيدًا مع نظائر الزايلوز — بنوا نسخة مخفية من 6AzGlc تحمل مجموعة فوسفات مخفية. بمجرد دخولها إلى السيتوزول، تكشف الإنزيمات الخلوية هذه المجموعة وتحوّل الجزيء إلى UDP‑6AzGlc، الشكل المنشط المطلوب من قبل زيلوزيل ترانسفيرازات المهندَسة. أكدت كروماتوغرافيا دقيقة أن الخلايا التي عولجت بالمركب المخفي المرتب بشكل صحيح أنتجت كميات كبيرة من السكر المصمم المنشط، في حين أن التحكم المرآتي أنتج القليل جدًا. 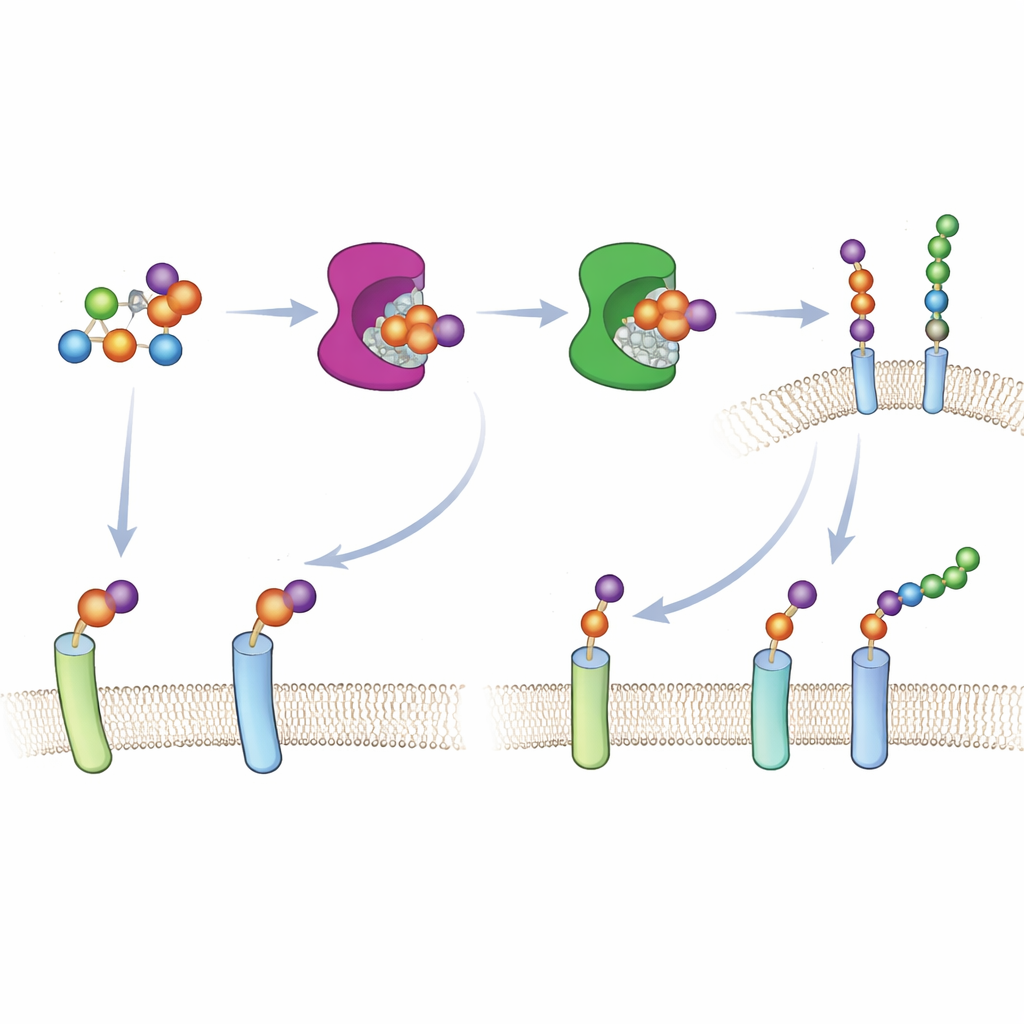
وسم وتحديد اللاعبين المخفيين
بوجود كلٍ من الإنزيم المعدَّل والسكر المنشط، أظهر الباحثون أن الخلايا التي تعبّر فقط عن XT1 أو XT2 المهندَسين هي التي دمجت وسم 6AzGlc في بروتيوغلِيكَانات سطحها. تعمل مجموعة الأزيد في 6AzGlc كمقبض كيميائي صغير يمكن «نقره» إلى صبغات متوهجة أو البيوتين، مما يتيح تصورًا وإثراءً للبروتينات الموسومة. كشفت التحليلات الطيفية للعينات المُثرّاة عن مجموعة غنية من البروتيوغلِيكَانات المعروفة — بما في ذلك ديكورين، عدة جليبيكانات، سنديكان‑4، CD44 وفيرسيكان — مؤكدة أن النظام يعلّم بروتينات حاملة حقيقية للسكريات. والأهم من ذلك، أن الإنزيمات المهندَسة حافظت على نفس تفضيلات التسلسل مثل نظرائها الطبيعية، ما يعني أن الوسم الكيميائي يُركب في مواقع الإرفاق الحقيقية بدلًا من مواقع جديدة اصطناعية.
بناء بروتيوغلِيكَانات مصممة
مكافأة غير متوقعة لوسم 6AzGlc هي أنه، على خلاف السكر البداية الطبيعي، لا يمكن تمديدها إلى سلسلة كاملة الطول بواسطة الإنزيمات اللاحقة. هذا يحدّ عمليًا من طول السلسلة ويُبسط البنية الجزيئية التي يجب تحليلها بواسطة الطيف الكتلي. حول المؤلفون هذه الخاصية إلى أداة: بعد أن يركّب XT1 6AzGlc في موقع إرفاق طبيعي، يستخدمون كيمياء النقر لربط شظايا صناعية من الهيبارين، مكوِّنين «بروتيوغلِيكَانات مصممة» ذات سلاسل سكرية محددة بدقة. في خلايا سرطان الثدي التي تفتقر إلى سنديكان‑1 الخاص بها، أعاد إدخال نسخ مصممة مشابهة انتشار الخلايا بشكل طبيعي على سطح مغطى بالبروتين، مثبتين أن البروتيوغلِيكَان المعاد بناؤه كيميائيًا يمكن أن يحلّ وظيفيًا محل الطبيعي.
ما معنى ذلك للأحياء والطب
تقدّم هذه الدراسة مجموعة أدوات قوية وُضعت لوضع علامات والتلاعب بشكل انتقائي بالسلاسل السكرية التي تتحكم في كيفية تواصل الخلايا. من خلال فصل أدوار XT1 وXT2 ووسم أهدافهما المباشرة فقط، يمكن للباحثين الآن رسم خريطة البروتيوغلِيكَانات العاملة في أنسجة وحالات مرضية محددة. كما أن القدرة على إيقاف نمو السلسلة الطبيعية واستبدالها بسكريات مُصممة تتيح للعلماء تفكيك أي مقدار من وظيفة البروتيوغلِيكَان يُحمل بواسطة العمود البروتيني مقابل غطائه السكري. على المدى الطويل، قد تساعد مثل هذه الهندسة الدقيقة في فك شيفرة الإشارات المعقدة على سطح الخلية وإلهام علاجات تصلح أو تعيد برمجة الأغطية الخلوية المعيبة في اضطرابات التطور والسرطان وأمراض أخرى.
الاستشهاد: Li, Z., Chawla, H., Di Vagno, L. et al. Xylosyltransferase engineering to manipulate proteoglycans in mammalian cells. Nat Chem Biol 22, 612–621 (2026). https://doi.org/10.1038/s41589-025-02113-w
الكلمات المفتاحية: بروتيوغلِيكَانات, جليكوسامينوغليكانات, زيلوزيل ترانسفيراز, الكيمياء الحيوية, إشارات سطح الخلية