Clear Sky Science · ar
موقع متغاير واحد يجمع التنشيط والتعديل والكبت في TRPM5
كيف يشكّل حارس صغير الطعم والتمثيل الغذائي
الأطعمة التي نستمتع بها وكيف يتعامل جسدنا مع السكر يعتمدان على بروتينات «حارسة» مجهرية داخل خلايانا. أحد هذه الحراس، قناة تُدعى TRPM5، يساعدنا على استشعار النكهات الحلوة والمرّة والأُميامي ويساعد البنكرياس على إفراز الإنسولين. تكشف هذه الدراسة كيف أن جيبًا صغيرًا واحدًا على TRPM5 يمكن أن يعمل كزر تحكم رئيسي، يشغل القناة أو يضبط حساسيتها أو يغلقها — رؤى قد توجه علاجات مستقبلية لمرض السكري والسمنة واضطرابات الأمعاء.
قناة عند تقاطع الطعم وسكر الدم
توجد TRPM5 في أغشية خلايا التذوق على اللسان، وخلايا إفراز الهرمونات في الأمعاء، وخلايا إفراز الإنسولين في البنكرياس. عند ارتفاع مستويات الكالسيوم داخل هذه الخلايا، تفتح TRPM5 وتسمح بتدفق الأيونات الموجبة، مسببًة تغييرًا عرضيًا في جهد الخلية. في براعم التذوق، تخبر هذه الإشارة الكهربائية الدماغ بوجود طعم حلو أو مرّ أو أومامي على اللسان. في البنكرياس، تساعد على ضبط دفعات الإنسولين بعد الوجبة. الأشخاص والحيوانات ذات وظائف TRPM5 المتأثرة تظهر مشاكل في إفراز الإنسولين والتحكم بمستوى السكر في الدم، مما يشير إلى أن عقاقير تستهدف TRPM5 قد تساعد يومًا ما في علاج اضطرابات التمثيل الغذائي. ومع ذلك، حتى وقت قريب، افتقر الباحثون إلى أدوات دقيقة لتشغيل هذه القناة أو إيقافها.
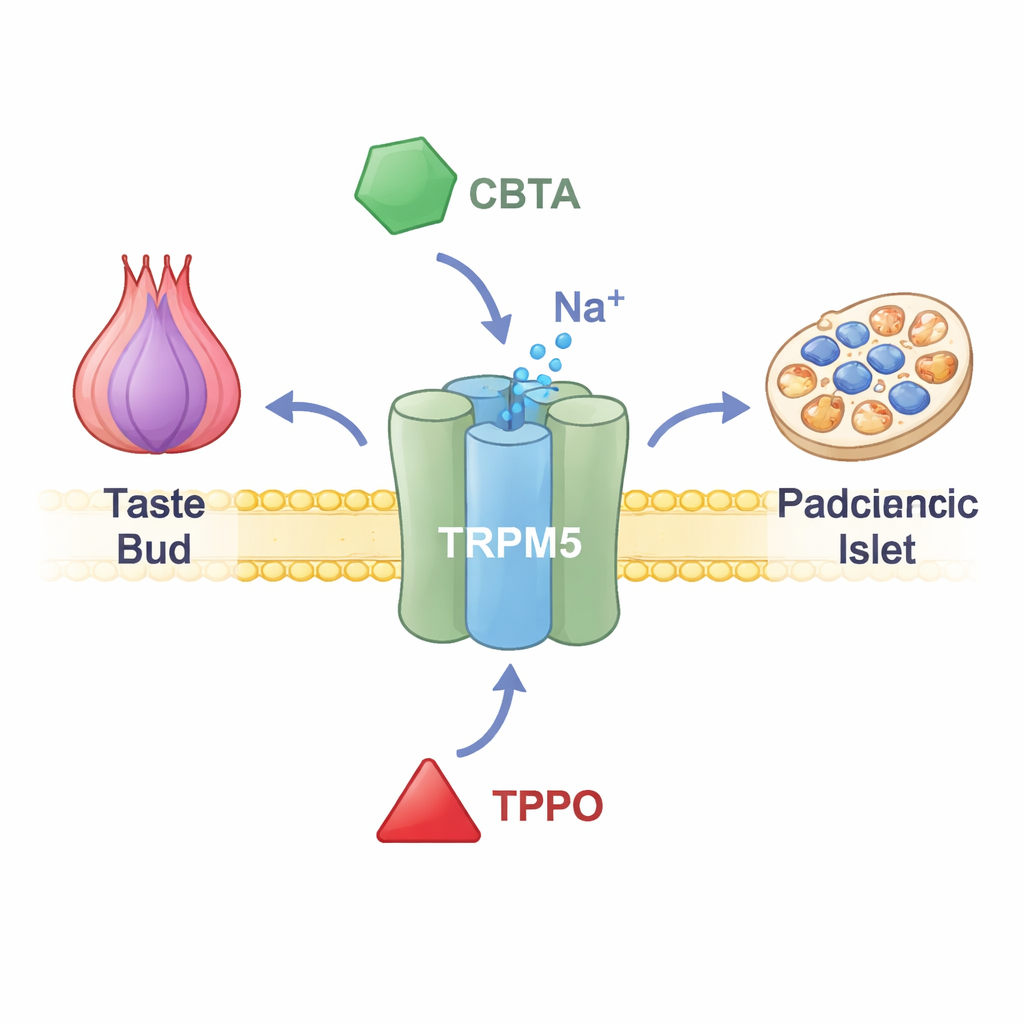
مفتاح كيميائي جديد يعزز القناة بقوة
ركز الباحثون على مركب صناعي يُدعى CBTA، المعروف سابقًا بتحفيز TRPM5 لكنه كان غير مفهوم جيدًا. باستخدام تسجيلات كهربائية من خلايا مُهندَسة لإنتاج TRPM5، أظهروا أن CBTA يمكنه فتح القناة حتى عندما يكون الكالسيوم شبه غائب، مما يثبت أنه يعمل كمُنَشّط حقيقي وليس مجرد معزز لتأثيرات الكالسيوم. عندما تتواجد كميات ضئيلة من الكالسيوم — مستويات عادة ما تترك TRPM5 هادئة — يتعاون CBTA والكالسيوم ليولدا تيارات أكبر بكثير من كل واحد بمفرده. هذا يعني أن CBTA يجعل TRPM5 حساسًا للغاية، بحيث أن مستويات الكالسيوم القريبة من الحالة الراسية تصبح كافية فجأة لقلب القناة مفتوحة تمامًا.
جيب تحكم مخفي كشفته ميكروسكوبيّة التبريد الإلكتروني
لمعرفة كيف يعمل ذلك بتفصيل ذري، استخدم الفريق المجهر الإلكتروني بالتبريد لالتقاط لقطات ثلاثية الأبعاد لـ TRPM5 في ظروف مختلفة. اكتشفوا أن CBTA يستقر في تجويف لم يُلاحظ سابقًا في الجزء العلوي من منطقة استشعار الجهد في القناة، فوق المكان الذي يرتبط فيه الكالسيوم عادةً. يتكوّن هذا التجويف من مجموعة من الأحماض الأمينية ويعمل كموقع تثبيت دقيق. عندما غير العلماء اللبنات الأساسية التي تبطن هذا الجيب، لم يعد بإمكان CBTA تنشيط TRPM5، رغم أن الكالسيوم ظل يعمل، مما يؤكد أن هذه الفتحة الضئيلة ضرورية لعمل الدواء. ومن اللافت أن ارتباط CBTA يُعيد ترتيبًا طفيفًا للأجزاء المجاورة من البروتين بطريقة تجعل من السهل جدًا للكالسيوم أن يحتل موضعه الاعتيادي، مفسرًا التآزر الدرامي الملحوظ في القياسات الكهربائية.
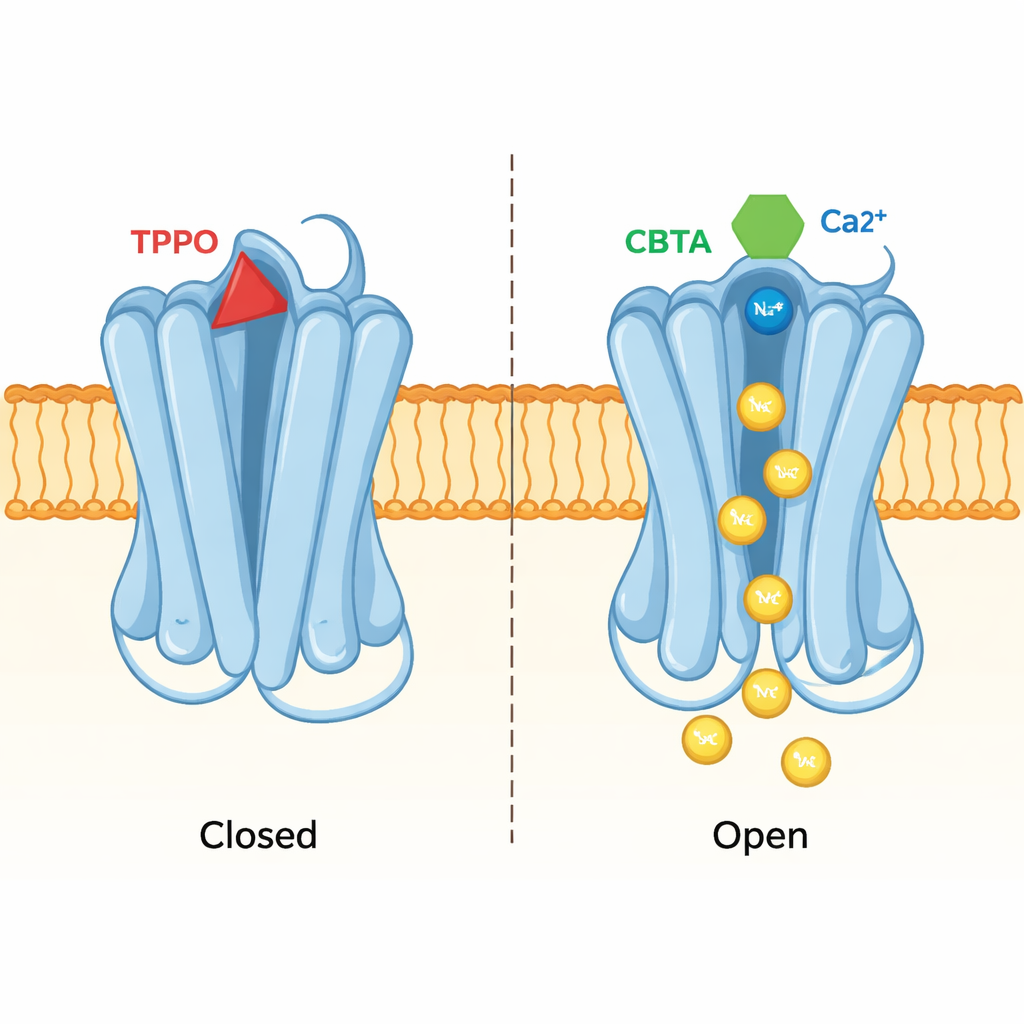
جيب واحد، نتيجتان متعاكستان
أظهر نفس النهج البنيوي كيف أن مثبطًا يُدعى TPPO يستخدم نفس الجيب تمامًا لإحداث التأثير المعاكس. عندما يرتبط TPPO، تظل مواقع الكالسيوم على TRPM5 مشبعة، لكن المسلك المركزي للقناة يبقى مضغوطًا ومغلقًا ولا تمر أي أيونات. مقارنات بين الهياكل المرتبطة بـ TPPO وCBTA أظهرت أن أشكالهما المختلفة تؤثران على مقاطع قريبة من البروتين في اتجاهين متعاكسين. يشجع CBTA حركات تنتشر إلى المسلك وتفتحه؛ بينما يعطل TPPO بدلاً من ذلك التواصل بين الجيب والمسلك، محافظًا على البوابة مغلقة. في الجوهر، يمكن لهذا الجيب الوحيد أن يعمل إما كمسَرِّع أو ككابح، اعتمادًا على الجزيء المحتل له.
إعادة توجيه الأسلاك الداخلية للقناة
تُظهر الدراسة أيضًا أن هذا الجيب المسيطر يمكنه تولّي وظائف تُؤدى عادةً بواسطة منطقة ربط الكالسيوم المنفصلة داخل الخلية. في قنوات مُطفَّلة حيث تم تعطيل موقع الكالسيوم الداخلي المعتاد، لم يتمكن الكالسيوم وحده من فتح TRPM5. ومع ذلك، ما زال CBTA يبدّل هذه الطفرات ويشغّلها ويعيد تشكيل عنصر بنيوي رئيسي يربط أجزاء القناة الداخلية والخارجية. في طفرات أخرى تكسر الوصلة بين ربط الكالسيوم وفتح المسلك، أعاد إضافة CBTA السلوك الطبيعي. تكشف هذه النتائج أن الموقع المكتشف حديثًا يمكنه إعادة توجيه أو إصلاح الاتصال بين مجالات القناة المختلفة، ليعمل كمحور مرن للإشارات بعيدة المدى داخل البروتين.
لماذا يهم هذا بالنسبة للأدوية المستقبلية
لغير المختصين، الرسالة الأساسية هي أن الباحثين وجدوا جيبًا واحدًا حساسًا للأدوية على TRPM5 يمكنه دمج التنشيط وضبط الحساسية والإغلاق. يمكن لمُنَشِّط صغير مثل CBTA أن يحاكي الكالسيوم ويزيد من حساسية القناة بشكل كبير، بينما يمكن لمركب آخر، TPPO، أن يثبت نفس القناة مغلقة، وكل ذلك عن طريق الارتباط في نفس الموضع. تفتح هذه الصورة الموحدة لكيفية التحكم في TRPM5 الباب أمام تصميم جزيئات مُصممة خصيصًا لتعزيز نشاطها أو تقليله في أنسجة محددة، مع تطبيقات محتملة تمتد من تحسين العلاجات القائمة على الطعم وأدوية حركة الأمعاء إلى تطوير استراتيجيات جديدة لإدارة سكر الدم واضطرابات التمثيل الغذائي.
الاستشهاد: Ruan, Z., Lee, J., Li, Y. et al. A single allosteric site merges activation, modulation and inhibition in TRPM5. Nat Chem Biol 22, 402–410 (2026). https://doi.org/10.1038/s41589-025-02097-7
الكلمات المفتاحية: قناة TRPM5, إدراك الطعم, إفراز الإنسولين, بوابة قنوات الأيونات, التعديل المتغاير