Clear Sky Science · ar
تحليلات الارتباط على مستوى الجينوم لقصور الغدة الدرقية المناعي الذاتية تكشف مساهمات مناعية ومحددة للدرقية وعلاقة عكسية مع خطر السرطان
لماذا يهم هذا للصحة اليومية
يشعر كثير من الناس بالتعب أو البرودة أو الضبابية الذهنية دون إدراك أن سبب ذلك قد يكون غدة درقية ضعيفة. يؤثر قصور الغدة الدرقية المناعي الذاتي، حيث يهاجم جهاز المناعة الغدة الدرقية تدريجياً، على أكثر من شخص من بين كل عشرين. تستخدم هذه الدراسة بيانات وراثية من مئات الآلاف من المتطوعين للإجابة على سؤالين كبيرين: ما التغييرات الوراثية الموروثة التي تزيد احتمال الإصابة بهذه الحالة؟ وكيف ترتبط هذه التغييرات نفسها بخطر الإصابة بالسرطان؟ تكشف الإجابات عن مفاضلة مفاجئة بين جهاز مناعي قد يضره أحياناً ويتلف الغدة الدرقية لكنه في المقابل قد يوفر حماية إضافية ضد الأورام.
نظرة عبر كامل الجينوم
جمع الباحثون السجلات الصحية والمعلومات الوراثية من مشروعين سكانيين كبيرين، FinnGen في فنلندا وUK Biobank في المملكة المتحدة. ركزوا على الأشخاص الذين احتاجوا إلى علاج طويل الأمد بهرمون الغدة الدرقية واستبعدوا بعناية أولئك الذين كانت مشاكل الغدة الدرقية لديهم ناتجة عن جراحة أو سرطان أو أسباب غير مناعية. أسفرت هذه الفلترة عن أكثر من 81,000 حالة من قصور الغدة الدرقية المناعي الذاتي وأكثر من 700,000 ضابط، مما يجعلها أكبر دراسة لهذه الحالة حتى الآن. عبر مسح ملايين العلامات الوراثية في كامل الجينوم، كشفوا عن 418 إشارة وراثية مستقلة خارج مجموعة الجينات المناعية الكبرى، موزعة على ما لا يقل عن 280 منطقة في الجينوم. شاركت العديد من هذه الإشارات تغييرات نادرة أو منخفضة التردد في الحمض النووي تُغير بنية البروتينات، مما يوفر أدلة مباشرة على الآليات البيولوجية الكامنة.
فصل التأثيرات المناعية العامة عن تلك الخاصة بالدرقية
يقع قصور الغدة الدرقية المناعي الذاتي عند تقاطع المناعية الذاتية العامة والبيولوجيا الخاصة للغدة الدرقية. لفصل هذين العنصرين، قارن الفريق نتائجهم مع دراسات وراثية لأمراض مناعية ذاتية أخرى ومع مستويات هرمون المنبه للغدة الدرقية في الدم، وهو العلامة السريرية الأساسية المستخدمة للكشف عن قصور الغدة الدرقية. باستخدام طريقة تصنيف بايزية، جمّعوا الإشارات الوراثية إلى مجموعات تلك المشتركة مع أمراض مناعية واسعة وتلك الأكثر تحديداً لتنظيم هرمونات الدرقية. قدّروا أن نحو 38% من الإشارات تعمل عبر مسارات مناعية عامة تؤثر على العديد من الحالات المناعية الذاتية، بينما نحو 20% تعمل أساساً عبر وظيفة الغدة الدرقية نفسها. كانت المتغيرات المرتبطة بالدرقية تميل إلى التأثير في مستويات الهرمون والجينات النشطة في نسيج الغدة الدرقية، في حين كانت المتغيرات المناعية العامة أكثر نشاطاً في الخلايا التائية، وهي خلايا الدم البيضاء التي تنسق الاستجابات المناعية.
تكبير منظور مفتاح مناعي
شملت إحدى النتائج اللافتة تغيراً نادراً في الحمض النووي في جين ZAP70، الذي يشفر بروتين إشارة أساسي داخل الخلايا التائية. من المعروف أن العيوب الشديدة في هذا البروتين تسبب نقصاً مناعياً عميقاً، لكن المتغير المحدد هنا يؤدي إلى فقدان جزئي فقط في الوظيفة. أظهرت تجارب مخبرية في خلايا تائية مُهندَسة أن هذا التغير في ZAP70 يضعف، لكنه لا يوقف تماماً، سلسلة الإشارات التي تتبع عادةً تعرف المستهدف. كانت الخلايا الحاملة للمتغير أقل قدرة على تشغيل علامات التفعيل وخطوات الإشارة التالية. يبدو أن هذا التراجع في الاستجابة يخل بالتوازن الدقيق الذي يقصّي عادة الخلايا التائية ذاتية التفاعل، مما يمهّد حاملة المتغير للإصابة بأمراض مناعية ذاتية بينما يزيد أيضاً بشكل طفيف من خطر تعرضهم لبعض أشكال القصور المناعي.
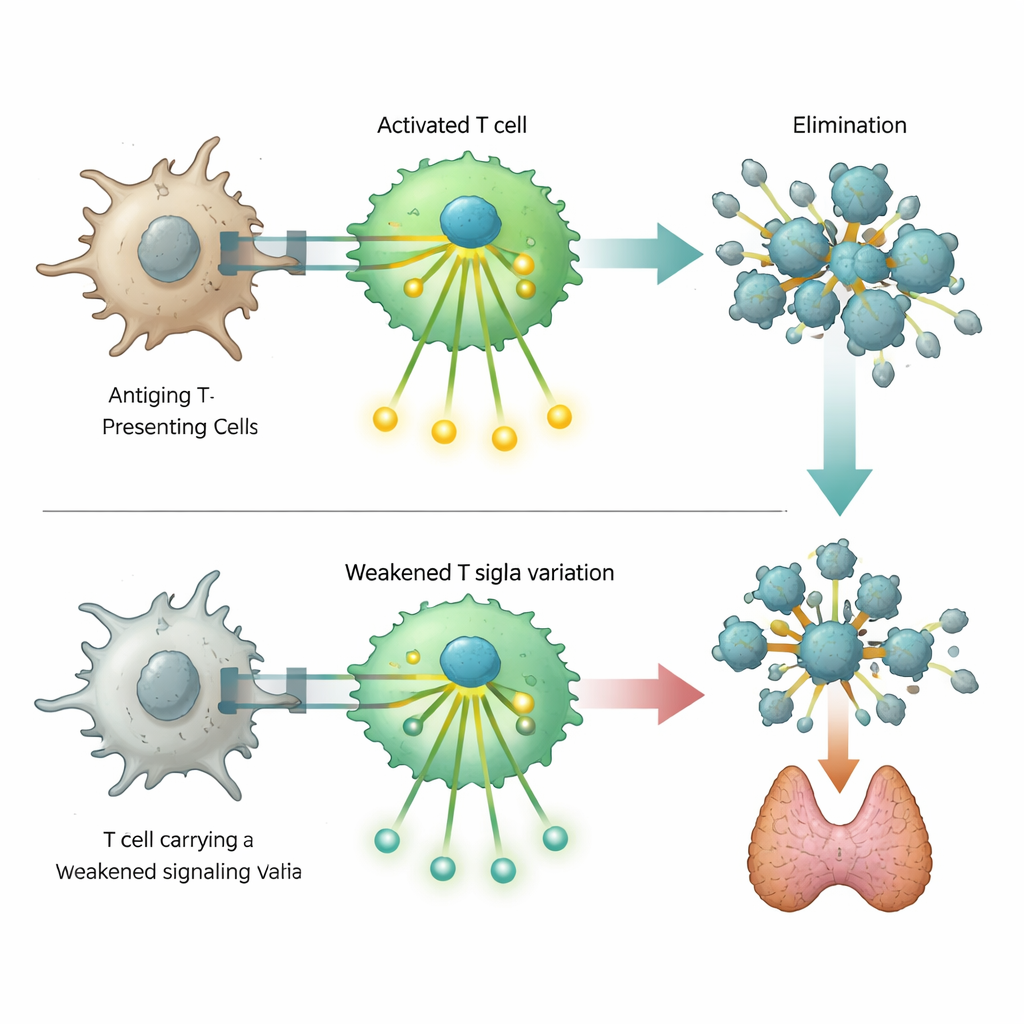
صلة غير متوقعة بحماية من السرطان
بما أن المسارات المناعية نفسها التي تحفز المناعية الذاتية قد تهاجم أيضاً الأورام، سأل المؤلفون بعد ذلك كيف ترتبط جينات قصور الغدة الدرقية المناعي بخطر السرطان. حسبوا درجة مخاطر بوليجينية تلخّص ميول كل شخص الموروثة تجاه القصور الدرقي واختبروا ارتباطها بالعديد من الأمراض في بيانات فنلندا. كما كان متوقعاً، ارتبطت الدرجة الأعلى بزيادة خطر حالات مناعية ذاتية متنوعة. وما كان أكثر إثارة للانتباه هو نمط ثابت من انخفاض خطر عدة أنواع من السرطان، خصوصاً سرطان الخلايا القاعدية وسرطانات الجلد الأخرى، وكذلك سرطان الثدي وسرطان البروستاتا وتجميع شامل «كل السرطانات». عندما نظر الفريق مباشرةً إلى دراسات شاملة للسرطان على مستوى الجينوم، وُجد أن نحو 10% من المواقع المرتبطة بالقصور الدرقي أثّرت أيضاً على سرطان الجلد، مع أن المتغير الوراثي نفسه عادة ما يزيد المناعية الدرقية الذاتية بينما يقلل من خطر سرطان الجلد. كانت هذه المتغيرات المشتركة متركزة في جينات متعلقة بالمناعة، بما في ذلك أهداف دوائية معروفة تُستخدم في علاجات تفقد كابح المناعة (checkpoint immunotherapy).
ماذا يعني هذا للمرضى والطب
من منظور مبسط، تُظهر هذه الدراسة أن بعض الأشخاص يولدون بأجهزة مناعية مائلة إلى النشاط قليلاً، مما يجعلهم أكثر عرضة لضرر بطيء وغالباً صامت للغدة الدرقية، ولكن في نفس الوقت أفضل قدرة على اكتشاف والقضاء على السرطانات الناشئة. تفصل الدراسة التغييرات الجينية التي تعمل عبر فرط نشاط مناعي عام عن تلك التي تؤثر تحديداً على إنتاج هرمونات الدرقية، موضحة لماذا يمكن أن تشترك حالات مثل داء هاشيموتو وداء غريفز في بعض جينات الخطر ومع ذلك تدفع وظيفة الغدة الدرقية في اتجاهين متعاكسين. كما تساعد في تفسير سبب استجابة المرضى الذين يطورون مشكلات درقية أثناء تلقي أدوية معززة للمناعة لعلاج السرطان بشكل أفضل في كثير من الأحيان لتلك العلاجات. عموماً، تشير النتائج إلى أن التغايرات الطبيعية الشائعة في جينات نقاط التفتيش المناعية والإشارة تشكل كل من مرض الغدة الدرقية المناعي وخطر السرطان sepanjang الحياة، مما يقدّم دلائل جديدة للوقاية واستخدام أكثر تخصيصاً للعلاج المناعي.
الاستشهاد: Reeve, M.P., Kanai, M., Graham, D.B. et al. Genome-wide association analyses of autoimmune hypothyroidism reveal autoimmune and thyroid-specific contributions and an inverse relationship with cancer risk. Nat Genet 58, 550–559 (2026). https://doi.org/10.1038/s41588-026-02521-1
الكلمات المفتاحية: قصور الغدة الدرقية المناعي الذاتي, أمراض الغدة الدرقية, المخاطر الوراثية, الجهاز المناعي, حماية من السرطان