Clear Sky Science · ar
جليكوان آر إن إيه المرتبط بالسلفات الهيباران ينظّم إشارات VEGF-A
كيف تضبط الخلايا إشارات الأوعية الدموية في الجسم بدقة
الأوعية الدموية لا تظهر بشكل عشوائي حيثما تظهر إشارات النمو — بل يجب ضابطتها بدقة لتغذية الأنسجة من دون تغذية الأورام أو التسبب بالعمى. تكشف هذه الورقة العلمية عن «مكبح» غير متوقع لإشارة نمو رئيسية تسمى VEGF-A. يظهر الباحثون أن قطعاً صغيرة من الحمض النووي الريبي، التي تزيّن سطح الخلايا بالشراكة مع سكريات وبروتينات، تستطيع تخفيض رسالة VEGF-A، معيدة تشكيل فهمنا للغة التي تستخدمها الخلايا على أسطحها.
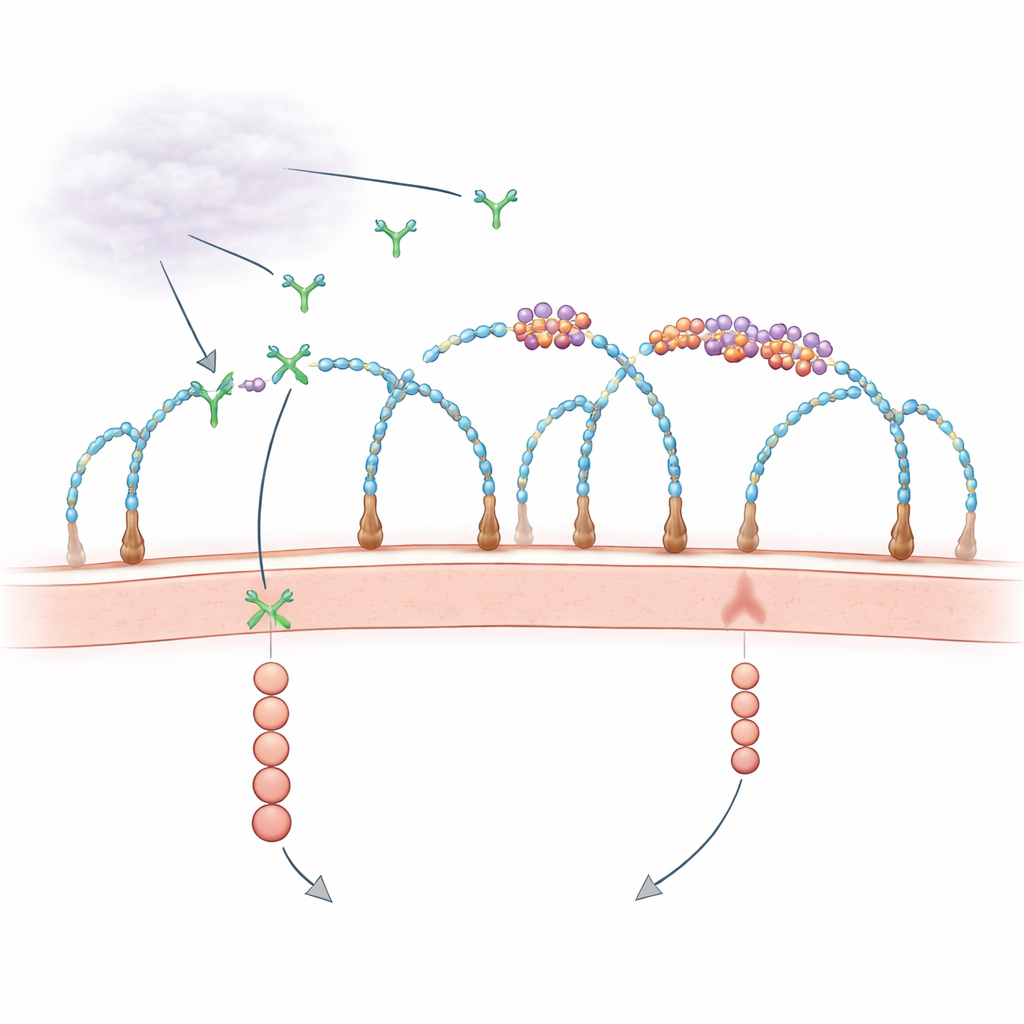
دور مفاجئ للحمض النووي الريبي على سطح الخلية
لعقود، عرف علماء الأحياء أن الغلاف الخارجي للخلية، الغني بالبروتينات المزينة بالسكريات والمعروفة ببروبتيغليكانات سلفات الهيباران، يساعد في التقاط عوامل النمو وتقديمها لمستقبلاتها. في الوقت ذاته، لمحات متفرقة ألمحت إلى أن شظايا RNA خارج الخلايا قد تؤثر على نمو الأوعية الدموية، لكن الجهات والآليات كانت غير واضحة. كشفت أعمال حديثة أن بعض الجزيئات الصغيرة من RNA ترتبط كيميائياً بسكريات معقدة لتكوّن «جليكوان آر إن إيه»، وأن بروتينات رابطة للـRNA تظهر أيضاً على سطح الخلية وتتشكل مع هذه الـRNA في مجموعات. تسأل الدراسة الجديدة سؤالاً محدداً: هل تتحكم هذه الجزر الصغيرة من RNA-بروتين على الغشاء فعلاً في كيفية استقبال إشارات النمو مثل VEGF-A؟
بناء جزر مجمّعة من RNA وبروتينات مع سلاسل سكرية
باستخدام شاشات تعطيل جيني شاملة عبر CRISPR ومجهرية عالية الدقة، اكتشف الباحثون أن سلاسل سكرية محددة — سلفات الهيباران المزينة بتشكيلات كبريتات معينة — تشكّل هياكل أساسية ضرورية لتجمع هذه الكتل من RNA-بروتين، التي أطلقوا عليها اسم ريبونوكليوبروتينات سطحية خلوية (csRNPs). عندما تمت إزالة الإنزيمات الأساسية المسؤولة عن بناء أو كبريتات سلفات الهيباران، اختفت مجموعات الجليكوان آر إن إيه وشركائها البروتينية من سطح الخلية، رغم أن الـRNA والبروتينات بقيت موجودة داخل الخلايا. إنزيمات تقص سلاسل سلفات الهيباران من السطح أو عوامل كيميائية تحجب الكبريتات أعطت نفس النتيجة. تظهر هذه النتائج أن سلاسل سلفات الهيباران السليمة والمكبّرة تنظّم csRNPs إلى جزر بحجم النانومتر عند الغشاء.
مجموعات الـRNA تعمل كمكابح لإشارة قوية لنمو الأوعية
انتقل الفريق بعدها إلى خلايا بطانة بشرية، وهي الخلايا المبطنة للأوعية الدموية والمستجيبة لـVEGF-A. وجدوا أن هذه الخلايا تعرض أيضاً مجموعات csRNP مثبتة على سلفات الهيباران. معالجة الخلايا الحية بـRNases، وهي إنزيمات تهضم الـRNA، أزالت عنصر الـRNA دون أن تزعزع السلاسل السكرية الأساسية. في تلك الظروف، شكل VEGF-A165، الشكل الأكثر شيوعاً وذي قدرة الارتباط بالهيباران، تنشيطاً أقوى بكثير لمسار الإشارة ERK المتدفق للأسفل، بينما الشكل الأقصر الخالي من ذيل ربط الهيباران (VEGF-A121) لم يتأثر. ارتبط عدد أكبر من جزيئات VEGF-A165 بسطح الخلية بعد إزالة الـRNA، ومع ذلك بقيت مستويات المستقبلات ثابتة. في أجهزة مجهرية ثلاثية الأبعاد ذات تدفق، نمت خلايا البطانة المعالجة بـRNase أبعد داخل هلام الكولاجين وشكلت هياكل أنبوبية بشكل أقوى، مما يشير إلى أن تدمير الـRNA السطحي يطلق سلوكاً محفزاً لتكوين الأوعية.
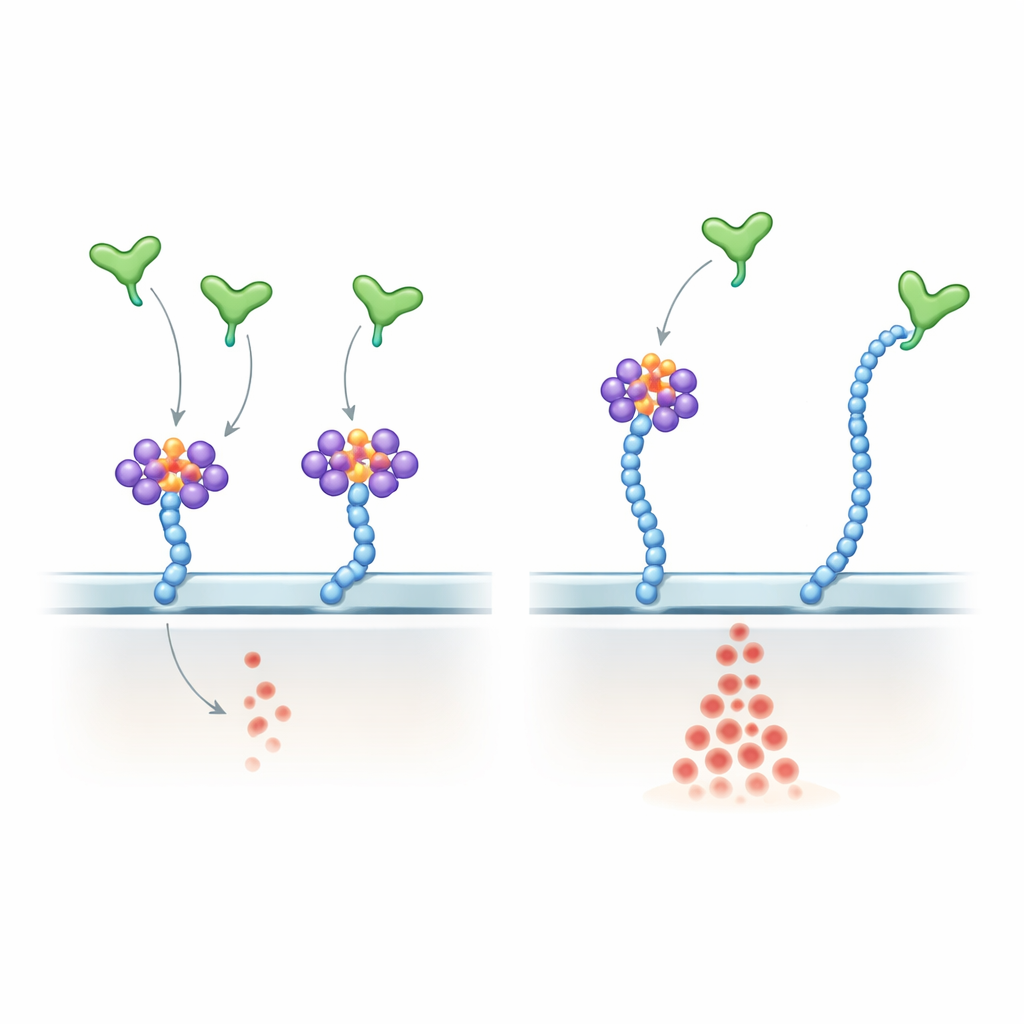
تفكيك كيفية استشعار VEGF-A للـRNA مقابل السكّر
لاستكشاف الآلية، أظهر المؤلفون أن VEGF-A165 يرتبط مباشرة ببعض الجزيئات الصغيرة من RNA، بما في ذلك العديد من جليكوان آر إن إيه المعروفة، عبر منطقته الكربوية‑النهائية موجبة الشحنة — نفس المنطقة التي ترتبط بسلفات الهيباران. قاموا بتعديل طفيف في VEGF-A165 استبدل فيه بقايا أرجينين أساسية في هذا الذيل بلايسين. حافظ المتحول على شحنته الموجبة العامة وما زال يلتقط سلاسل سلفات الهيباران، لكنه ارتبط بجليكوان آر إن إيه بشكل ضعيف وأصبح إلى حد كبير غير حساس لمعالجة RNase. في خلايا البطانة، أنتج المتحول تنشيط ERK أقوى وأكثر مقاومة لـRNase من VEGF-A165 الطبيعي، محاكياً بشكل وثيق تأثير إزالة الـRNA من سطح الخلية. في فئران حية، أدى حقن المتحول في العين إلى نمو شبكي حشوي أوعية أكثر ازدهاراً مقارنةً بالبروتين الطبيعي. في أجنة سمك الزَبْرَدْي، أدى الإفراط في التعبير عن النسخة المتحولة من Vegfa إلى تعطيل نمطية الأوعية وزيادة أعداد خلايا البطانة.
من الآلية الأساسية إلى دلالات أوسع
أخيراً، أظهر المؤلفون أن ربط ذيل ربط الهيباران من VEGF-A إلى بروتين إشارية غير ذي صلة، Wnt3a، يمكنه إعادة توجيه نشاط Wnt: إرفاق الذيل الطبيعي قلل التغيرات التطورية المدفوعة بـWnt، في حين أن إرفاق الذيل غير الحساس للـRNA عززها. تدعم هذه التجارب نموذجاً تقضي أن تجمعات csRNP، المثبتة بواسطة سلفات هيباران مخصصة، ترتبط بـVEGF-A والعوامل المماثلة لكبح نشاطها. عندما يزول مكوّن الـRNA أو تفقد عوامل النمو القدرة على استشعار الـRNA، يميل التوازن نحو إشارات أقوى وتطوّر وعائي متغير عبر عدة أنواع.
لماذا هذا مهم للصحة والعلاجات المستقبلية
لغير المتخصص، الرسالة الأساسية هي أن الخلايا تستخدم ليس البروتينات والسكريات فحسب، بل أيضاً جزيئات RNA الصغيرة المعروضة على سطحها لضبط إشارات نمو قوية مثل VEGF-A بدقة. هذه التجمعات من RNA‑بروتين المثبتة بالسكّر تعمل كمكابح قابلة للضبط على تكوين الأوعية، مما يساعد على ضمان أن الأوعية الجديدة تنبت في المكان والزمان المناسبين. إضعاف هذا التوازن — بواسطة تحلل الـRNA السطحي أو تغيير خصائص ربط الـRNA لعوامل النمو — يمكن أن يضخم أو يوجه نمو الأوعية بشكل خاطئ. قد يفتح فهم هذه الطبقة الضابطة المكشوفة حديثاً الباب أمام علاجات تضبط التكوّن الوعائي بدقة أكبر في السرطان، وأمراض العين، وشفاء الجروح، والطب التجديدي عن طريق استهداف الـRNA السطحي أو هياكله السكرية أو مناطق استشعار الـRNA في عوامل النمو.
الاستشهاد: Chai, P., Kheiri, S., Kuo, A. et al. GlycoRNA complexed with heparan sulfate regulates VEGF-A signalling. Nature 651, 808–818 (2026). https://doi.org/10.1038/s41586-025-10052-8
الكلمات المفتاحية: تكوّن الأوعية الدموية, عامل نمو بطانة الأوعية الدموية, سلفات الهيباران, حمض رibonucleic على سطح الخلية, جليكوان آر إن إيه