Clear Sky Science · ar
تفكيك شبكات تنظيم الجينات التي تتحكم في مصير خلايا القشرة البشرية
كيف تقرر خلايا الدماغ السلفية ما الذي ستصبحه
قبل ولادتنا، يُبنى دماغنا من مجموعة صغيرة من الخلايا الشبيهة بالجذور التي يتعين عليها أن تقرر ما إذا كانت ستواصل الانقسام أم ستتحول إلى أحد أنواع الخلايا العصبية والخلايا المساعدة المتعددة. مفاتيح صغيرة في حمضنا النووي، تُسمى عوامل تنظيم الجينات، توجه هذه الخيارات. تُظهر هذه الدراسة، بتفصيل غير معتاد، كيف تتعاون عشرات من هذه المفاتيح لتشكيل القشرة البشرية النامية—منطقة الدماغ المسؤولة عن التفكير والإحساس والذاكرة—وكيف يمكن لأعطاب في هذه الضوابط أن تُسهِم في اضطرابات عقلية ونمائية.
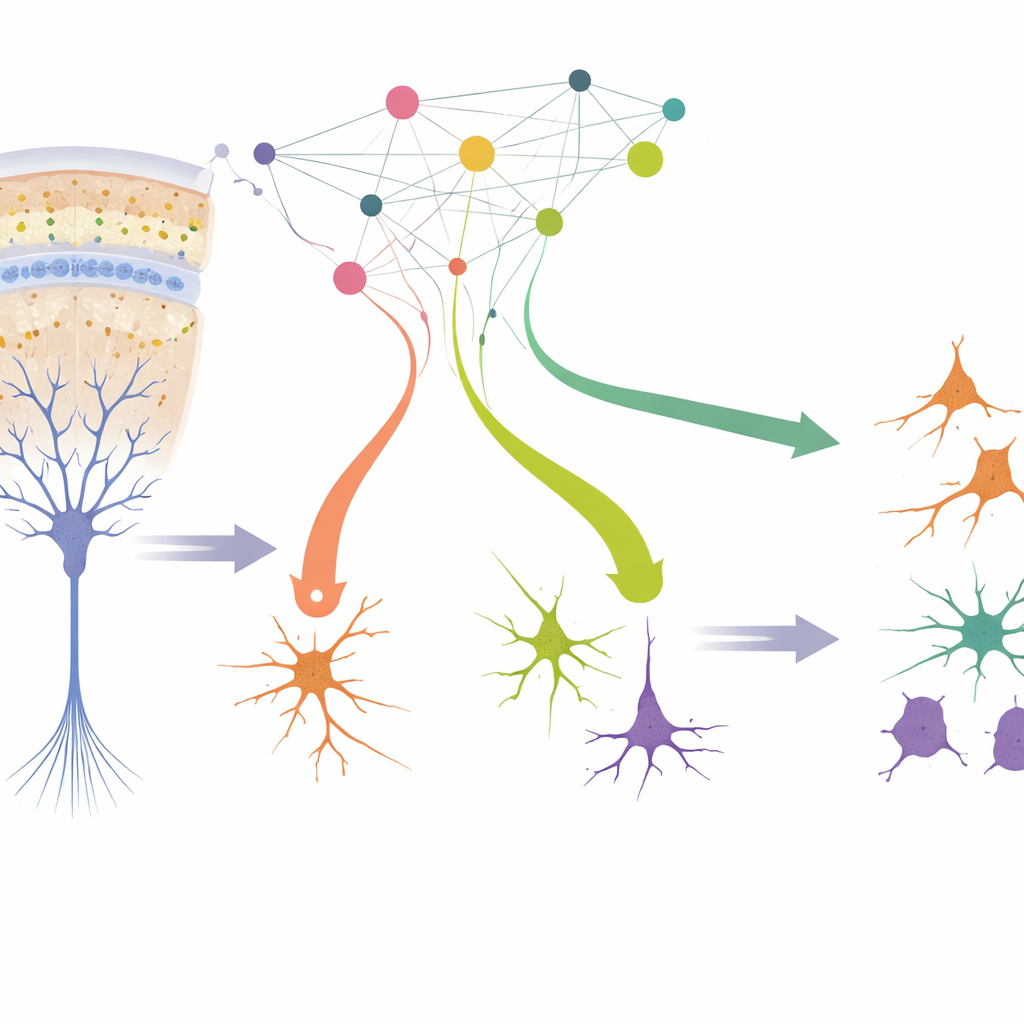
نافذة مخبرية على القشرة البشرية النامية
أنشأ المؤلفون نظامًا مخبريًا يحاكي عن كثب كيفية تطور القشرة البشرية في الرحم. بدأوا بالخلايا النجمية الشعاعية، الخلايا السلفية الرئيسية التي تبطن السطح الداخلي للدماغ أثناء منتصف الحمل وتنتج معظم الخلايا القشرية الأخرى. من خلال تعريض أنسجة جنينية بشرية لعوامل نمو لفترة وجيزة، ركّزوا هذه الخلايا السلفية ثم أزالوا العوامل لتبدأ الخلايا بطبيعتها في التخصص. في غضون أسبوع، أنتجت المستزرعات اللاعبين الرئيسيين الموجودين في القشرة قبل الولادة: الخلايا العصبية المثبطة التي تنقل الإشارات، والخلية العصبية المثبطة (interneurons) التي تضبط النشاط بدقة، وخلايا الدبق التي تدعم وتعزل الخلايا العصبية. أظهرت مقارنات مفصلة مع أطالس الدماغ القائمة أن الخلايا المزروعة مخبريًا تشبه نظيراتها في الجسم الحي بدرجة كبيرة وتُظهر ضغوطًا أقل من الخلايا في العديد من نماذج العضيات الدماغية.
إيقاف تشغيل الجينات واحدًا تلو الآخر، خلية تلو الأخرى
لمعرفة كيف تتحكم جينات محددة في هذا العرض التطوري، لجأ الفريق إلى طريقة فحص قوية تُدعى Perturb‑seq. استخدموا نظام تثبيط CRISPR الذي يمكنه تقليل نشاط الجينات المختارة بثبات بدلاً من قطعها، متجنبين بذلك تلف الحمض النووي السام. في أكثر من مئة ألف خلية مفردة، كبحوا بشكل انتقائي 44 عامل نسخيًا—جينات تعمل كمفاتيح رئيسية على جينات عديدة—ثم قاسوا مجموعة الجينات النشطة بالكامل في كل خلية. أتاح لهم ذلك ربط فقدان كل مفتاح بالتغييرات في نشاط الجينات والتحولات في أنواع الخلايا التي ظهرت في المستزرعات.
موازنة أنواع الخلايا والتوقيت في القشرة النامية
أحدثت عدة مفاتيح مستهدفة تأثيرات ملفتة. خفض نشاط NR2E1 دفع الخلايا النجمية الشعاعية للتوقف عن الانقسام في وقت أبكر وإنتاج المزيد من الخلايا العصبية المثبطة ومن ثم المزيد من الخلايا قليلة التغصن (oligodendrocytes)، مما يشير إلى أن هذا العامل يبطئ الساعة التطورية عادةً. بالمقابل، أدى تقليل ARX إلى التأثير المعاكس: فضّل الخلايا العصبية المثيرة على المثبطة وحافظ على الخطوط النسبية في حالة أكثر عدم نضج. عامل آخر، ZNF219—الذي لم يُعرف سابقًا بعمله في القشرة—وُجد أنه يمنع التمايز العصبي؛ فعند قمعه زاد إنتاج كل من الخلايا العصبية المثيرة والمثبطة مع ميل نحو الخلايا المثيرة. من خلال دمج اضطرابات الجينات مع شفرات شريطية للحمض النووي تُعلم سلالة جميع أحفاد كل خلية سلفية بشكل دائم، أظهر الباحثون أن هذه المفاتيح تغير "انحياز المصير" لنسائل مفردة من الخلايا النجمية الشعاعية، موّجهة مقدار مساهمة كل نَسْل لخطوط نسبية مختلفة وفي أي مرحلة تطورية.
جينات ناتجة مشتركة مرتبطة باضطرابات الدماغ
عندما قارن الفريق تغييرات التعبير الجيني الناجمة عن الاضطرابات المختلفة، لاحظوا أن نحو ربع كل الجينات المتأثرة كانت مستهدفة من أكثر من عامل نسخي واحد. كثير من هذه الأهداف المشتركة تشارك في كيفية تواصل الخلايا العصبية الشابة، هجرتها ونضجها. والأهم من ذلك، تداخلت هذه الجينات المتقاربة بقوة مع مجموعات جينية رُبطت سابقًا بحالات مثل الفصام والاكتئاب الشديد. على سبيل المثال، جينات مثل PTPRD وIL1RAPL1، المعروفة من دراسات بشرية وفئران بتأثيرها على تكوين الخلايا العصبية والسلوك، تقاطعت في مفترقات عدة دوائر تنظيمية. وهذا يقترح أن ضربات جينية مختلفة في التطور المبكر يمكن أن تتجمع إلى مسارات نزولية مشتركة تشكل توصيلات الدماغ وخطر المرض.
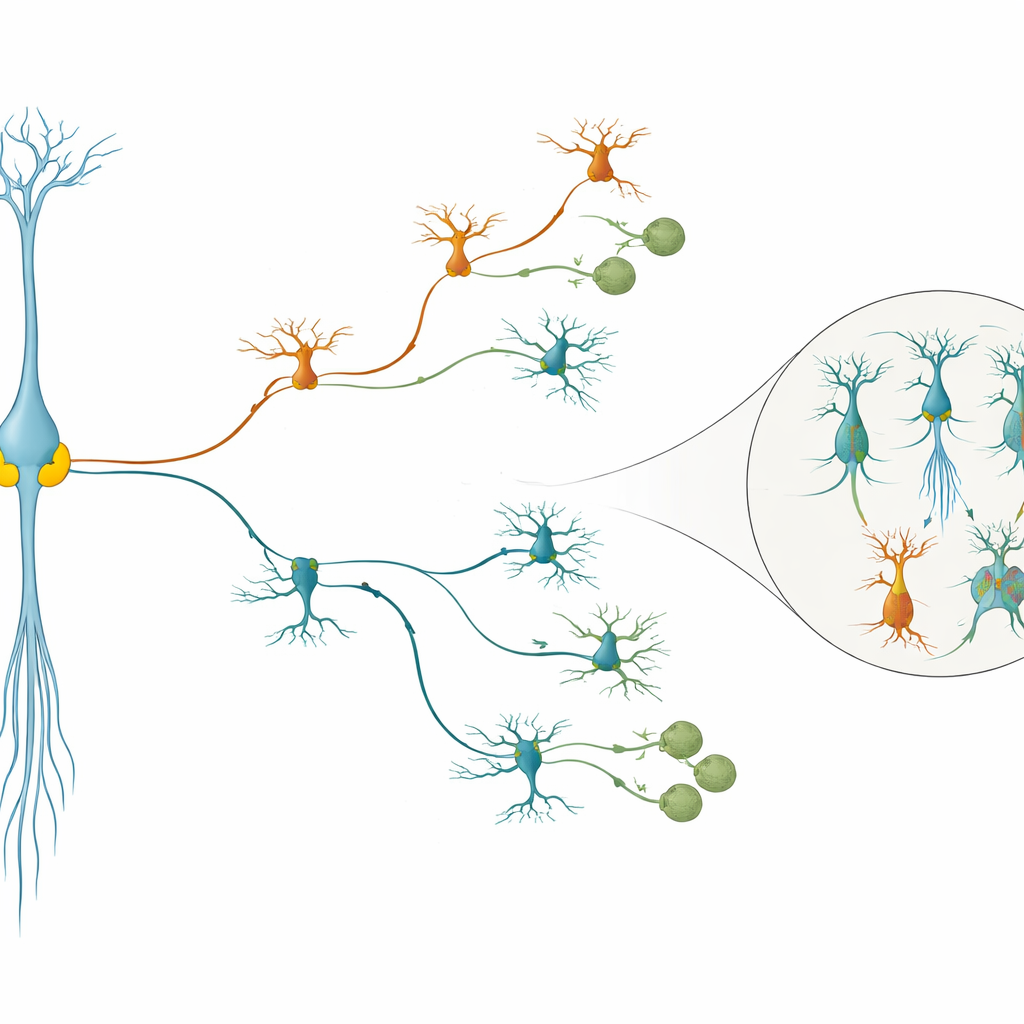
حماية هوية الخلايا العصبية بعد ولادة الخلية
بعيدًا عن تحديد "ماذا" ستصنع الخلية السلفية، حمى بعض المفاتيح أيضًا "أي نوع فرعي" ستصبح تلك الخلية. ضمن الخلايا العصبية المثبطة، أدى فقدان ARX إلى ظهور مجموعة فرعية غير عادية مميزة بجين LMO1 وتغيرات في مسارات الإشارة التي توجه عادة حركة الخلايا وتكوين المشابك؛ وظهرت خلايا غريبة مماثلة في كل من شرائح الأنسجة البشرية وخلايا قرد المكاك. باستخدام استراتيجية الاضطراب المزدوج، أظهر المؤلفون أن قمع ARX وLMO1 معًا محى جزئيًا هذه الحالة الشاذة، مما يشير إلى أن ARX يحافظ عادةً على هوية الخلايا البينية السليمة جزئيًا عن طريق كبح LMO1. ومن الجدير بالذكر أن العديد من عوامل النسخ ذات التأثيرات الأقوى—بما في ذلك ARX وNR2E1 وSOX2 وCTCF وNEUROD2 وPHF21A وZNF219—ارتبطت باضطرابات النمو العصبي والاضطرابات النفسية، ربطًا بين نتائجهم أحادية الخلية والوراثة السريرية.
لماذا تهم هذه النتائج لفهم الدماغ البشري
معًا، تقدم هذه العمل خطة عمل توضح كيف تقوم شبكة من مفاتيح الجينات في الخلايا النجمية الشعاعية البشرية بتنظيم كل من مزيج أنواع الخلايا وتوقيت تطور القشرة، وكيف يمكن لأخطاء في تلك الشبكة أن تحرف هوية الخلايا العصبية. من خلال استخدام نظام خلايا أولي موثوق، وقراءات أحادية الخلية وتتبع السلالة، يوفر المؤلفون إطارًا مرنًا لاستكشاف جينات ومسارات إضافية في تطور دماغ الإنسان والرئيسيات. للمطلعين غير المتخصصين، الخلاصة الأساسية هي أن تغييرات جينية مختلفة كثيرة يمكن أن تتلاقى على برامج تطورية مشتركة تشكل كيفية بناء أدمغتنا—وعندما تتعطل هذه البرامج، يمكن أن تتجلى العواقب لاحقًا كاضطرابات معرفية ونفسية.
الاستشهاد: Ding, J.W., Kim, C.N., Ostrowski, M.S. et al. Dissecting gene regulatory networks governing human cortical cell fate. Nature 651, 732–742 (2026). https://doi.org/10.1038/s41586-025-09997-7
الكلمات المفتاحية: تطور القشرة الدماغية, الخلايا النجمية الشعاعية, CRISPR أحادي الخلية, تكوين الخلايا العصبية, اضطرابات نفسية عصبية