Clear Sky Science · ar
الدرع الأيضي المعتمد على البولي أمينات ينظم الازدواج الاختياري
كيف تساعد الجزيئات الصغيرة الخلايا على قراءة جيناتها
داخل كل خلية، يمكن قراءة مخطط الحمض النووي نفسه بطرق متعددة، مما يسمح لعدد محدود من الجينات بإنتاج تنوّع هائل من البروتينات. تعتمد هذه المرونة على عملية تُسمى الازدواج الاختياري، التي تُحرِّر رسائل الحمض الريبي النووي قبل تحويلها إلى بروتينات. تكشف هذه الورقة أن جزيئات صغيرة موجبة الشحنة تُسمى البولي أمينات توجه هذه خطوة التحرير بهدوء، وتعمل كنوع من الدرع الواقي الذي يساعد الخلايا على اتخاذ قرار بشأن أي نسخ من الحمض الريبي تُصنَع. وبما أن الازدواج الاختياري حاسم في السرطان، ووظائف الدماغ، والخلايا الجذعية، فإن كشف هذه الطبقة المخفية من التنظيم له آثار واسعة على الصحة والمرض.
مساعدون شحنات صغيرة في كل خلية
البولي أمينات هي جزيئات صغيرة ومرنة تحمل عدة شحنات موجبة. تصنعها الخلايا من المغذيات الأساسية، وقد عُرفت منذ زمن طويل كمساعدات للنمو والبقاء، خاصة في الخلايا سريعة الانقسام مثل الأورام. تساءل المؤلفون عما إذا كانت البولي أمينات تعمل أيضًا كأشارات، وليس فقط كوقود. من خلال حجب إنتاج البولي أمينات جزئيًا في خلايا سرطان البروستات وفي الفئران، قاسوا كيف تغيرت البروتينات والحمض الريبي مع مرور الزمن. وجدوا أنه قبل انخفاض مستويات البولي أمينات بشكل كبير بكثير، حدث موجة قوية من التغيرات في فسفرة البروتين—وهي علامات كيميائية تُشغِّل أو تُطفئ مفاتيح البروتين—وخاصة على مكونات آلية تحرير الحمض الريبي الخلوية، المجمع المسؤول عن الازدواج (spliceosome).
إعادة توصيل محرر الحمض الريبي في الخلية
بالنظر تحديدًا إلى الحمض الريبي، استخدم الفريق تسلسلًا عميقًا لتتبع الازدواج الاختياري عند تثبيط تخليق البولي أمينات. تم استبعاد أو تضمين مئات المقاطع الريبية بشكل مختلف، في خطوط خلايا سرطانية وأنواع خلايا طبيعية وأنسجة الفئران. لم تكن هذه التغيرات مجرد أثر جانبي لتباطؤ انقسام الخلايا أو لعملية أخرى معتمدة على البولي أمينات تُدعى الهيبوسينيشن (hypusination). بل عندما أعاد الباحثون تزويد الخلايا ببولي أمينات خارجية، عادت العديد من تحولات الازدواج إلى طبيعتها بسرعة. أنتجت الأدوية والأدوات الجينية التي خفضت البولي أمينات أنماط ازدواج مماثلة، وخفض مزيد من البولي أمينات باستخدام مزيج دوائي قوّى التغيرات أكثر، ما أكد أن التأثير مرتبط ارتباطًا وثيقًا بتوفر البولي أمينات.
هدف مخفي: وحدة SF3 في آلية الازدواج
لتحديد مكان عمل البولي أمينات داخل آلية الازدواج، قارن المؤلفون البصمة الازدواجية الناتجة عن خفض البولي أمينات مع خريطة مرجعية كبيرة نُشِئت عن طريق إسكات أكثر من 300 عامل ازدواج معروف بشكل فردي. أشار أقرب تطابق إلى جزء محدد من المجمع المسبب للانقسام يُسمى تحتالمجموعة SF3، التي تساعد على التعرف على إشارات رئيسية في الحمض الريبي. دعمت التحليلات الحاسوبية لبيانات ربط البروتين–الحمض الريبي العامة هذه الصلة: كانت الحمضيات الريبية التي تغير ازدواجها بفقدان البولي أمينات أكثر احتمالًا أن تكون مرتبطة ببروتينات SF3. عندما تعطلت مكونات SF3 جزئيًا جينيًا أو بدواء، تم طمس تأثيرات نقص البولي أمينات على الازدواج إلى حد كبير، مما يبين أن نشاط SF3 السليم مطلوب لهذا المسار التنظيمي الجديد. 
الدرع الأيضي: كيف تمنع البولي أمينات وسم البروتينات
بالغوص أعمق، لاحظ الباحثون أن مواقع الفسفرة الأكثر تضررًا على بروتينات SF3 تتجمع داخل مقاطع قصيرة غنية بالأحماض الأمينية السالبة الشحنة. أوضحت النمذجة الجزيئية وتجارب الرنين المغناطيسي النووي أن البولي أمينات تستقر في هذه البقع الحمضية، مكوِّنة اتصالات كهروستاتيكية متعددة وتغطي جزئيًا بقايا السيرين القريبة التي عادةً ما تُضاف إليها مجموعات الفوسفات. هذا "العناق" الفيزيائي يقلل من مدى إمكانية وصول الكينازات—الإنزيمات التي تُلصق الفوسفات—إلى هذه المواقع. في تجارب أنبوب الاختبار، منعت إضافة البولي أمينات مباشرةً كينازًا يدعى CK1 من فسفرة بروتينات SF3. وفي الخلايا، قلّص تثبيط CK1 ونظيره القريب CK2 التغيرات في الازدواج الناجمة عن نقص البولي أمينات، وأظهرت فئران معدّلة هندسيًا فقدت في بروتين SF3A3 ثلاث مواقع فسفرة أساسية أنها أصبحت غير حساسة إلى حد كبير لتحولات الازدواج المعتمدة على البولي أمينات. 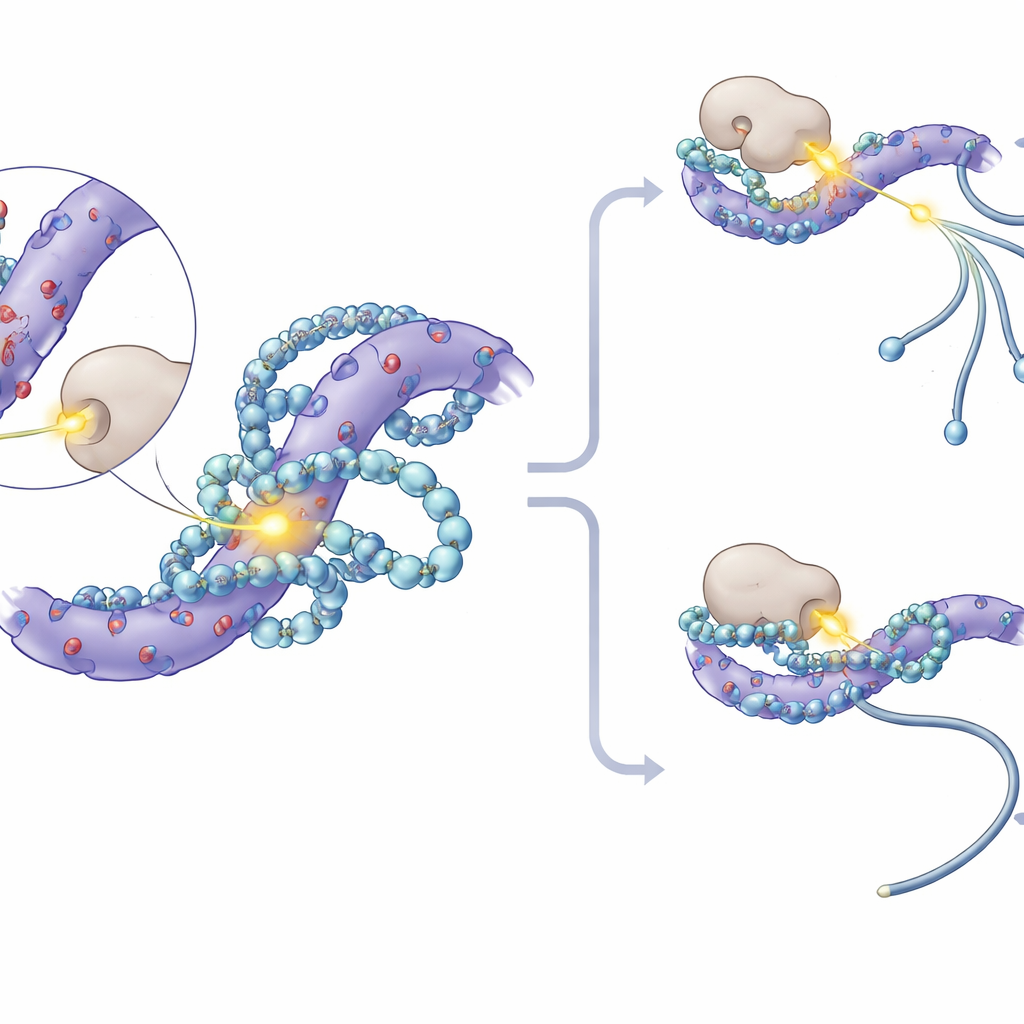
جزيء مُصمَّم يفصل الأدوار
تقدّم الدراسة أيضًا دواءً شبيهًا بالبولي أمينات يُدعى BENSpm، يحمل شحنة موجبة أقوى ولكنه في الوقت نفسه يوقف إنتاج البولي أمينات داخل الخلية. ربط BENSpm بإحكام ببقع SF3 الحمضية ومنع عمل الكينازات، تمامًا مثل البولي أمينات الطبيعية، ومع ذلك لم يعِد نمو الخلايا عندما كانت البولي أمينات الحقيقية نادرة. أتاح ذلك للمؤلفين فصل وظائف البولي أمينات الكلاسيكية (دعم النمو والأيض) عن دور الدرع الجديد. في خلايا جذعية جنينية للفأر، دفع استنفاد البولي أمينات الخلايا نحو فقدان علامة "الذات الجذعية" Nanog وغير مشهد الازدواج لديها. استعاد BENSpm كلاً من بصمة الازدواج وتعبير Nanog رغم استمرار كبح تخليق البولي أمينات الطبيعي، مما يشير إلى أن الدرع الأيضي مطلب أساسي للحفاظ على هوية الخلايا الجذعية.
لماذا تهم هذه الاكتشافات
بعبارات بسيطة، توضح هذه الدراسة أن البولي أمينات تعمل كقفازات واقية صغيرة حول أجزاء حساسة من بروتينات الازدواج الرئيسية. عندما تكون القفازات مرتدية، لا تستطيع الكينازات الإمساك بتلك المواقع بسهولة ووسمها، ويستمر تحرير الحمض الريبي في مساره الطبيعي. عندما تنخفض البولي أمينات، تُخلَع القفازات، يرتفع مستوى الفسفرة، وتتغير أنماط الازدواج، مما يترتب عليه نتائج مهمة للخلايا السرطانية والخلايا الجذعية على حد سواء. من خلال تعريف آلية "الدرع الأيضي" وتقديم جزيء أداتي يحاكيها انتقائيًا، تفتح الدراسة الباب أمام طرق جديدة لضبط قراءة الجينات دون تغيير الحمض النووي ذاته، وقد تُلهم مستقبلاً علاجات تستهدف الازدواج في السرطان والطب التجديدي.
الاستشهاد: Zabala-Letona, A., Pujana-Vaquerizo, M., Martinez-Laosa, B. et al. Polyamine-dependent metabolic shielding regulates alternative splicing. Nature 651, 819–828 (2026). https://doi.org/10.1038/s41586-025-09965-1
الكلمات المفتاحية: البولي أمينات, الازدواج الاختياري, معالجة الحمض الريبي النووي, الإشارات الأيضية, تنظيم الخلايا الجذعية