Clear Sky Science · ar
مسارات التفعيل الخاصة بالليغان تحدد إشارات GPCR في الخلايا
كيف يمكن لمستقبل واحد أن يتصرف كأنّه عدة مفاتيح
تؤثر العديد من الأدوية الحالية على عائلة كبيرة من بروتينات سطح الخلية تُسمى مستقبلات المرتبطة ببروتين G، أو GPCRs. تساهم هذه المستقبلات في تنظيم معدل ضربات القلب والمزاج والتنفس والعديد من وظائف الجسم الأخرى. لعقود كانت تُعامل كمفاتيح بسيطة تشغيل/إيقاف: يرتبط الدواء، تُقلب الحالة، ويتدفق الإشارة داخل الخلية. يُظهر هذا المقال أن الواقع أكثر ثراءً من ذلك. باستخدام نوع جديد من "الجاسوس" الفلوري المدمج مباشرة في المستقبل، يراقب المؤلفون، في خلايا حية، كيف ترسل أدوية مختلفة نفس المستقبل على مسارات تفعيل مميزة—كأنها اختيار طرق مختلفة عبر مدينة—لإنتاج أنماط إشارات مختلفة. فهم هذه الطرق المخفية يمكن أن يساعد في تصميم أدوية تعطي الفائدة المرغوبة مع تجنّب الآثار الجانبية.
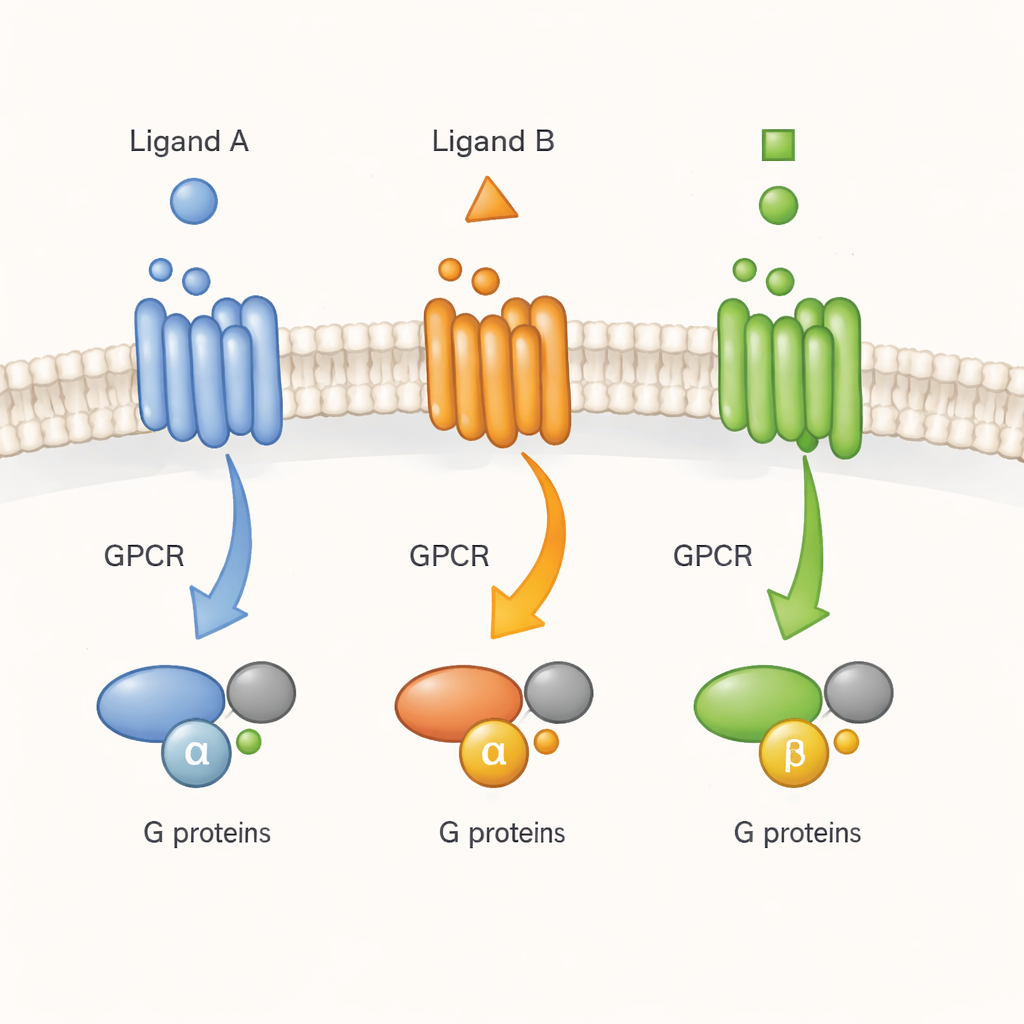
مراقبة جرس باب الخلية في الوقت الحقيقي
غالبًا ما تُوصف مستقبلات GPCR كأجراس باب جزيئية: جزيء الإشارة (الليغان) يقرع من الخارج، والمستقبل ينقل الرسالة إلى بروتينات G من الداخل. أشارت أعمال سابقة على مستقبلات مُنقاة في محاليل منظفة إلى أن GPCRs لا تقتصر على شكل واحد خامد وشكل واحد نشط فقط. بل تُجرب العديد من الأشكال التي يمكن للأدوية تثبيتها بدرجات متفاوتة. لكن لم يكن واضحًا ما إذا كان نفس التعقيد موجودًا في بيئة الخلية الحية المزدحمة والديناميكية. هنا يركز المؤلفون على مستقبل نمطي واحد، مستقبل الـM2 الموسكاريني للأستيل كولين، وهو منظم مهم لنشاط القلب والأعصاب، ويسألون ما إذا كانت الليغانات المختلفة تدفعه إلى أشكال نشطة متميزة تهم للإشارات الخلوية الحقيقية.
بناء مراسلين ضوئيين صغار على سطح المستقبل
لمتابعة حركات المستقبل دون تعطيل وظيفته الطبيعية، استخدم الفريق توسيع الشيفرة الجينية، وهي تقنية تسمح بإدخال حمض أميني مصمم خاص في مواقع مختارة على السطح الخارجي للمستقبل. يمكن ربط هذه "المرساة" الكيميائية بصبغة فلورية صغيرة داخل الخلايا الحية. من خلال فحص 72 موضعًا والاحتفاظ فقط بتلك التي لا تزال تتصرف كمستقبلات طبيعية، بنوا مجموعة مكونة من سبعة متغيرات لمستقبل M2، كل واحد يحمل صبغة مفردة في موقع حلقي خارجي مختلف. عند تطبيق الرسول الطبيعي الأستيل كولين، ارتفعت أو انخفضت سطوعات الصبغة في هذه المواقع بطرق مميزة، كاشفة كيف تحرك كل جزء من السطح الخارجي للمستقبل مع بدء الإشارة. والأهم أن هذه المستقبلات الموسومة ظلّت قادرة على تنشيط بروتينات G والخضوع للاستهلاك الطبيعي داخل الخلية، ما يدل على أن أجهزة الاستشعار كانت مخلصة وليست مُعطِّلة.
الأدوية تترك "بصمات شكلية" مميزة
قارن الباحثون بعد ذلك عدة أدوية كلها تُشغّل مستقبل M2 لكن بقوى مختلفة: الأستيل كولين الطبيعي في الجسم، ناهض اصطناعي فائق القوة يُدعى إبيروكسو، واثنان من النواهد الجزئية الأضعف، الأريكولين والبيلوكاربين. أنتج كل دواء نمطًا فريدًا من تغيّرات التألق عبر مواقع المراسل السبعة—بصمة شكلية. في معظم المواضع، تتبعت درجة الحركة مدى قوة تنشيط الدواء للمستقبل. ومع ذلك، في موضعين كان العلاقة معكوسة: الأدْوية الأضعف أحدثت أكبر التغيّرات، بينما أقوى دواء أنتج تغيّرات تكاد تكون معدومة. لا يمكن تفسير مثل هذا السلوك بوجود حالة نشطة واحدة فقط. بل يدل على أن نفس المستقبل، في خلايا حية، يمكن أن يتخذ عدة أشكال نشطة مميزة، بعضها مفضّل بواسطة أدوية قوية، وأخرى بواسطة أدوية ضعيفة.
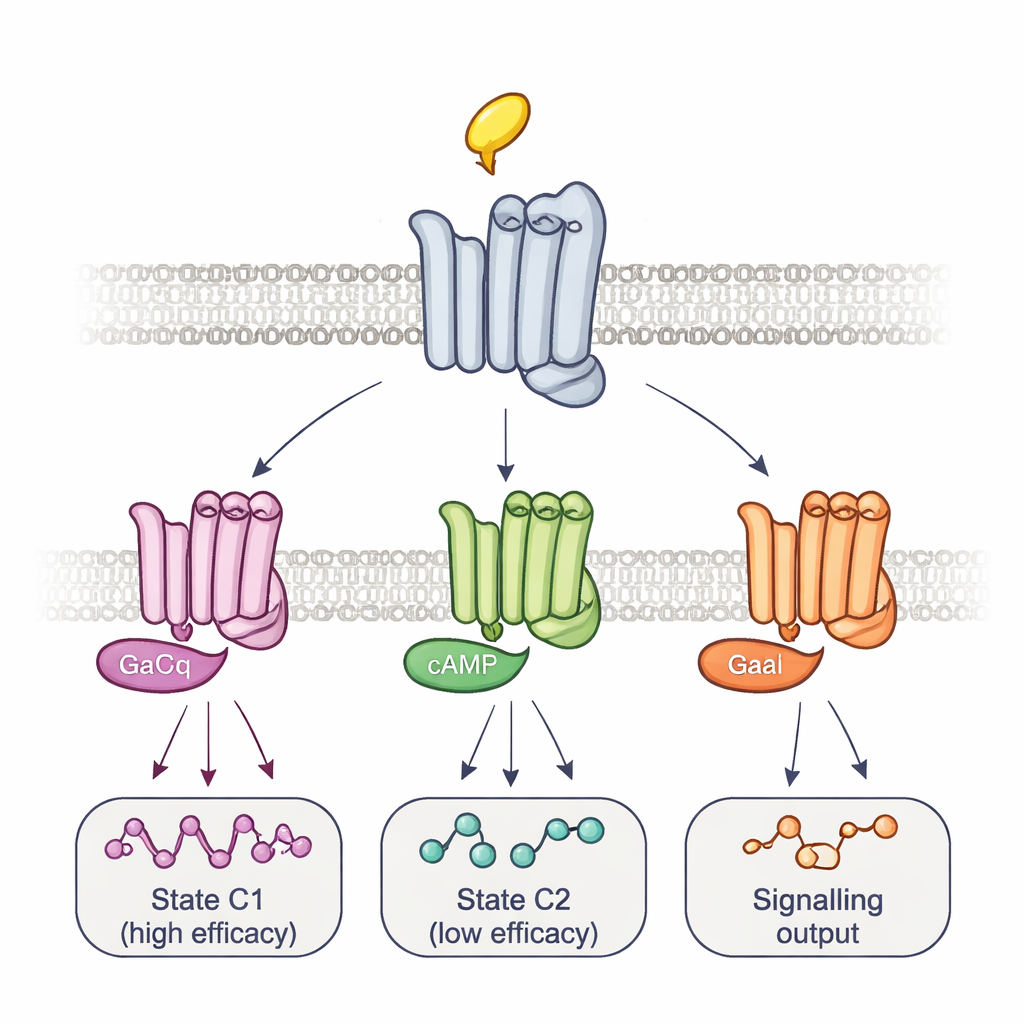
مجاميع متعددة ومسارات زمنية للإشارة
لربط هذه الأشكال بالإشارات الفعلية، عدّل الفريق بروتينات G نفسها. أدى الإفراط في التعبير عن بروتين G مُطوَّر يشكل مجاميع قوية وطويلة العمر مع المستقبلات إلى محو الإشارة من بعض مواقع المراسل بينما عزّز أخرى بشكل انتقائي. يكشف هذا النمط، مع توقيت تغيّرات التألق، عن وجود ما لا يقل عن مجمعين رئيسيين للمستقبل–بروتين G: مجمع يتشكل سريعًا وعالي الفعالية وآخر أبطأ ومنخفض الفعالية. حوّلت الأدوية المختلفة التوازن بين هذه المجاميع وحتى استخدمت خطوات وسيطة مختلفة للوصول إليها، متبعة مسارات تفعيل خاصة بكل دواء. باستخدام فحص ضوئي منفصل يقيس 14 نوعًا فرعيًا من بروتينات G، أظهر المؤلفون أن هذه التوازنات تساعد في تحديد ليس فقط مدى شدة تنشيط الدواء للإشارة ككل، بل أي بروتينات G بالذات تُشغّل. على سبيل المثال، نشّط الأريكولين تفضيليًا بعض بروتينات Go، بينما فضّل البيلوكاربين بشدّة المجمع منخفض الفعالية.
لماذا يهم هذا لصناعة أدوية أفضل
لغير المتخصصين، الرسالة الأساسية هي أن المستقبل الواحد ليس مجرد مفتاح واحد بل مجموعة من المفاتيح المرتبطة، كل واحدة يمكن الوصول إليها عبر مسارات مختلفة وكل منها موصولة بتأثيرات لاحقة مختلفة قليلاً. يقدم هذا البحث رؤية مباشرة لتلك المسارات والحالات في خلايا سليمة، بدلًا من أنظمة مبسطة لأنابيب الاختبار. من خلال رسم خريطة لكيفية تحيز أدوية بعينها للمستقبل نحو مجمعات وشركاء بروتين G محددين، يحصل الباحثون على مخطط لتصميم أدوية "أذكى"—مركبات تدفع المستقبل إلى حالات تولّد إشارات مفيدة مع تجنّب تلك المرتبطة بالآثار الجانبية. يجب أن تكون استراتيجية جهاز الاستشعار الفلوري المطوّرة هنا قابلة للتطبيق على مستقبلات عديدة أخرى، فاتحة نافذة على رقصة حركة الدواء في الوقت الحقيقي داخل الخلايا الحية.
الاستشهاد: Thomas, R., Jacoby, P.S., De Faveri, C. et al. Ligand-specific activation trajectories dictate GPCR signalling in cells. Nature 650, 1053–1062 (2026). https://doi.org/10.1038/s41586-025-09963-3
الكلمات المفتاحية: إشارات GPCR, فعالية الليغان, بروتينات G, أجهزة استشعار شكلية, اكتشاف الأدوية