Clear Sky Science · ar
اللدونة الخلوية للخلايا التائية المحفَّزة بواسطة الميكروبيوتا تسمح بالسيطرة المناعية على الأورام
كيف قد تساعد الجراثيم المعوية الصديقة في مكافحة السرطان
لقد غيّر العلاج المناعي للسرطان ملامح العلاج للعديد من المرضى، ومع ذلك لا يرى سوى جزء منهم تقلص أورامهم وبقاءها بعيدًا. تطرح هذه الدراسة سؤالاً بسيطًا ظاهريًا لكنه ذا تبعات كبيرة: هل يمكن لبعض بكتيريا الأمعاء أن "تدرّب" خلايا المناعة بطريقة تجعل أدوية حجب نقاط التفتيش، مثل علاج مضاد PD‑1، تعمل بشكل أفضل؟ من خلال تتبع مسار خلايا المناعة من الأمعاء الدقيقة إلى الأورام في الفئران، يكشف المؤلفون عن رابط مباشر وقابل للاختبار بين ميكروب معوي واحد والسيطرة الناجحة على الورم.
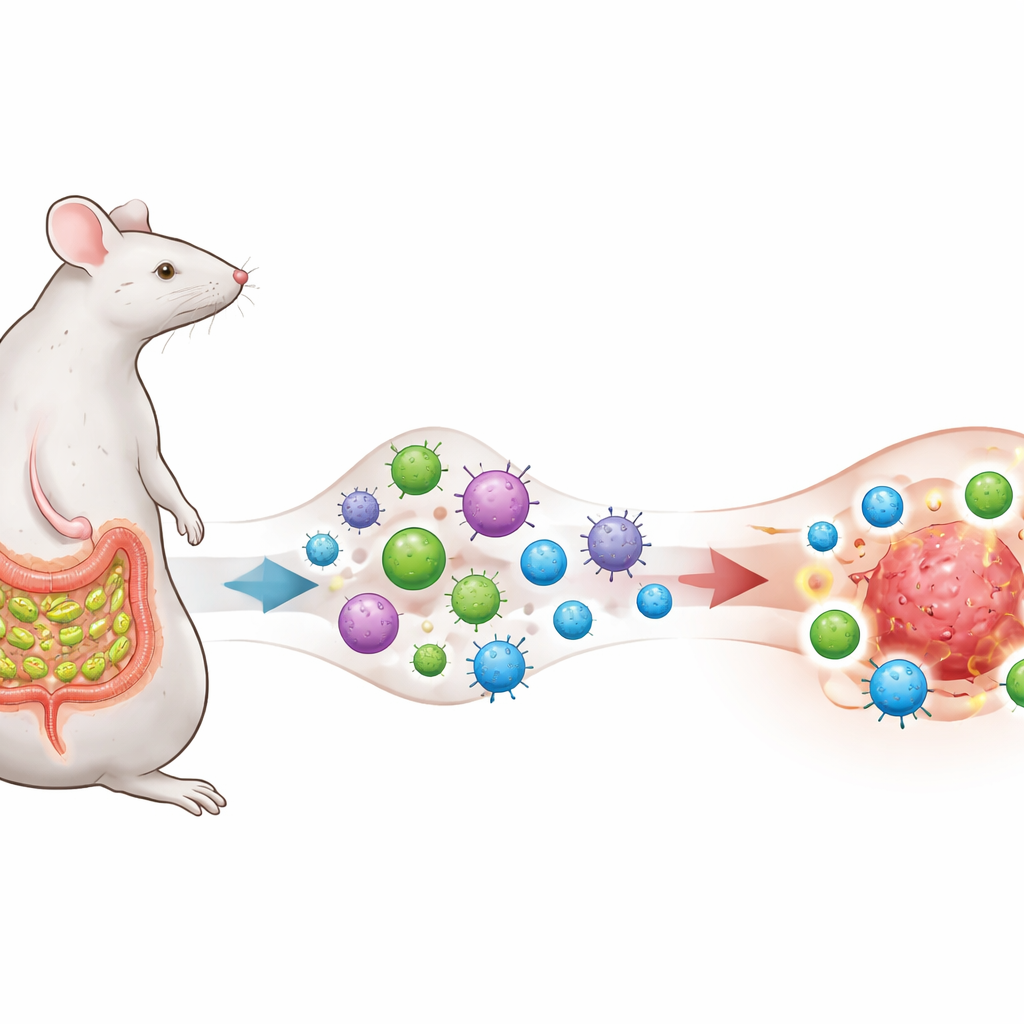
ميكروب يدرب جهاز المناعة
ركز الباحثون على بكتيريا معوية تُسمى البكتيريا الحلقية المقسمة (segmented filamentous bacteria - SFB)، المعروفة بأنها تعيش قريبًا من بطانة الأمعاء الدقيقة في الفئران وتثير استجابة قوية للخلايا المساعدة من نوع TH17 التي تبني عادةً التوازن النسيجي. قاموا بتعديل خلايا الميلانوما والرئة والقولون بحيث تعرض جزءًا من بروتين يوجد أيضًا في SFB، محدثين "تداخل مستضدات" متعمدًا بين الميكروب والأورام. أما الفئران فإما ظلت خالية من SFB أو استوطنها هذا الميكروب، وتلقت جميعها علاجًا بمضاد PD‑1، وهو جسم مضاد شائع لحجب نقاط التفتيش يهدف إلى رفع كبح الخلايا التائية.
الخلايا المدربة في الأمعاء تحول الأورام من باردة إلى ساخنة
يُظهر علاج مضاد PD‑1 بمفرده، أو وجود SFB بمفرده، تأثيرًا ضئيلًا على إبطاء نمو الورم. لكن عندما تحمل الأورام مستضدًا مشتقًا من SFB وتستوطن الفئران بـSFB، يصبح مضاد PD‑1 فعّالًا للغاية: تتقلص الأورام، تتحسن البقيا، وترفض الحيوانات الناجية إعادة التحدي الورمي لاحقًا دون علاج إضافي، ما يشير إلى ذاكرة مناعية دائمة. في هذه الفئران الناجحة، تمتلئ الأورام بخلايا CD8 القاتلة العدوانية التي تنتج الإنترفيرون‑γ وجزيئات سامة أخرى، بينما تشكل الخلايا التائية التنظيمية المثبطة حصة أصغر من المجمع المناعي. باختصار، يُعاد تشكيل البيئة المحلية حول السرطان من "باردة" وقليلة الاستجابة إلى "ساخنة" وملتهبة.
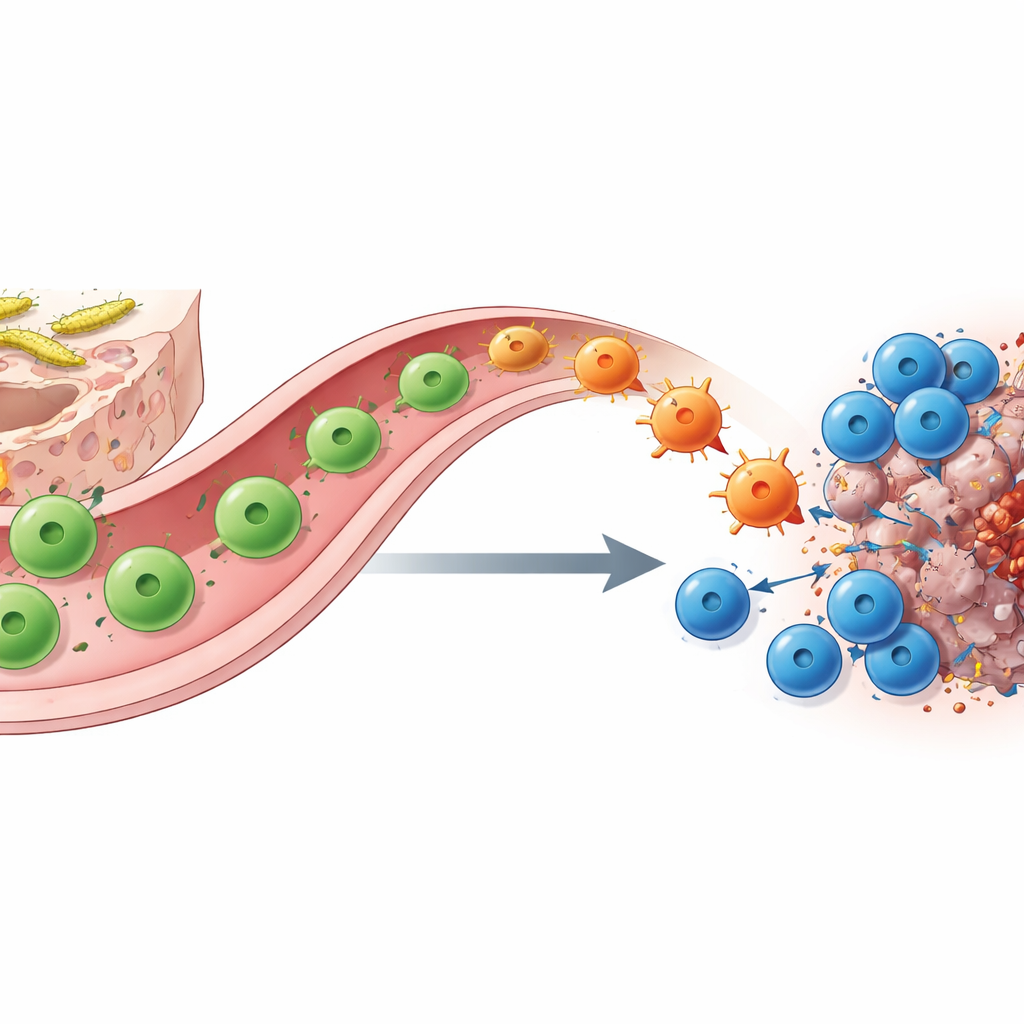
الخلايا المساعدة المتحولة تجسر بين الأمعاء والورم
كيف يسبب استيطان SFB هذا التحول؟ باستخدام الترميز الجزيئي، وتسلسل الخلية الواحدة وتتبعًا وراثيًا ذكيًا، يبين المؤلفون أن اللاعبين الأساسيين هم خلايا CD4 المساعدة الخاصة بـSFB. في الأمعاء الدقيقة تبدأ هذه الخلايا كخلايا TH17 التي تدعم وظيفة الحاجز وتنتج عادةً الجزيء IL‑17A. عندما تواجه مستضدًا مطابقًا في ورم تحت تأثير حجب نقاط التفتيش، تهاجر من الأمعاء إلى موقع السرطان وتتحوّل "متخصصة من جديد" إلى خلايا شبيهة بـTH1 تفرز بدلاً من ذلك كميات كبيرة من الإنترفيرون‑γ وTNF. تعزز هذه الخلايا المحوّلة "سابقًا‑TH17" عرض المستضد وتفرز جاذبات كيميائية، ما يجذب خلايا CD8 القاتلة ويقوّيها. إزالة إما الخلايا المساعدة أو القاتلة، أو الحذف الجيني للخلايا المنحدرة من سلالة IL‑17A التي تعمل كمقدّمات، يُلغي إلى حد كبير فائدة مضاد PD‑1، مما يؤكد شراكتهما.
ليست كل الميكروبات تعطِي تعليمات مفيدة
لاختبار ما إذا كان أي بكتير معوي يحمل مستضدًا متطابقًا يكفي، كررت الفريق التجربة مع ميكروب آخر مرافق، Helicobacter hepaticus. هذا الكائن يحفز أيضًا استجابات تائية قوية لكنه يوسّع في المقام الأول خلايا ذات طابع تنظيمي تخفف الالتهاب. عندما تُهندس الأورام لعرض مستضد من H. hepaticus وتستوطن الفئران بهذا البكتير، لا يتحسن علاج مضاد PD‑1. فعلى الرغم من أن العديد من خلايا المساعدة الخاصة بـH. hepaticus تسافر إلى الورم، فإنها تحتفظ بطابع تنظيمي وتنتج قليلًا من الإنترفيرون‑γ، فتفشل في تنشيط الخلايا القاتلة. يُظهر هذا التباين أن جودة وَلَدونة برامج الخلايا التائية المحفَّزة بالميكروبات—وليس مجرد تطابق المستضد—تحددان ما إذا كانت الميكروبيوتا ستساعد أم تعيق العلاج المناعي للسرطان.
ما الذي قد يعنيه هذا لرعاية السرطان مستقبلاً
إجمالًا، يقدم العمل دليلًا مباشرًا في الحيوانات على أن بكتيريا معوية محددة يمكن أن تُدرّب مسبقًا الخلايا المساعدة في الأمعاء، ترسلها إلى أورام تشارك المستضد وتدفعها، تحت تأثير حجب نقاط التفتيش، لتغيير دورها إلى خلايا قوية قاتلة للأورام. من خلال توضيح هذا الدائرة من الأمعاء إلى الورم، توحي الدراسة بأن ميكروبات مُنتقاة بعناية أو مُهندَسة قد تُستخدم يومًا ما إلى جانب العلاج المناعي لتحويل أورام مزيد من المرضى إلى أهداف قابلة للعلاج وملتهبة—بشرط أن تحفّز تلك الميكروبات نوعًا مناسبًا من الاستجابة التائية المرنة الموالية للالتهاب بدلاً من استجابة مهدئة وتنظيمية.
الاستشهاد: Najar, T.A., Hao, Y., Hao, Y. et al. Microbiota-induced T cell plasticity enables immune-mediated tumour control. Nature 651, 201–210 (2026). https://doi.org/10.1038/s41586-025-09913-z
الكلمات المفتاحية: ميكروبيوتا الأمعاء, العلاج المناعي للسرطان, لدونة الخلايا التائية, حجب نقاط التفتيش المناعية, البيئة الميكروية للورم