Clear Sky Science · ar
شاشات CRISPR ثنائية الاتجاه تفك شفرة دائرة خلوية لفيبروز تعتمد على GLIS3
عندما يتحول الشفاء إلى ندب ضار
من المفترض أن أمعائنا تصلح نفسها بعد كل خدش أو تهيّج. لكن في الأمراض المزمنة مثل داء كرون والتهاب القولون التقرحي، قد ينحرف هذا المسار التصالحي، مما يؤدي إلى نسيج ندبي سميك وصلب يضيّق القناة الهضمية وقد يتطلب إجراء جراحة. تكشف هذه الدراسة عن حوار خفي بين الخلايا المناعية والخلايا التركيبية في الأمعاء يدفع هذا التندب، وتحدد مفتاح تشغيل رئيسياً، وهو جين يُدعى GLIS3، قد يوفر وسيلة جديدة لكسر هذه الحلقة.
شبكة خفية داخل أمعاء ملتهبة
لفهم سبب إصابة بعض المرضى بالالتهاب والليف المقاومين للعلاج، أنشأ الباحثون «خريطة خلوية» للأمعاء البشرية. جمعوا تتابع الحمض النووي الريبوزي أحادي الخلية، الذي يقرأ الجينات النشطة في كل خلية على حدة، مع تحديد مكاني يضع تلك الخلايا في شرائح النسيج الحقيقية. باستخدام عينات من أشخاص مصابين بداء كرون والتهاب القولون التقرحي وأشخاص ضوابط، رسموا أكثر من أربعة ملايين خلية عبر جدار الأمعاء. ضمن هذا التجمع، برزت مجموعة فرعية من الخلايا الليفية: الخلايا الليفية المرتبطة بالالتهاب أو IAFs. كانت هذه الخلايا تتجمع في مناطق من القولون الملتهب النشط والمزمن وحملت توقيعاً جينياً مرتبطاً بالمقاومة للعلاجات المضادة لعامل النخر الورمي (anti–TNF)، ما يوحي بأنها تلعب دوراً مركزياً في المرض الذي يصعب علاجه. 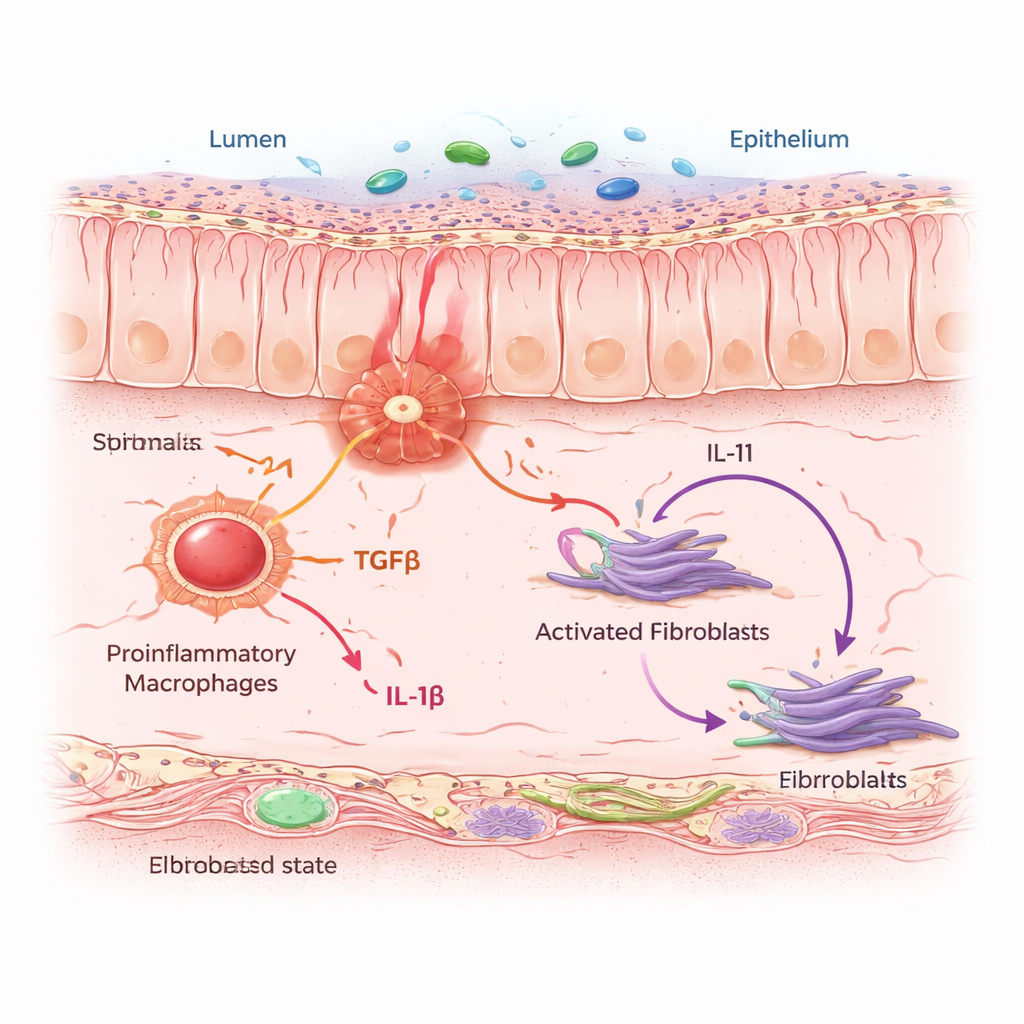
البلعمات تهمس، والخلايا الليفية تُكوّن ندباً
لم تعمل IAFs بمفردها. كانت تتجمع في «أحياء» مكتظة بالبلعمات المُلَهِبة — خلايا مناعية تستشعر الخطر وتطلق إشارات إنذار. باستخدام نماذج حاسوبية وتجارب تعايش الخلايا، أظهر الفريق أنه عندما تُدفع البلعمات إلى حالة التهابية، تفرز بروتينين رسولين رئيسيين: TGFβ وIL-1β. تستمع الخلايا الليفية المجاورة لهذه الإشارات عبر مستقبلات محددة. عندما تصل الإشارتان معاً، تتحول الخلايا الليفية إلى حالة IAF وتبدأ بإنتاج IL-11، وهو سايتوكين يشتبه بالفعل في تعزيز التندب، إلى جانب الكولاجين وبروتينات مصفوفية أخرى تعمل على تضخيم وتصلب جدار الأمعاء. في الفئران المعرضة لنظام التهاب قولون مزمن، أدت حجب IL-11 أو حذفه انتقائياً في الخلايا الليفية إلى تقليل تراكم الكولاجين دون أن تمنع الالتهاب الأولي، مما يدل على أن IL-11 محرك حاسم لمرحلة التندب.
GLIS3: مفتاح التحكم في الخلايا الليفية المندبة
للانتقال من الارتباطات إلى الآليات، استخدم المؤلفون أدوات CRISPR واسعة النطاق. هندسوا خلايا ليفية بشرية بحيث يمكن مراقبة إنتاج IL-11 بعلامة فلورية، ثم أجروا شاشات موازية تقوم إما بإطفاء جينات أو بتفعيلها عبر الجينوم. من خلال فرز الخلايا التي أنتجت كميات غير عادية عالية أو منخفضة من IL-11 بعد تحفيزها بـTGFβ وIL-1β، حددوا الجينات التي تتحكم في هذا الاستجابة. من بين العديد من مكونات التمثيل الإشاري، برز عامل نسخي واحد — GLIS3 — كمنظم رئيسي. عندما تعطّل GLIS3، أنتجت الخلايا الليفية كمية أقل بكثير من IL-11؛ وعندما زاد نشاطه، ارتفع مستوى IL-11 بشكل كبير. أظهرت تجارب إضافية أن GLIS3 ينتقل إلى نواة الخلايا الليفية استجابة لإشارات البلعمات، ويرتبط مباشرة بالحمض النووي قرب جين IL11 وجينات أخرى، ويُفعل برنامجاً واسعاً من الجينات الالتهابية والليفية، بما في ذلك الكولاجينات والعوامل التي تجذب خلايا مناعية إضافية. 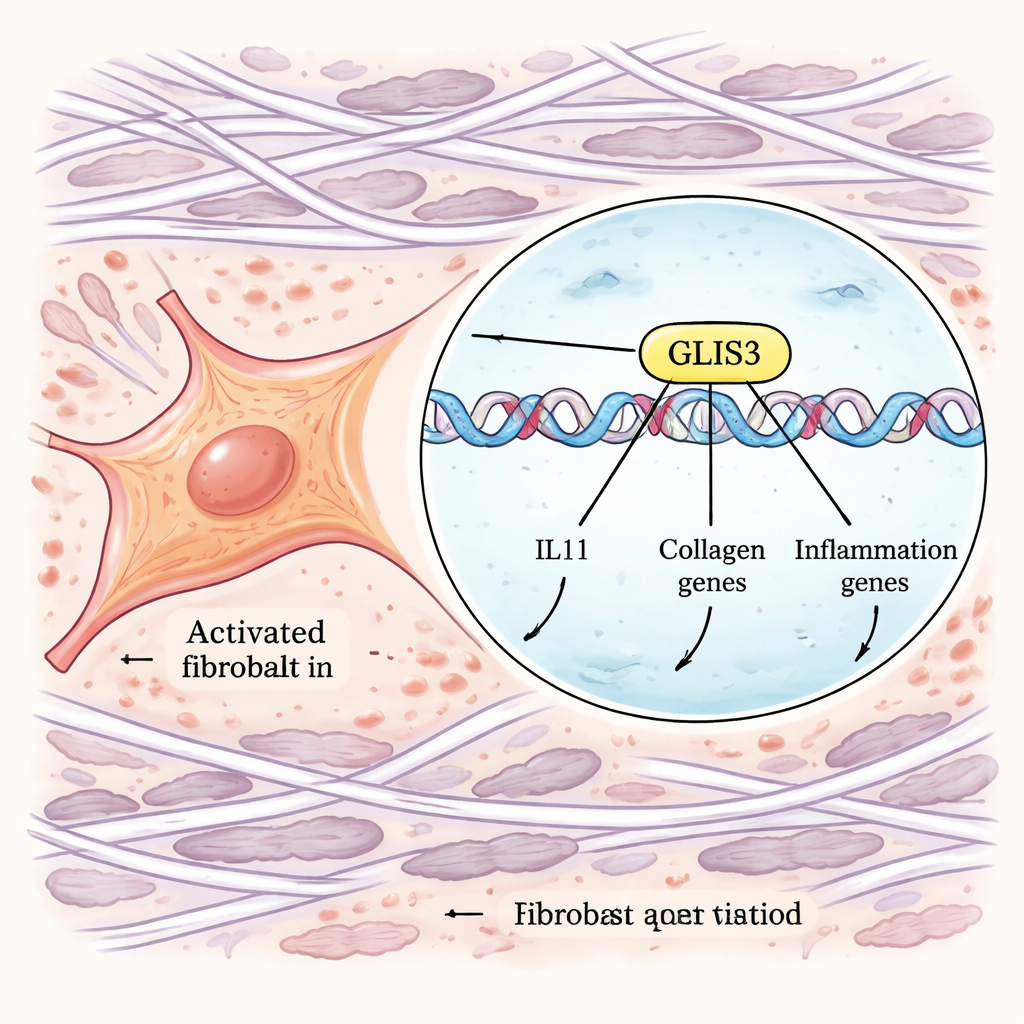
من نماذج الفأر إلى شدة المرض لدى المرضى
سأل الفريق بعد ذلك ما إذا كان برنامج GLIS3 هذا ذو أهمية في الكائنات الحية. في الفئران، أنشأوا سلالة يمكن فيها إزالة GLIS3 فقط من الخلايا الليفية. عندما خضعت هذه الحيوانات لالتهاب قولون مزمن، طورت ندباً معوياً أقل، وكانت مستويات الكولاجين وتعبير جينات التليف أقل، وأظهرت التهابية أقل مقارنة بالفئران الطبيعية. أكدت الخرائط المكانية أن الفئران الخالية من GLIS3 كان لديها خلايا ليفية منتجة للـIL-11 أقل وبها عدد أقل من البلعمات والمختلطات المحفزة القريبة، مما يشير إلى أن تعطيل GLIS3 يضعف الدائرة الالتهابية-الليفية بأكملها. بالانتقال إلى مجموعة كبيرة من الأطفال المصابين بالتهاب القولون التقرحي، استخلص المؤلفون «توقيعاً» مكوَّناً من 50 جيناً لـGLIS3 ووجدوا أن نشاطه في خزعات القولون ارتبط ارتباطاً وثيقاً بشدة المرض وبوفرة IAFs والبلعمات النشطة، ما يربط هذا المسار مباشرة بنتائج المرضى.
كسر حلقة الالتهاب والتندب
بالنسبة لغير المتخصصين، الخلاصة أن هذا العمل يكشف حلقة تعزز نفسها ذاتياً: البلعمات الملتهبة تحفز الخلايا الليفية لتصبح IAFs مكونة للندب؛ وهذه IAFs، تحت سيطرة GLIS3، تفرز IL-11 والكولاجين وعوامل أخرى تعيد تشكيل النسيج وتجذب خلايا التهابية إضافية. قد لا تَكْفِ الأدوية القياسية التي تُخمد الجهاز المناعي بشكل عام لكسر هذه الحلقة بالكامل، مما يفسر لماذا يفشل العديد من المرضى في النهاية في الاستجابة للعلاجات الحالية. من خلال تحديد GLIS3 وحالة الخلايا الليفية المنتجة لـIL-11 كنقاط مركزية في دائرة الالتهاب-التليف، تشير هذه الدراسة إلى استراتيجيات أكثر استهدافاً — موجهة إلى الخلايا الليفية بدلاً من التركيز على الخلايا المناعية فقط — التي قد تمنع أو تعكس التندب في مرض الأمعاء الالتهابي وربما في حالات التهابية مزمنة أخرى.
الاستشهاد: Pokatayev, V., Jaiswal, A., Shih, A.R. et al. Bidirectional CRISPR screens decode a GLIS3-dependent fibrotic cell circuit. Nature 650, 997–1006 (2026). https://doi.org/10.1038/s41586-025-09907-x
الكلمات المفتاحية: مرض الأمعاء الالتهابي, تندب معوي, الخلايا الليفية, البلعمات, GLIS3