Clear Sky Science · ar
الإجهاد يتحكم في وراثة الهايتروكروماتين عبر يوبكويتين للهستون H3
كيف تتذكر الخلايا الإجهاد
تحتاج خلايانا طرقًا لـ «تذكر» الإجهادات الماضية — مثل الحرارة، نقص المغذيات أو التعرض للأدوية — حتى تتمكن من الاستجابة بشكل أسرع في المرة التالية. أحد أنظمة الذاكرة الفعّالة يعتمد على الهايتروكروماتين، وهو DNA مضغوط بإحكام يبقي بعض الجينات مطفأة لعدة انقسامات خلوية. تستكشف هذه الورقة كيف تضبط الخلايا تلك الذاكرة بشكل نشط استجابةً للإجهاد، كاشفةً عن محور جزيئي يربط الإشارات البيئية بتغييرات طويلة الأمد في نشاط الجينات. قد يساعد فهم نظام التحكم هذا على تفسير كيف تطور الفطريات مقاومة للأدوية وكيف يعيد الإجهاد تشكيل المشهد فوق الجيني في خلايانا.
قفل على الجينوم
يمكن اعتبار الهايتروكروماتين كقفل جزيئي على امتداد أجزاء من الـ DNA، يحافظ على صمت الجينات القريبة. يُبنى هذا القفل من علامات كيميائية على بروتينات الهِستون، وخاصة العلامة المسماة H3K9me3. بمجرد إنشائه، يمكنه نسخ نفسه في كل مرة يُنسخ فيها الـ DNA، مما يسمح بوراثة أنماط قمع الجينات دون تغيير تسلسل الـ DNA الأساسي. حتى الآن، أشارت غالبية الأعمال إلى أن هذه النسخ الذاتي يعتمد بشكل رئيسي على حلقة تغذية راجعة «قراءة–كتابة»: مركب إنزيمي يتعرف على علامات H3K9me3 الموجودة ويضيف نفس العلامة إلى هستونات مجاورة، موسعًا تدريجيًا نطاق الصمت. لكن هذا النموذج لم يفسر تمامًا كيف تُسرِّع أو تُبطئ أو تُوجه الظروف البيئية انتشار الهايتروكروماتين.
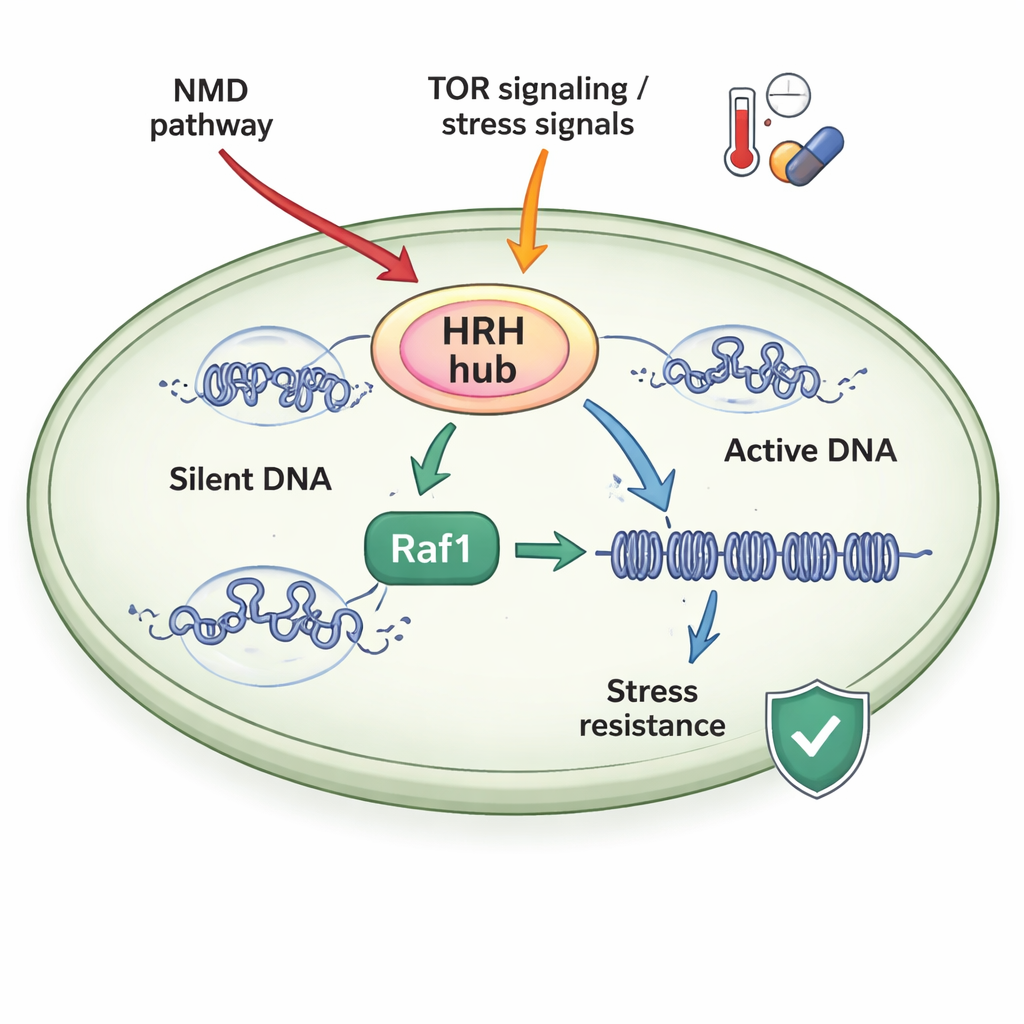
محور تحكم حساس للإجهاد
درس الباحثون خميرة الانقسام، كائن نموذجي بسيط تتشابه آليات الكروماتين فيه مع تلك الموجودة في الكائنات الأعلى. ركزوا على مركب يُدعى ClrC، الذي يكتب علامة H3K9me3 ويُلحق أيضًا بروتينًا صغيرًا، اليوبيكويتين، إلى موضع آخر على هستون H3 (H3K14ub). يلعب وحدة فرعية رئيسية في ClrC تُسمى Raf1 دور «بواب» محددة: عندما يكون Raf1 نادرًا، يَطفو كثير من الإنزيم الرئيسي (Clr4) بدلًا من الالتحاق بالمركب على الكروماتين، وتفشل نطاقات الصمت في الانتشار. عندما يكون Raf1 وفيرًا، يتجمع المزيد من ClrC ويرتبط بثبات بالـ DNA، مما يسمح لعلامتي H3K14ub وH3K9me3 بالتمدد على طول الكروموسومات وتعزيز كبت الجينات.
ضبط القفل باليوبيكويتين
من خلال رسم خرائط علامات الكروماتين عبر الجينوم، أظهر الفريق أن H3K14ub مُثرية للغاية في كل مكان يتشكل فيه الهايتروكروماتين وأن هذه العلامة تختفي عمليًا إذا أُزيل Raf1. عندما تحمل الخلايا طفرة تمنع خطوة إضافة اليوبيكويتين (مع بقاء H3K9me3 سليمًا عند نقطة الانطلاق)، تعجز نطاقات الصمت عن الانتشار إلى الخارج. بعبارة أخرى، H3K14ub ليست مجرد زينة؛ بل هي مطلوبة لدفع جبهة الهايتروكروماتين إلى الأمام. تكشف التجارب البيوكيميائية والتصويرية عن السبب: H3K14ub يعزز بشكل كبير نشاط إنزيم Clr4 ويساعد في إبقاء المركب كله مثبتًا على الكروماتين، رافعًا كثافة H3K9me3 المحلية فوق العتبة اللازمة للوراثة المستقرة. ومن اللافت أن زيادة مستويات Raf1 يمكن أن تعوض عن عدة عوامل أخرى عادةً ما تكون ضرورية للحفاظ على هذه النطاقات الصامتة، مما يؤكد أن اليوبيكويتلة المدفوعة بـ Raf1 هي رافعة تحكم مركزية.
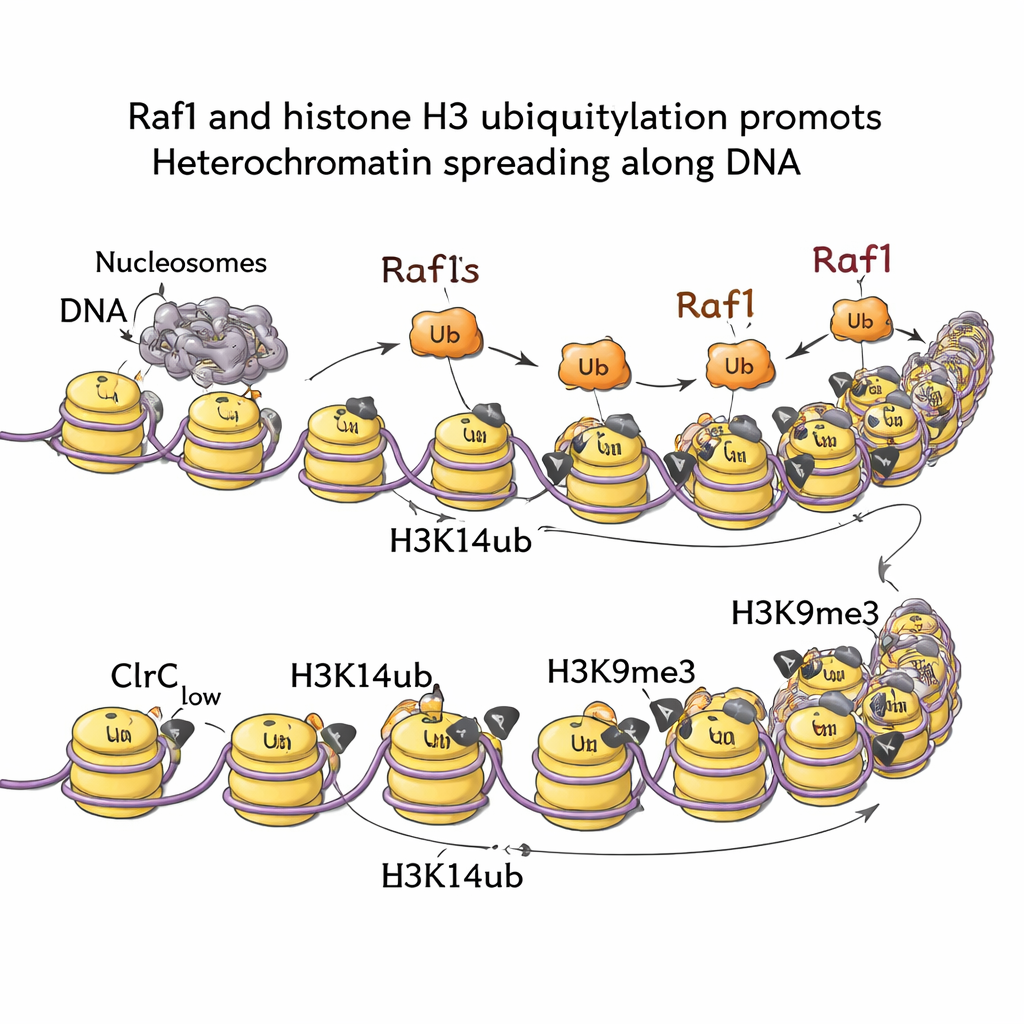
إشارات من مسارات تحلل الـ RNA والنمو
الخلايا لا تترك مستويات Raf1 للصدفة. تُظهر الدراسة أن نظامين رئيسيين مستجيبين للإجهاد يندمجان في ما يسميه المؤلفون محور تنظيم وراثة الهايتروكروماتين (HRH)، المرتكز على Raf1. أولاً، مسار التحلل المعتمد على الأخطاء (NMD) — المعروف بتدمير رسائل الـ mRNA المعيبة — يستهدف الرسالة التي تشفر Raf1، محافظًا بذلك على مستويات Raf1 منخفضة في الظروف العادية. تعطيل NMD يثبت RNA الخاص بـ Raf1، يزيد من وفرة بروتين Raf1 ويعيد انتشار الهايتروكروماتين في طفرات لا تستطيع خلاف ذلك الحفاظ على نطاقات الصمت. ثانيًا، مستشعر النمو والإجهاد المسمى TORC2، الذي يعمل عبر الكيناز Gad8، يعزز تعبير Raf1. الحرارة العالية تطفئ هذا المسار، مما يخفض مستويات Raf1 ويضعف الهايتروكروماتين ويجعل من الصعب على الخلايا الحفاظ على حالات الصمت ما لم يُرفع Raf1 تجريبيًا.
الإجهاد، مقاومة الدواء والدلالات الأوسع
ربط المؤلفون بعد ذلك هذا المحور الجزيئي بالتكيف في العالم الحقيقي. تعريض الخميرة للكافيين، وهو إجهاد معروف أيضًا بأنه يضعف NMD في أنظمة أخرى، يرفع مستويات Raf1 ويعزز انتشار الهايتروكروماتين إلى مواقع جديدة، بما في ذلك جينات يؤدي كبتها إلى مقاومة للكافيين والأدوية المضادة للفطريات. وبالمثل، تصبح الخلايا التي يُرفع فيها Raf1 صناعيًا أكثر مقاومة للفلوكونازول والكلوتريمازول، وهما عاملان مضادان للفطريات شائعان. وعلى العكس، عندما يُخفض Raf1 — بالحرارة أو بفقدان إشارات TORC2–Gad8 — يصبح الهايتروكروماتين غير مستقر وتتلاشى الذاكرة فوق الجينية، ما لم يُستعد Raf1. ونظرًا لأن بروتينات شبيهة بـ Raf1 ومركب ClrC وعلامة H3K14ub لها نظائر في الفطريات الممرضة والفقاريات، تشير هذه النتائج إلى أن محورًا مشابهًا لاستشعار الإجهاد قد يشكل المقاومة للأدوية والتطور والمرض في العديد من الأنواع.
لماذا هذا مهم
بمصطلحات يومية، تُظهر هذه الدراسة أن كبت الجينات بواسطة الكروماتين ليس قفلًا جامدًا بل نظام ذكي قابل للتعديل. تستخدم الخلايا محورًا مركزيًا لقراءة الإشارات البيئية — تغيرات الحرارة، حالة المغذيات، الضغوط الكيميائية — وتدور مقياس Raf1 صعودًا أو هبوطًا. وهذا بدوره يتحكم في مقدار الجينوم المغلف في صمت طويل الأمد ومدى سهولة «إعادة برمجة» الخلايا دون طفرات في الـ DNA. من خلال كشف الدور الرئيسي لليوبيكويتلة على هستون H3 وجرعة Raf1 في هذه العملية، توفر الدراسة مخططًا لكيفية قدرة الإجهاد على إعادة تشكيل المشهد فوق الجيني بسرعة — وتلمح إلى طرق جديدة للتأثير على مقاومة الفطريات للأدوية أو كبت الجينات الشاذ في الأمراض البشرية.
الاستشهاد: Bhatt, B., Wei, Y., Pradhan, A.K. et al. Stress controls heterochromatin inheritance via histone H3 ubiquitylation. Nature 650, 768–778 (2026). https://doi.org/10.1038/s41586-025-09899-8
الكلمات المفتاحية: الهايتروكروماتين, الوراثة فوق الجينية, يوبيكويتينيشن للهستون, التكيف مع الإجهاد, مقاومة الفطريات للأدوية