Clear Sky Science · ar
حويصلات محاكية حية مصمّمة من خلايا ورمية معدّلة تعمل كلقاحات مخصّصة للمناعة بعد الجراحة ضد السرطان
تحويل بقايا الورم إلى خط دفاع ثانٍ
بالنسبة للكثير من المرضى المصابين بأورام صلبة، تظل الجراحة الجولة الأولى فقط في معركة طويلة. حتى بعد استئصال جزء كبير من الورم، قد تهرب مجموعات صغيرة من الخلايا السرطانية وتؤسس نقائل قاتلة لاحقًا. تستكشف هذه الدراسة طريقة مبتكرة لتحويل خلايا ورمية من المريض نفسه إلى لقاح شخصي، مصمّم لتتبع هذه البقايا بعد الجراحة ومساعدة الجهاز المناعي على منع تكرار السرطان.
لماذا يصعب القضاء على الخلايا السرطانية المتبقية
تواجه العلاجات القياسية صعوبة مع الخلايا التي تبقى بعد إزالة الكتلة الورمية الرئيسية من قبل الجراح. غالبًا ما تختبئ هذه الخلايا المبعثرة في أعضاء بعيدة وتكون محمية من الأدوية وهجمات الجهاز المناعي. تحاول اللقاحات المناعية الحالية تدريب الجسم على التعرف على علامات الورم باستخدام خلايا مناعية متخصصة تُسمى الخلايا التغصنية، لكن هذه اللقاحات الحية صعبة التصنيع، ولا تنتقل بكفاءة إلى الأعضاء المناعية الحيوية، وأظهرت فوائد متواضعة في العيادات. والتحدي المركزي هو أن كل ورم لدى مريض يحمل مزيجًا فريدًا من الطفرات، لذلك فإن اللقاحات ذات المقاس الواحد لا تلائم الجميع عادة وتفشل في استهداف عناصر مهمة.
مفتاح خفي يجعل خلايا السرطان أكثر وضوحًا
بدأ الباحثون بالبحث عن مفاتيح طبيعية في النظام المناعي تجعل الخلايا أفضل في عرض محتوياتها للكاميرات المناعية. ركّزوا على بروتين يُدعى سينتاكسين 11، وهو موجود بكثرة عادة في الخلايا المناعية لكن نادر في كثير من الأورام. بزيادة هذا البروتين في خلايا سرطان الثدي العدوانية المستمدة من نماذج فأرية، وجدوا أن الخلايا السرطانية بدأت تتصرف أشبه بالمرقّبات المناعية المهنية: أظهرت مستويات أعلى من «بطاقات تعريف» جزيئية وإشارات مساعدة على سطحها. بفعالية، أعيد برمجة خلايا الورم للكشف عن المزيد من ميزاتها الفريدة للجهاز المناعي بدلًا من إخفائها.
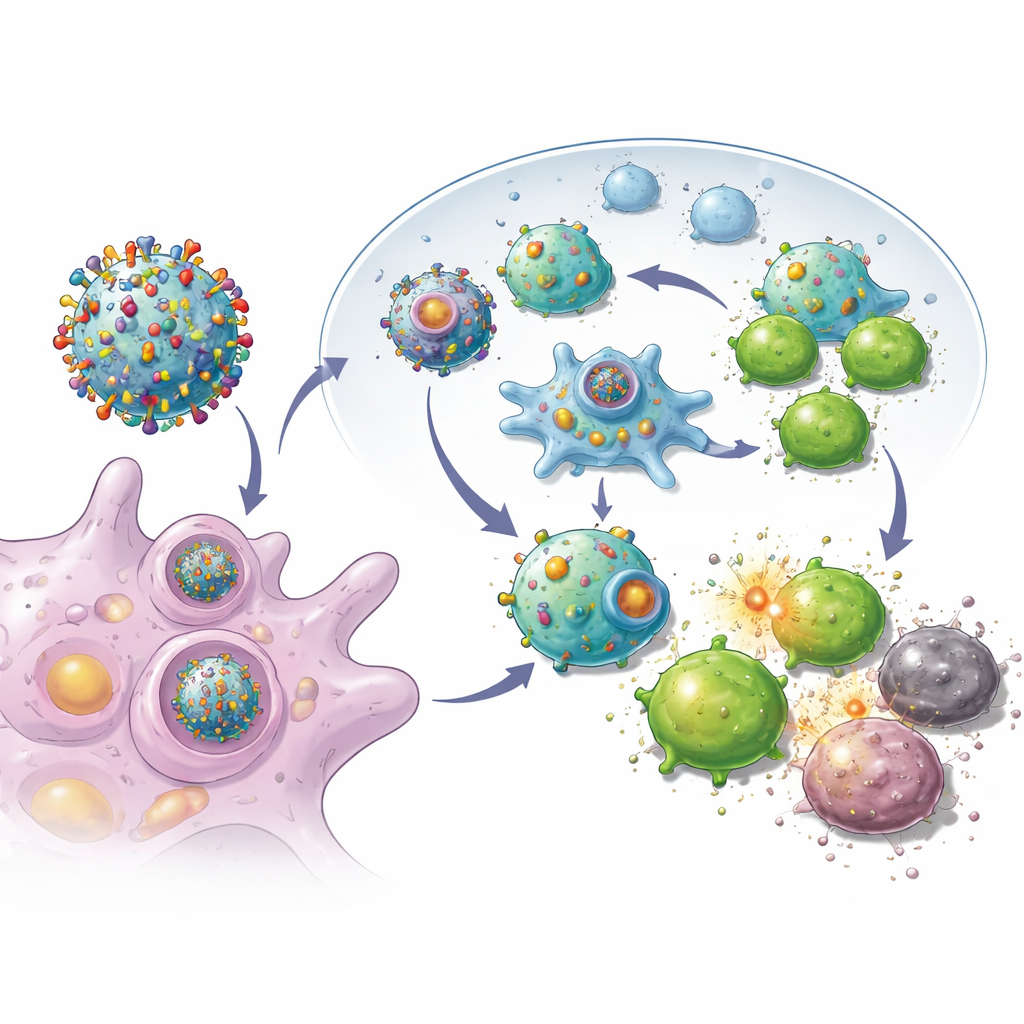
بناء مراسلات مناعية صغيرة مقلدة
مزوّدين بهذه الخلايا الورمية المعاد برمجتها، جرد الفريق أغشية هذه الخلايا الخارجية واستخدمها لتغطية جزيئات نانوية قابلة للتحلل محمّلة بعقار صغير منشط للمناعة. النتيجة كانت سربًا من الفقاعات النانوية، كل واحدة تحمل المجموعة الكاملة من علامات ذلك الورم بالإضافة إلى إشارات «انطلق» مدمجة للخلايا التائية القاتلة. عند حقنها تحت جلد الفئران بعد الجراحة، انتقلت هذه الحويصلات بكفاءة إلى العقد اللمفاوية القريبة، حيث يتم تدريب الخلايا المناعية. هناك استطاعت أن تتفاعل مباشرة مع الخلايا التائية القاتلة وأن تُبتلع بواسطة المرقّبات المناعية الطبيعية، التي عززت الاستجابة لاحقًا. أظهرت التجارب أن الخلايا التائية المعرضة لهذه الحويصلات تضاعفت بنشاط أكبر وكانت أفضل في تدمير الخلايا السرطانية مقارنة بتلك المنشطة بتصاميم نانوية أبسط.
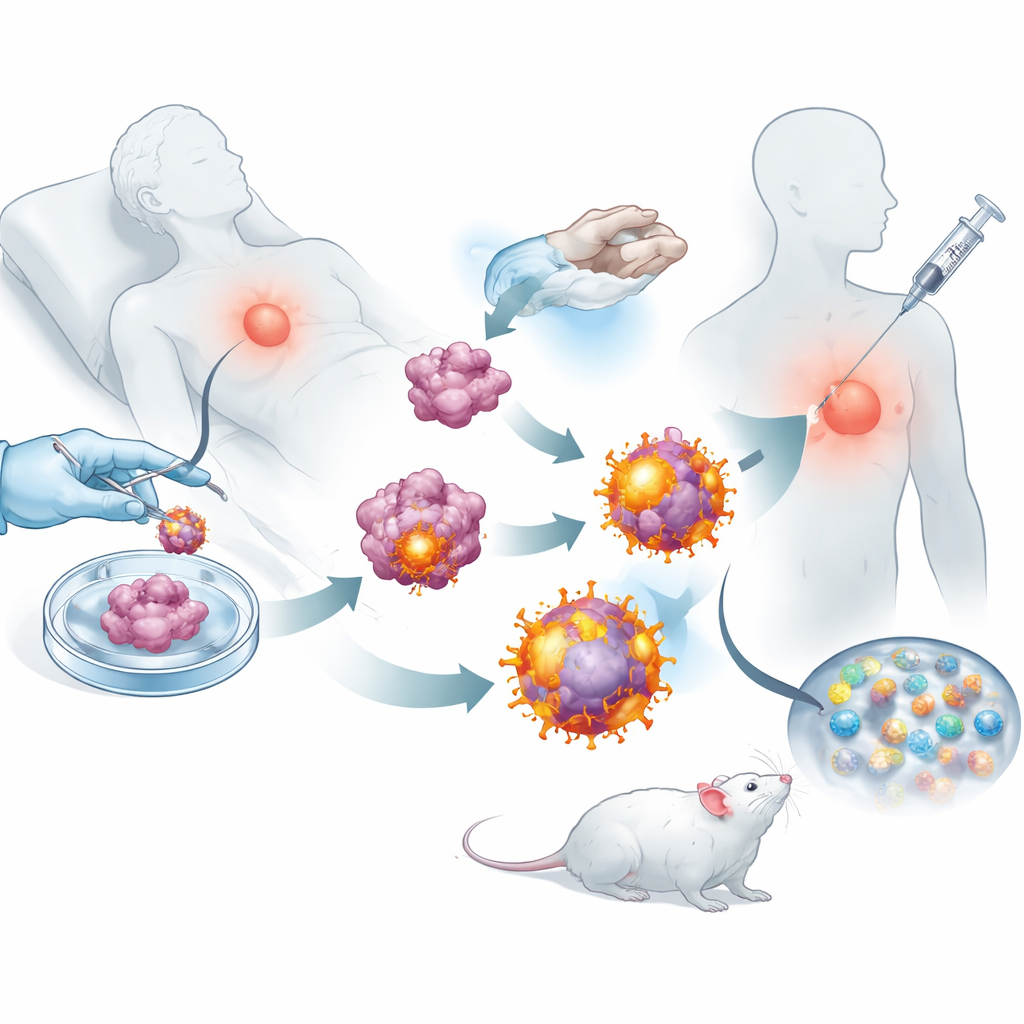
إبقاء السرطان تحت السيطرة بعد الجراحة
باستخدام عدة نماذج فأرية لسرطان الثدي والورم الميلانيني، اختبر الباحثون ما إذا كان هذا اللقاح المفصّل يمكن أن يغير فعليًا مسار المرض. في الحيوانات التي أُزيلت منها معظم كتلة الورم الثديي جراحيًا، طورت الفئران الملقّحة تكرارات أصغر ونقائل رئوية أقل بكثير من الحيوانات غير المعالجة. كانت العقد اللمفاوية والطحال والأورام من الفئران المعالجة تعج بالخلايا التائية القاتلة النشطة وخلايا الذاكرة طويلة العمر، مما يشير إلى أن الجهاز المناعي قد استُيقظ وتدرّب على المدى الطويل. عند الجمع بين اللقاح وجرعة من جسم مضاد معتمد يعرقل نقاط تفتيش مناعية وتمنع الأورام من شلّ الخلايا التائية، أدت المعالجة إلى تحكم مطوّل في الورم وفي كثير من الفئران إلى تراجع كامل وبقاء طويل الأمد.
تسريع علاج مخصص
أحد العقبات أمام تحويل هذا المفهوم إلى علاج واقعي هو الزمن: طرق تعديل الجينات لإعادة برمجة خلايا الورم قد تكون بطيئة. لمواجهة ذلك، فحص الفريق مركبات طبيعية واكتشف مركب ديأوكسيبودوفيلوتوكسين، وهو جزيء صغير يرفع بسرعة مستويات بروتين المفتاح ونفس علامات السطح المحفزة للمناعة. باستخدام هذا الاختصار، بنوا حويصلات مغطاة بالغشاء مشابهة على جزيئات نانوية في وقت أقصر مع الحفاظ على قدرتها على إيقاظ استجابات مناعية قوية ومحددة للورم. أظهرت الاختبارات أن اللقاحات المصنوعة بهذا العقار كانت فعّالة بنفس قدر تلك المنتجة بالطريقة الجينية، وكانت فوائدها تعتمد على التعرف على نوع الورم الصحيح بدلًا من سمية عامة للخلايا السرطانية.
ماذا قد يعني هذا لرعاية السرطان في المستقبل
الرسالة الأساسية لغير المتخصص هي أن ورم المريض نفسه يمكن إعادة تشكيله إلى أداة تدريب مصغّرة للجهاز المناعي. بتحويل الخلايا السرطانية إلى مصادر لمعلومات شخصية غنية وتغليف تلك المعلومات على ناقلات نانوية متينة، يهدف هذا النهج إلى اقتناص الخلايا التي تتركها الجراحة ومنع نمو بؤر جديدة. وبينما تبقى خطوات كثيرة قبل أن تُعرض مثل هذه اللقاحات بشكل روتيني على البشر — بما في ذلك إثبات السلامة والفعالية في أورام بشرية وبناء سلاسل تصنيع موثوقة — يرسم هذا العمل طريقًا نحو علاجات بعد الجراحة عالية التخصيص تستنفر دفاعات الجسم لإكمال ما بدأه الجراح.
الاستشهاد: Yu, P., Jin, Z., Meng, L. et al. Biomimetic vesicles engineered from modified tumour cells act as personalized vaccines for post-surgical cancer immunotherapy. Nat. Nanotechnol. 21, 443–454 (2026). https://doi.org/10.1038/s41565-025-02113-w
الكلمات المفتاحية: لقاح السرطان, المناعة العلاجية, الطب النانوي, العلاج بعد الجراحة, أورام مخصصة