Clear Sky Science · ar
التحليل المقارن لمجموعات بيانات المسح الطافح للطفرات العميقة في الفيروسات المعوية من النوع A وB يكشف عن تباين وظيفي وأهداف علاجية
لماذا تهمنا الفيروسات الريبية الصغيرة
الفيروسات المعوية هي مجموعة كبيرة من الفيروسات الريبية الصغيرة التي تدور بهدوء في أنحاء العالم، وعادة ما تسبب نزلات برد خفيفة أو مشاكل معوية، ولكنها في بعض الأحيان تؤدي إلى شلل أو تلف في القلب أو أمراض شديدة أخرى. لدينا لقاحات قليلة وعدد أقل من الأدوية الفعالة ضدها على نطاق واسع، جزئياً لأن هذه الفيروسات تتطور بسرعة. تطرح هذه الدراسة سؤالاً يبدو بسيطاً لكنه ذو تبعات عملية كبيرة: عندما تتحور هذه الفيروسات، أي أجزاء من أداتها يمكنها التغير بحرية، وأي أجزاء حيوية لدرجة أن التطور يُبقيها ثابتة تقريباً؟ تشير الإجابات إلى استراتيجيات جديدة لتصميم علاجات يصعب على الفيروس تفاديها.
قراءة كتاب التعليمات الفيروسي، طفرة واحدة في كل مرة
ركز الباحثون على فيروسين معويين بشريين يسببان أمراضاً مختلفة تماماً: فيروس المعوية A71 المرتبط بأمراض عصبية شديدة عند الأطفال، وفيروس كوكساكي B3 المرتبط بالتهاب القلب وحتى بسرطان البنكرياس. باستخدام تقنية تسمى المسح الطافح للطفرات العميقة، أنشأوا مكتبات فيروسية تم فيها تغيير كل موضع تقريباً في بروتينات كل فيروس بشكل منهجي. أُتيح لهذه الفيروسات المطعّمة أن تصيب خلايا في المزرعة الخلوية، واستُخدمت تقنيات التسلسل عالية الإنتاجية لقياس كيف أثّر كل تغيير على نمو الفيروس. بمقارنة كل طفرة بالفيروس الأصلي، بنى الفريق خريطة مفصّلة للمواقع في البروتيوم الفيروسي التي تحتمل التغير وتلك التي تخضع لقيود شديدة. 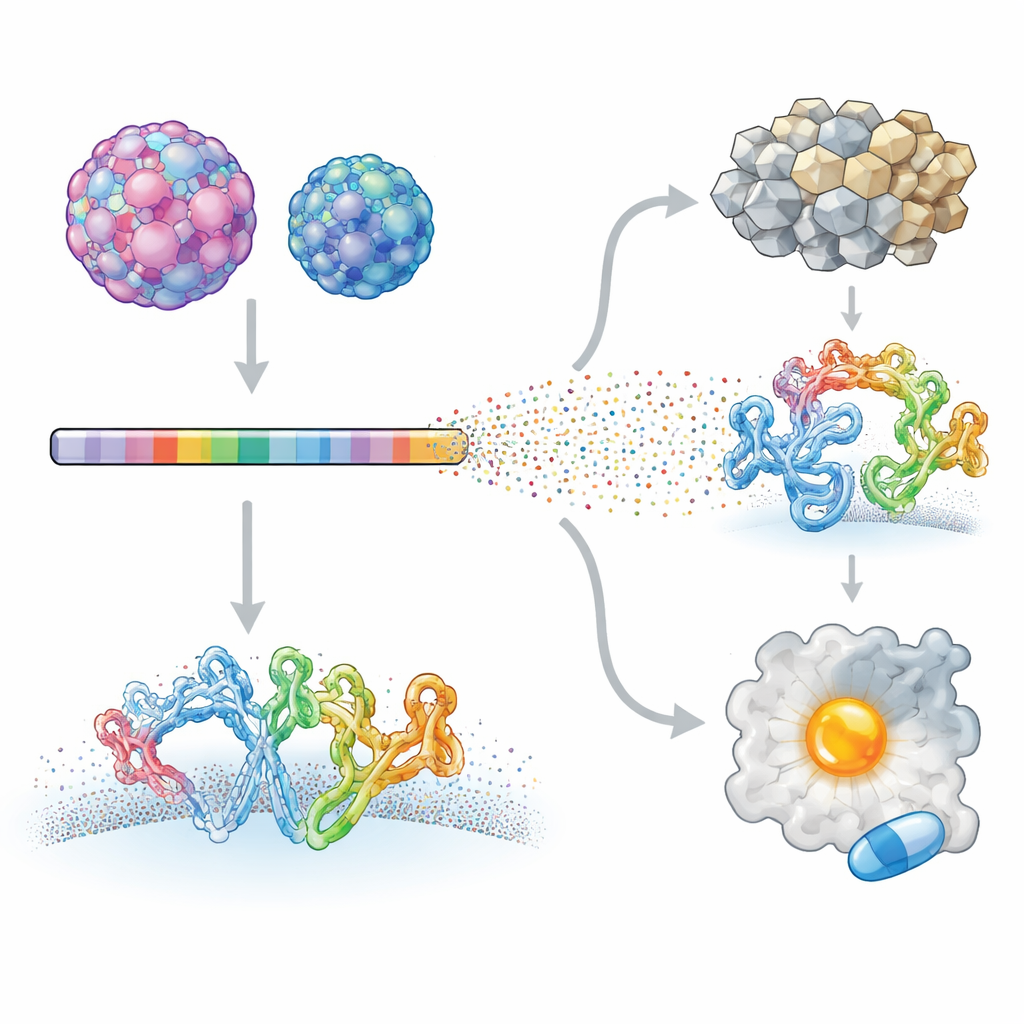
حدود صلبة مشتركة ومرونة خاصة بكل فيروس
بالرغم من تقاسمهما نحو نصف تسلسلات الأحماض الأمينية فقط، أظهر الفيروسان أنماط قيود إجمالية متشابهة بشكل لافت. كانت الإنزيمات الداخلية «الحصان العامل» التي تكرر الجينوم وتقص البروتينات وتفك الريبونوا مزيلة الهياكل حساسة جداً للطفرات في كلا الفيروسين. وبالمثل، ثبت أن الأسطح الخفية التي تمسك غلاف البروتين، أو الكبسيد، من الصعب تغييرها دون كسر الفيروس. بالمقابل، كانت العديد من المناطق المواجهة للخارج والمتفاعلة مع العائل أكثر حرية في التغير وغالباً ما اختلفت حدة بين النوعين. أظهر التحليل البنيوي أن المناطق المحفوظة والغير متحملة للطفرات تتركز حول المواقع الفعالة وواجهات التجميع، بينما كانت المناطق التي تلامس المستقبلات الخلوية أو الأغشية أو الجزيئات المناعية نقاطاً ساخنة من المرونة الخاصة بكل نوع.
كيف تلتقي الفيروسات بالخلايا وتتخطى الدفاعات
ثم ركز الفريق على المصافحة الجزيئية بين الفيروس والعائل. يستخدم فيروس المعوية A71 وفيروس كوكساكي B3 مستقبلات خلوية مختلفة للدخول، ووجدت الدراسة أن آثار الاتصالات الدقيقة على سطح الكبسيد هي من بين أكثر المناطق تبايناً من حيث تحمل الطفرات. الأحماض الأمينية التي تثبّت المستقبل بالنسبة لأحد الفيروسين تكون مقيدة بشدة في ذلك الفيروس لكنها متسامحة نسبياً في الآخر، مما يعكس كيف صقل كل منهما منصة الالتحام الخاصة به. ظهرت اختلافات مماثلة في بروتين صغير مرتبط بالغشاء يدعى 3A، يساعد في إعادة تشكيل الأغشية الخلوية واستقطاب عوامل العائل لتكرار الجينوم. اقترحت النمذجة أن الفيروسين يستخدمان رقع تلامس مختلفة جزئياً على 3A للتفاعل مع العامل الخلوي نفسه، GBF1، وقد يدخلان هذا البروتين في الأغشية بعمق مختلف أيضاً. تساعد هذه الاختلافات على تفسير سبب قدرة فيروسات قريبة وراثياً على إصابة أنسجة مختلفة وإثارة أنماط مرضية مميزة.
ما الذي تغفله التجارب المخبرية—وما الذي تصيبه
لوضع تجارب المزرعة الخلوية في سياق العالم الحقيقي، قارن المؤلفون خرائط الطفرات الخاصة بهم مع آلاف تسلسلات الفيروسات الطبيعية من عينات مرضى. عموماً، تميل المواقع التي كانت مرنة في المختبر إلى أن تكون متباينة أيضاً في الطبيعة، لا سيما عبر مقارنات على مستوى النوع. ومع ذلك، عندما فحصوا أي أحماض أمينية محددة مفضلة في كل موقع، اتفقت التطور الطبيعي والانتقاء المخبرّي بشكل أوثق داخل نوع فيروسي واحد. من اللافت أن أكبر نقاط الاختلاف تجمعّت على سطح الكبسيد الخارجي وعلى مناطق التفاعل مع العائل في البروتينات غير التركيبية 2A و3A—وهي بالضبط الأماكن التي من المتوقع أن يكون للمناعة والبيئات المعقدة للعائل تأثير أكبر. هذا يوحي بأن المسح الطافح للطفرات العميق يلتقط القيود الميكانيكية الأساسية لبروتينات الفيروس، بينما تفرض العدوى الحقيقية ضغوطاً إضافية من المناعة وتوجه النسيج التي يصعب إعادة إنتاجها في المختبر.
إيجاد نقطة ضعف مشتركة للأدوية المستقبلية
أخيراً، تساءل الباحثون ما إذا كانت هذه الخرائط يمكن أن تسلّط الضوء على كعب أخيل مشترك لتطوير الأدوية. باستخدام أدوات حاسوبية، بحثوا في كلا الفيروسين عن جيوب على أسطح البروتين يمكن أن تربط، من حيث المبدأ، جزيئات صغيرة فعّالة دوائياً. ثم غطّوا هذه الجيوب ببيانات الطفرات لرؤية أي الجيوب تتألف من بقايا لا يستطيع الفيروس تغييرها بسهولة دون أن يضر نفسه. برزت جيب واحد يقع على حلزونية 2C—محرك حلقي يساعد على فك شريط الحمض النووي الريبي الفيروسي. شكله وبقاياه المكونة محفوظة بشدة عبر أربعة أنواع رئيسية من الفيروسات المعوية البشرية، وهو بعيد عن المواقع الفعالة المعروفة، والتغيرات هناك نادرة في الطبيعة ومؤذية بشدة في اختبارات المختبر.
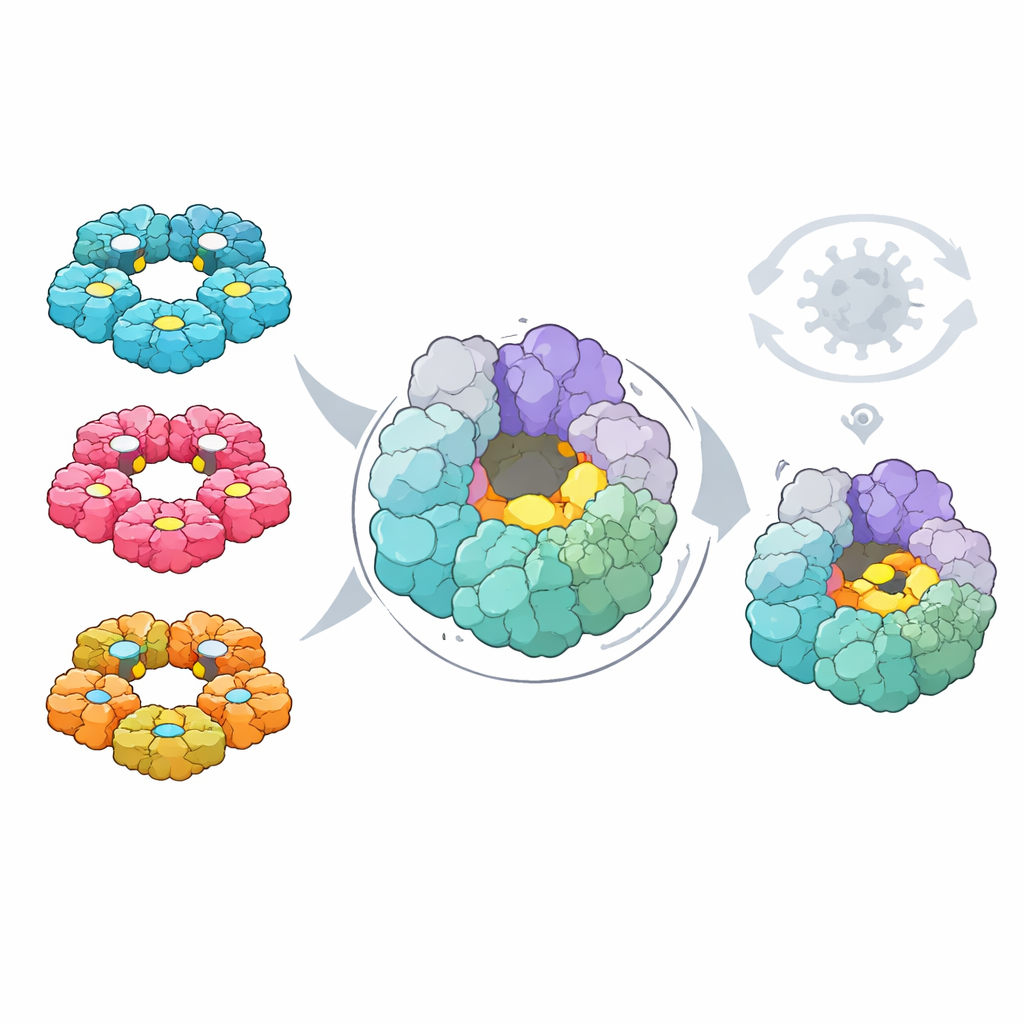
ما الذي يعنيه هذا للعلاجات المستقبلية
من خلال استقصاء منهجي لكيفية تأثير كل تغيير أحادي الحرف على فيروسين معويين مهمين، تكشف هذه الدراسة عن تقسيم واضح بين نواة فيروسية مشتركة وصلبة وواجهات أكثر مرونة خاصة بكل فيروس تتفاعل مع العائل. تشمل النواة المحفوظة جيباً جديد الإبراز على حلزونية 2C يبدو من الصعب على الفيروس أن يتحور فيه دون أن يفقد لياقته، مما يجعله هدفاً جذاباً لمضادات فيروسية واسعة الطيف ذات حاجز عالٍ لظهور المقاومة. في الوقت نفسه، تفسر الأسطح الخارجية الأكثر قابلية للتكيف ومواقع التماس مع العائل سبب اختلاف سلوك الفيروسات المماثلة داخل الجسم، وتوضح أين يجب أن تواجه اللقاحات والعلاجات المناعية التطور السريع. معاً، تقدم هذه النتائج خارطة طريق لتصميم علاجات تستغل حدود الفيروس التطورية نفسها.
الاستشهاد: Álvarez-Rodríguez, B., Bakhache, W., McCormick, L. et al. Comparative analysis of deep mutational scanning datasets in enteroviruses A and B identifies functional divergence and therapeutic targets. Nat Ecol Evol 10, 467–480 (2026). https://doi.org/10.1038/s41559-026-02993-8
الكلمات المفتاحية: الفيروسات المعوية, تطور فيروسي, المسح الطافح للطفرات العميقة, أهداف مضادة للفيروسات, حلزونية 2C