Clear Sky Science · ar
منتجات زائفة أحادية التكافؤ تُعزّز تفكّك IDO1 عبر E3 الأصلي KLHDC3
إيقاف إنزيم يساعد السرطان
جهازنا المناعي يراقب باستمرار الخلايا السرطانية، لكن الأورام غالباً ما ترد باختطاف كيمياء الجسم نفسها. لاعب رئيسي في هذا الصراع هو إنزيم يُدعى IDO1، الذي يساعد الأورام على تعطيل الخلايا المناعية. تصف هذه الدراسة فئة جديدة من الجزيئات الصغيرة التي تفعل أكثر من مجرد حجب نشاط IDO1 — إذ تقنع الخلايا بالتخلّص من الإنزيم تماماً. عن طريق تسخير جهاز التخلص من النفايات الطبيعي في الخلايا، قد تعيد هذه المركبات الهجوم المناعي على الأورام بطرق لم تستطع الأدوية القديمة تحقيقها.
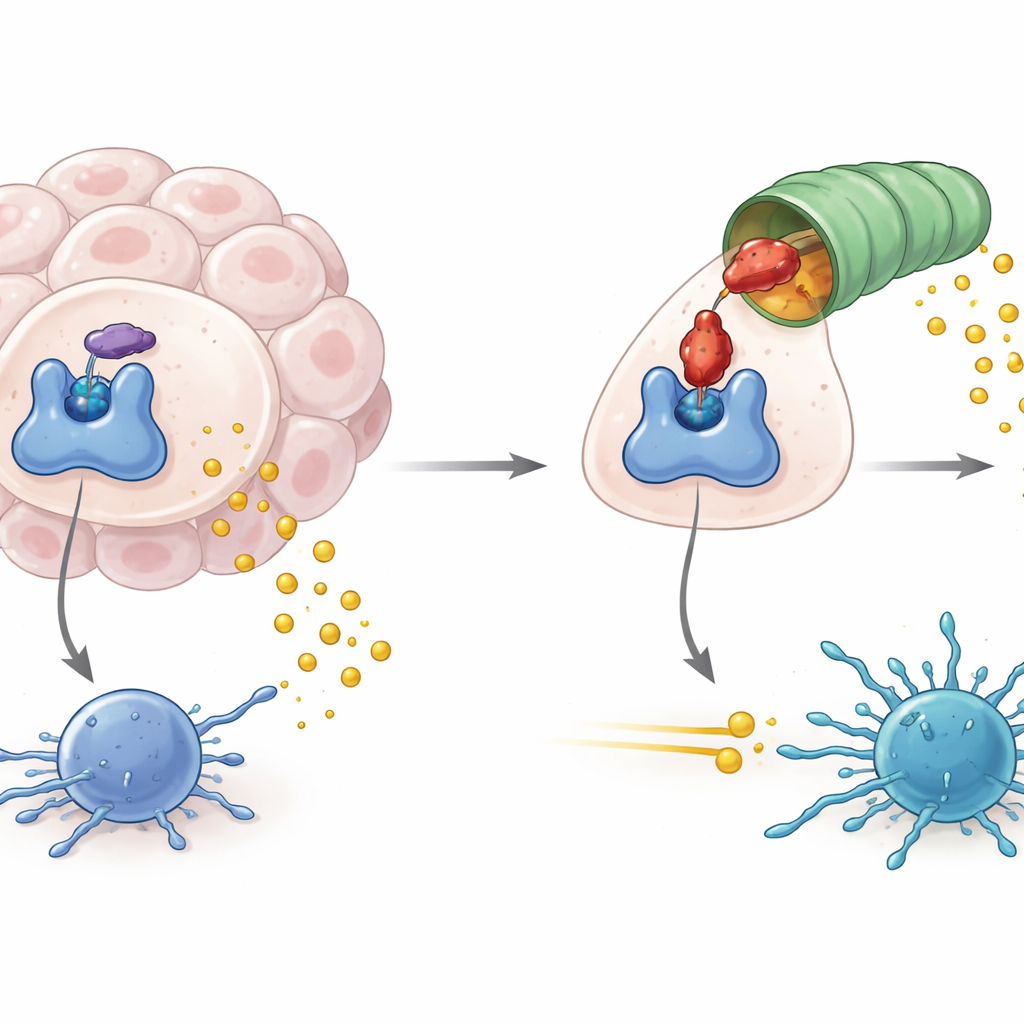
كيف تستغل الأورام بوابة أيضية
يقع IDO1 عند مدخل مسار أيضي يكسر الحمض الأميني التربتوفان إلى منتج يُسمى كينورينين. عندما يكون IDO1 وفيراً ونشيطاً، تنخفض مستويات التربتوفان ويرتفع الكينورينين، ما يخلق بيئة كيميائية تقلل من نشاط الخلايا المناعية، بما في ذلك خلايا T المقاتلة للأورام. رُبط النشاط العالي لـ IDO1 ليس فقط بضعف المناعة المضادة للأورام بل أيضاً بسرطانات الغدد اللمفاوية المرتبطة بالفيروسات وبعض أشكال التنكس العصبي. لذلك ركز مطورو الأدوية على حجب نشاط إنزيم IDO1 على أمل قطع هذا الإشارة المضعفة للمناعة ومساعدة العلاجات المناعية الحالية على العمل بشكل أفضل.
لماذا قصر حُجُب الإنزيم التقليدية على نفسها أدى إلى إخفاقات
رغم نتائج قوية في الدراسات الحيوانية، كانت التجارب السريرية لمثبطات IDO1 التقليدية مخيبة للآمال. تفسير ناشئ هو أن IDO1 أكثر من مجرد محفز كيميائي. حتى عندما يُحجب نشاطه الكيميائي، يمكن للبروتين نفسه أن يعمل كمحور إشارية لا يزال يعزز نمو الورم وانتشاره. بعض المثبطات تؤدي حتى إلى استقرار IDO1، ما يزيد كمية البروتين في الخلايا. بعبارة أخرى، إيقاف الوظيفة التحفيزية وحدها قد يترك أدواره غير الإنزيمية المؤيدة للورم دون تغيير — أو أسوأ، قد يقويها فعلياً.
تصميم مركبات تُحفّز التدمير الذاتي
بحث المؤلفون في مكتبة كبيرة من الجزيئات «الزائفة الطبيعية» — مركبات صناعية مبنية من شظايا مستوحاة من المنتجات الطبيعية لكن مُركّبة بطرق جديدة. وجدوا عائلة من الجزيئات سمّوها iDegs، مشتقة من لبنة نباتية تُعرف باسم (−)-myrtanol. ترتبط هذه المركبات داخل الجيب الاعتيادي لـ IDO1 المخصّص لمرافقه الحاوي على الحديد، الهيم. عبر إزاحة الهيم، تُضعف iDegs قدرة IDO1 على إنتاج الكينورينين والأهم من ذلك أنها تعيد تشكيل جزء من ذيل البروتين. تكشف هياكل بلورية عالية الدقة أنه عندما تشغل iDegs موضع الهيم، فإنها تُرخي وتُشوّه جزئياً حلزوناً في الطرف الكربوكسيلي C- النهائي كان عادةً محفوظاً في تكوّن مضغوط ومحمي.
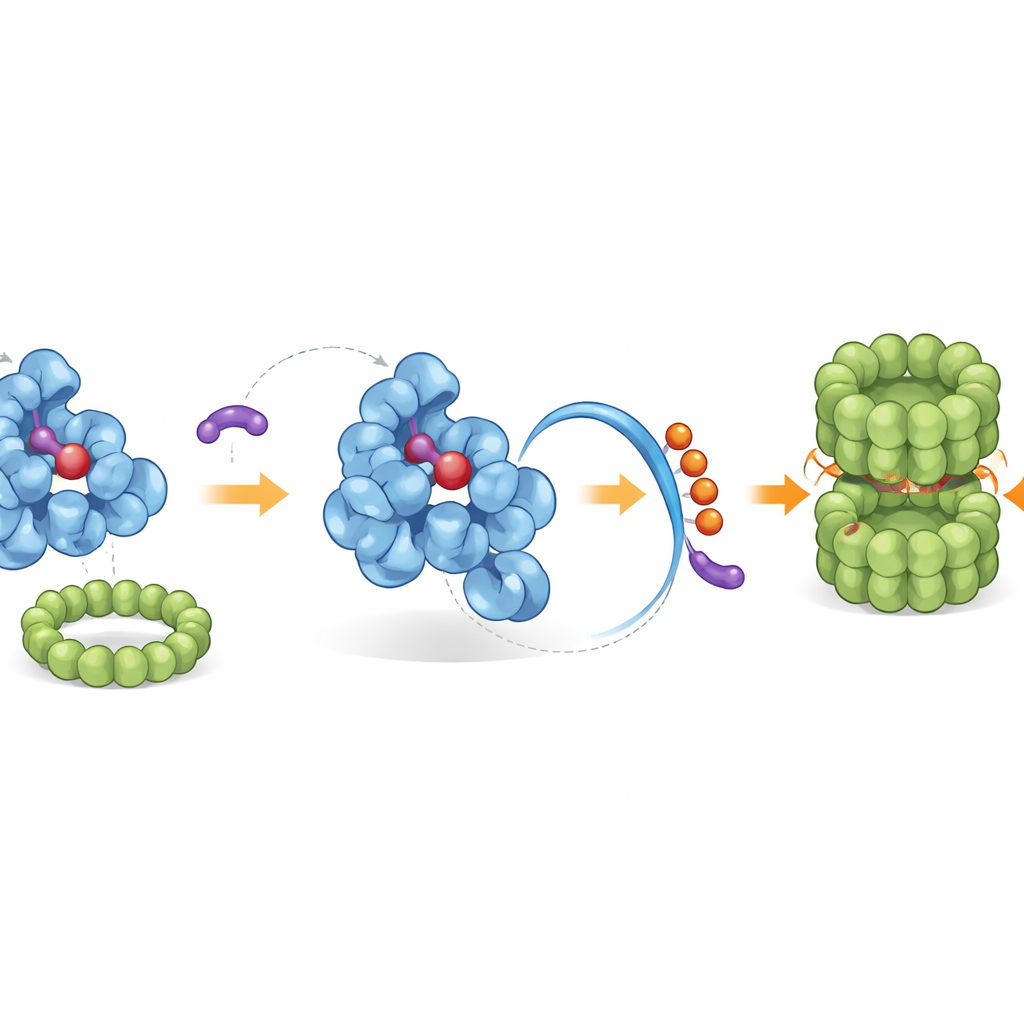
استدعاء طاقم التنظيف الخلوي الأصلي
يكشف الذيل المُعاد تشكيله عن «شارة نهاية» مدمجة يتعرف عليها جهاز التخلص من النفايات في الخلية. باستخدام فحوصات جينية وإعادة التكوين البيوكيميائي، حدد الباحثون مركب ليغاز محدداً، يُدعى CRL2–KLHDC3، يعلّق طبيعياً رايات يوبكويتين صغيرة على ذيل IDO1 المكشوف، مُعلماً إياه للتدمير عبر البروتيازوم — المُمزّق الجزيئي في الخلية. في الظروف الطبيعية، يُعلّق بهذه الكفاءة الشكل الخالي من الهيم من IDO1 فقط، بينما يكون IDO1 المرتبط بالهيم محمياً. تُقلب iDegs هذا التوازن بارتباطها فقط بالشكل الخالي من الهيم، مضخّمةً مسار التدهور الطبيعي. أعضاء قوية من السلسلة لا يحجبون إنتاج الكينورينين فحسب، بل يزيدون أيضاً من وسم اليوبكويتين على IDO1 ويقلّلون بشكل حاد من مستوياته البروتينية عبر عدة أنواع خلوية سرطانية.
تغيير مصير IDO1 — والاستجابات المناعية
لهذه السلوكيات ثنائية الفعل نتائج وظيفية مهمة. في اختبارات الهجرة باستخدام خلايا سرطان المبيض، أدى مثبط IDO1 المستكشف سريرياً والذي يثبّت الإنزيم فعلياً إلى تسريع حركة الخلايا، متماشياً مع الدور غير الإنزيمي المؤيد للورم لـ IDO1. بالمقابل، أبطأت مركبة من فئة iDeg الهجرة، متوافقة مع كل من تثبيط الإنزيم وفقدان البروتين نفسه. تكشف الدراسة بذلك عن طريقة جديدة للتحكم في IDO1: ليس عن طريق سحبه قسراً إلى ليغاز خارجي ضخم بواسطة جزيء مصمم، بل عن طريق «تعزيز» مسار تدهور أصلي موجود بالفعل في الخلايا.
ماذا قد يعني هذا لعلاجات السرطان المستقبلية
لغير المتخصّصين، الرسالة الأساسية هي أن الجودة — وليس الكمية فحسب — لمثبط الإنزيم مهمة. تعمل هذه الجزيئات الصغيرة الجديدة كمفاتيح دقيقة: تقفل IDO1 في شكل هش تكون الخلية مُهيّأة لتدميره، مقطعة بذلك مساهماته الأيضية والإشارية في بقاء الورم. ونظراً لأن iDegs مدمجة وبعيدة عن التعقيد الشكلي الدوائي وتعتمد على ليغاز الخلية لإزالة IDO1، فقد تقدم نهجاً أكثر دقة وقابلية للتطبيق على نطاق أوسع من أدوية «مُدَمِّرات البروتين» السابقة. إذا أمكن تطبيق استراتيجيات مماثلة على بروتينات مشكلة أخرى، فإن هذا العمل يشير إلى جيل جديد من العلاجات التي تُحفّز الخلايا المريضة على تفكيك أسلحتها الجزيئية بنفسها.
الاستشهاد: Hennes, E., Lucas, B., Scholes, N.S. et al. Monovalent pseudo-natural products supercharge degradation of IDO1 by its native E3 KLHDC3. Nat. Chem. 18, 585–596 (2026). https://doi.org/10.1038/s41557-025-02021-5
الكلمات المفتاحية: IDO1, العلاج المناعي للسرطان, استهداف تدهور البروتين, ليغاز يوبكويتين, مزيلات الجزيئات الصغيرة