Clear Sky Science · ar
موازنة الراوابط المتوافقة حيوياً في تنسيق المعادن الانتقالية تمكّن الأريلنة اللطيفة للبروتينات داخل الخلايا
تحويل المعادن إلى أدوات لطيفة داخل الخلايا
تعتمد العديد من التفاعلات الكيميائية القوية على المعادن، لكن تقريب هذه المعادن إلى خلايا حية غالباً ما يؤدي إلى مشكلات: تلف، إجهاد، وموت الخلايا. تُظهر هذه الدراسة أنه مع "مقبض" جزيئي مناسب حول ذرة النيكل، يصبح من الممكن إجراء تفاعل معقد داخل الخلايا الحية دون إلحاق ضرر بها. يتيح هذا الاكتشاف للعلماء وسم آلاف المواقع المحددة على البروتينات وحتى تتبّع مُمْرِضات يصعب رصدها، ما يفتح طرقاً جديدة لرسم ما يحدث فعلياً داخل الخلايا في الصحة والمرض.
لماذا المعادن صديقة وعدوة في آن
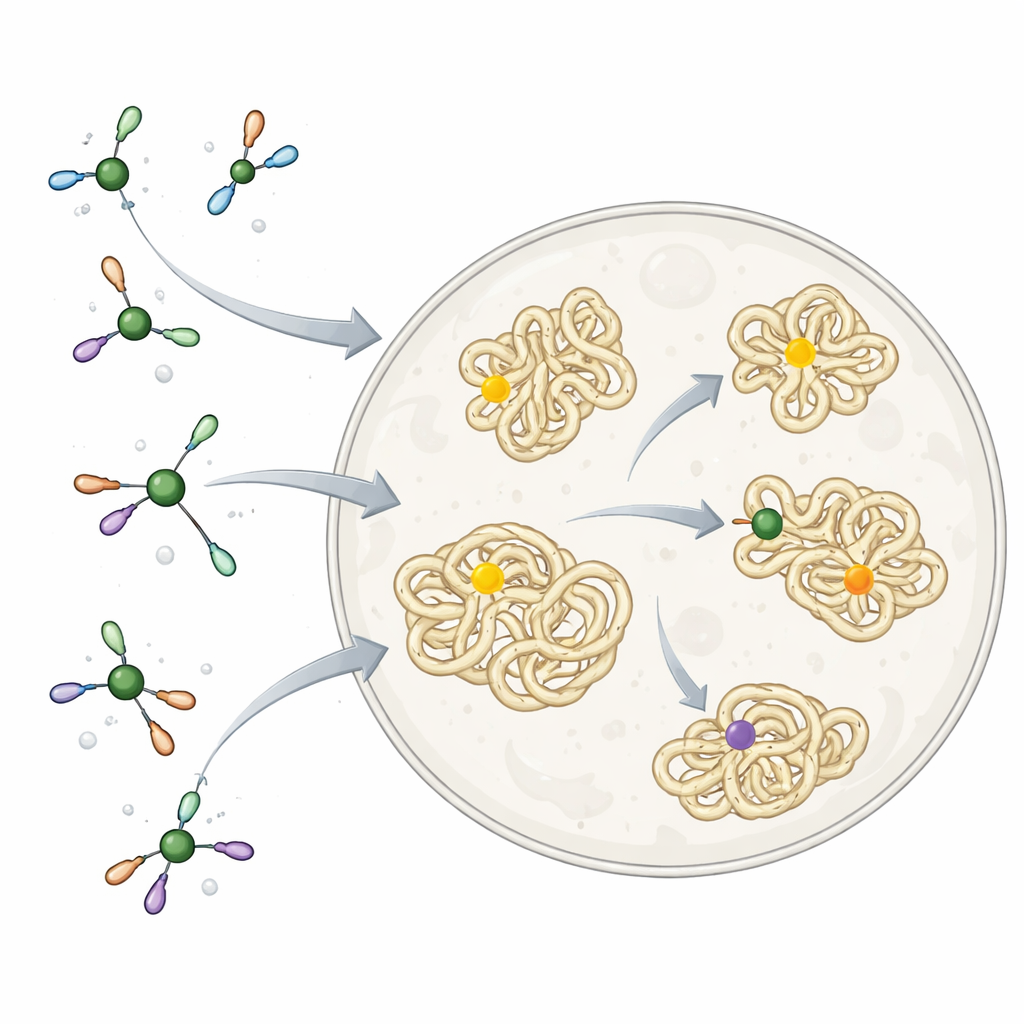
يعمل النيكل ومعادن أخرى بصمت داخل أجسامنا كجزء من إنزيمات طبيعية، لكن يمكن أن تكون سامة إذا ارتبطت في المكان الخطأ. تحل الطبيعة هذه المشكلة بتغليف المعادن بجزيئات صغيرة وبالبروتينات المختارة بعناية، التي توجهها إلى الأهداف الصحيحة وتمنع التفاعلات غير المرغوبة. بالمقابل، يستخدم الكيميائيون غالباً مرافقات معدنية شديدة التفاعلية وغير مُلائمة للأنظمة الحية. كانت هذه أدوات ممتازة لبناء جزيئات معقدة في أنبوبة تفاعل، لكنها قاسية للغاية للاستخدام داخل الخلايا، لا سيما عندما يكون الهدف هو ربط "شارة" صغيرة بحامض أميني معين في بروتين دون إزعاج بقية الخلية.
تصميم معاير نيكل ألطف
استلهم الباحثون من طريقة تعامل الخلايا نفسها مع النيكل. بنوا مجموعة من مجمعات النيكل ملفوفة في لوَاقٍ بسيطة ومتوافقة حيوياً تسمى TMEDA. يعمل هذا الجزيء الصغير مثل مشبك ناعم: محكم بما يكفي لمنع النيكل من الالتصاق بمكونات خلوية خاطئة، لكنه مرن بما يكفي لتمكينه من إجراء تفاعل رئيسي. يربط هذا التفاعل شظية "أريل" — مجموعة مسطحة على شكل حلقة توجد كثيراً في الأدوية — بذرة الكبريت في حمض الأمين السيستين في البروتينات. على بروتينات منقّاة في المحلول، ارتبطت هذه مجمعات النيكل بسرعة وبانتقائية بالشظايا الأريلية لمواقع سيستين مفردة، وعملت عبر أشكال ومواقع بروتينية مختلفة، مما دل على أن الكيمياء متوافقة على نطاق واسع مع جزيئات بيولوجية حقيقية.
تحرير البروتينات داخل الخلايا الحية
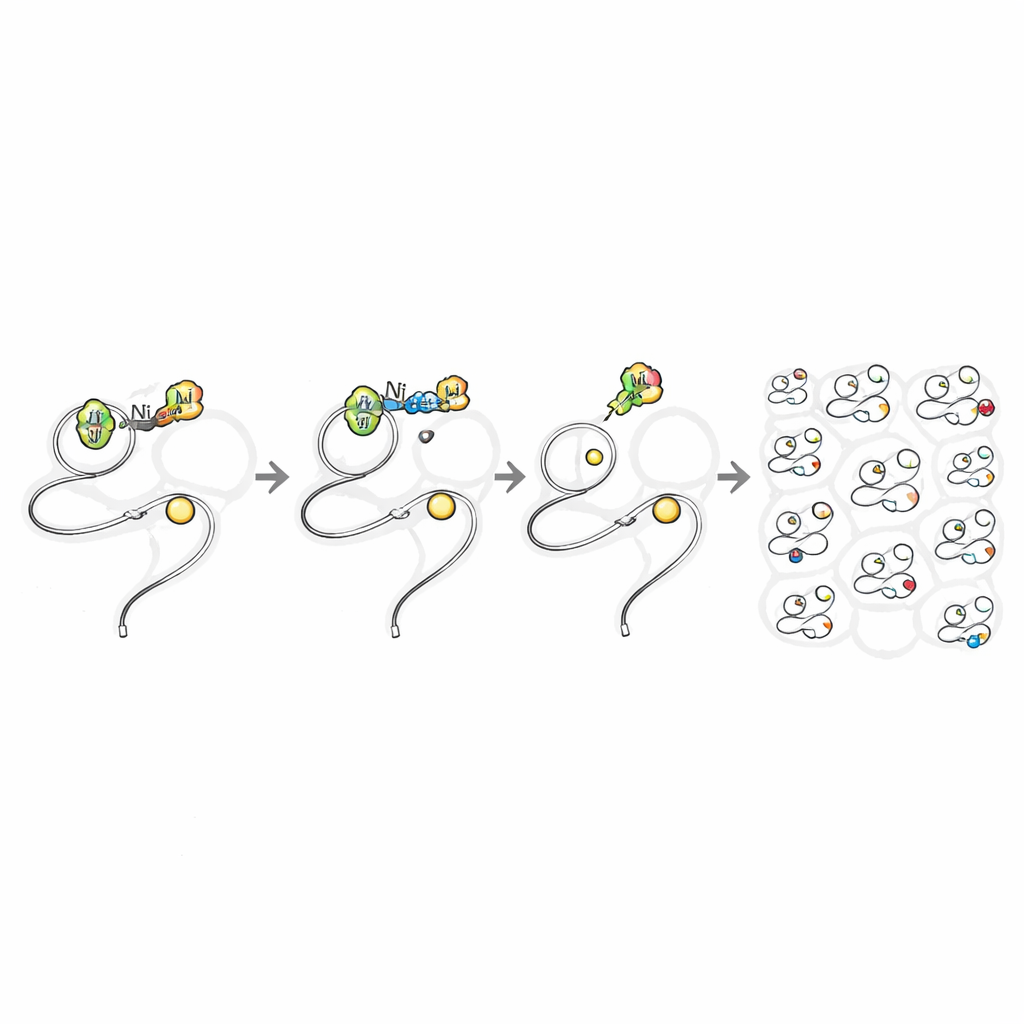
بعد ذلك، تساءل الفريق عما إذا كانت هذه المرافقات نفسها قد تعمل داخل الخلايا الحية دون أن تكون سامة. قارنوا أملاح النيكل البسيطة، المعروفة بأنها ضارة، بمجمعات النيكل المرتبطة بـTMEDA. في خلايا الثدييات، تسببت مصادر النيكل البسيطة في موت خلايا كبير عند جرعات منخفضة نسبياً، بينما بقيت المجمعات المتوازنة بالراوابط محتملة التحمّل حتى عند تراكيز ملي مولارية. سمح هذا هامش الأمان للباحثين بنقع خلايا بكتيرية وثديية في مرافقات النيكل فترة كافية لتدخل وتعدّل البروتينات. من خلال بناء مقبض أزيدي في نسخة واحدة من مجموعة الأريل، تمكنوا بعد التفاعل من وصل أصباغ فلورية أو شارات بيوتين عبر تفاعل "كليك"، كاشفين عن تلوّن واضح ومتدرج بالجرعة للبروتينات في جميع أنحاء السيتوبلازم ونواة الخلايا الحية.
رسم مواقع البروتين التفاعلية عبر البروتيوم
مع توفر تفاعل آمن وسريع داخل الخلايا، حوّل المؤلفون هذا الأسلوب إلى أداة اكتشاف. عالَجوا خلايا بشرية حية بمُركّب النيكل الحامل للأزيد، ثم استخدموا شارة بيوتين قابلة للقطع ضوئياً وقياس طيفي متقدم لرؤية أي السيستينات قد تم تعديلها بالضبط. في تجربة واحدة تم اكتشاف ما يقرب من 11,000 موقع سيستين عبر ما يقرب من 5,000 بروتين — أي نحو ضعف عدد البروتينات مقارنة بجميع دراسات توصيف السيستين في الخلايا الحية السابقة مجتمعة. كان الوسم انتقائياً للغاية للسيستين وأظهر انحيازاً ضئيلاً تجاه أنواع بروتينات أو مواقع أو مواقع نشطة معروفة معينة. ومن اللافت أن العديد من البروتينات المستهدفة كانت تعتبر "غير قابلة للربط" وفق معايير اكتشاف الأدوية الحالية، بما في ذلك بروتينات إشارة منخفضة الوفرة ومفاتيح حساسة بالأكسدة يصعب دراستها بالوراثة فقط.
تتبّع المُمْرِضات المخفيّة في الزمن الحقيقي
أثبتت نفس الكيمياء أيضاً حساسية كافية لالتقاط البروتينات الغريبة المصنوعة أثناء العدوى. في خلايا بشرية تحتوي على تسلسلات فيروسية كامنَة، كشف الأسلوب عوامل نسخ فيروسية موجودة بمستويات ضئيلة للغاية، بما في ذلك أشكال سبلايس متبادلة. ثم أصاب الفريق خلايا بمُمْرِضين مختلفين جداً: البكتيريا داخل الخلوية Chlamydia trachomatis وفيروس سيندبيس، وهو فيروس رنا مرتبط بالشيكونغونيا. من خلال نبض الخلايا المصابة بمُرَكّب النيكل في أزمنة مختلفة، تمكنوا من اصطياد مواقع سيستين على بروتينات ريبوسومية وتنظيمية بكتيرية رئيسية مع انتقال البكتيريا بين مراحل دورة حياتها، وعلى بروتينات فيروسية غير تركيبية حاسمة تدفع تكرار الرنا. تبرز هذه المواقع الموسومة الآن كنقاط ضعف محتملة لاستراتيجيات مضادة للفيروسات أو المضادات البكتيرية في المستقبل.
ما الذي يعنيه هذا لمستقبل الكيمياء الخلوية
من خلال موازنة غلاف الراوابط حول النيكل بعناية، تُظهر هذه الدراسة أن معدنًا كان يُعتبر تقليدياً محفوفاً بالمخاطر يمكنه إجراء تفاعل تعديل بروتيني تساهمي دقيق داخل الخلايا الحية مع أذى ضئيل. هذا يجعل من الممكن رسم خريطة وظيفية مفصلة لمواقع السيستين التفاعلية عبر البروتيوم، بما في ذلك البروتينات النادرة أو العابرة أو التي يصعب استهدافها بالأدوية. كما يوفر وسيلة لتتبّع وفحص المُمْرِضات داخل خلايا العائل على مستوى الأحماض الأمينية المفردة. وعلى نطاق أوسع، توحي الدراسة بأن العديد من الكيميائيات المعدنية "المحرمة" الأخرى قد تُروَّض بطريقة مماثلة، فاتحةً عصراً جديداً تعمل فيه أدوات الكيمياء التخليقية القوية بأمان داخل الأنظمة الحية.
الاستشهاد: Fu, X., Liu, W., Demyanenko, Y. et al. Biocompatible ligand balancing in transition metal coordination enables benign in-cell protein arylation. Nat. Chem. 18, 457–472 (2026). https://doi.org/10.1038/s41557-025-02017-1
الكلمات المفتاحية: توصيف السيستين, اقتران النيكل الحيوي, وسم البروتينات في الخلايا الحية, كيموبروتيوميكس, رسم خرائط بروتيوم الممرض