Clear Sky Science · ar
اليوتبيكوتينيشن عند اللِيسين-11 يحفّز استحثاث الإنترفيرون من النوع I/III عبر مسارات cGAS–STING ومستشعرات Toll-like 3 و4
كيف تطلق خلايانا الإنذار
عندما تغزو الفيروسات أو الجزيئات الضارة الجسم، يتعيّن على خلايانا أن تقرّر خلال دقائق ما إذا كانت ستطلق إشارات إنذارية مضادة للفيروسات تُسمى الإنترفيرونات. هذه الإشارات قد تَنْقِذنا من عدوى شديدة—لكن عند إطلاقها بصورة خاطئة، فإنها تسبب أمراضاً مناعية ذاتية ضارة. تكشف هذه الدراسة عن «لوحة تحويل» جزيئية كانت مخفية سابقاً داخل الخلايا تساعد على تقرير متى يتم تشغيل استجابات الإنترفيرون ومتى تُكبح. فهم هذه اللوحة يوفر دلائل لتحسين اللقاحات والعلاجات المضادة للفيروسات والعلاجات لحالات المرض التي يقودها الإنترفيرون.
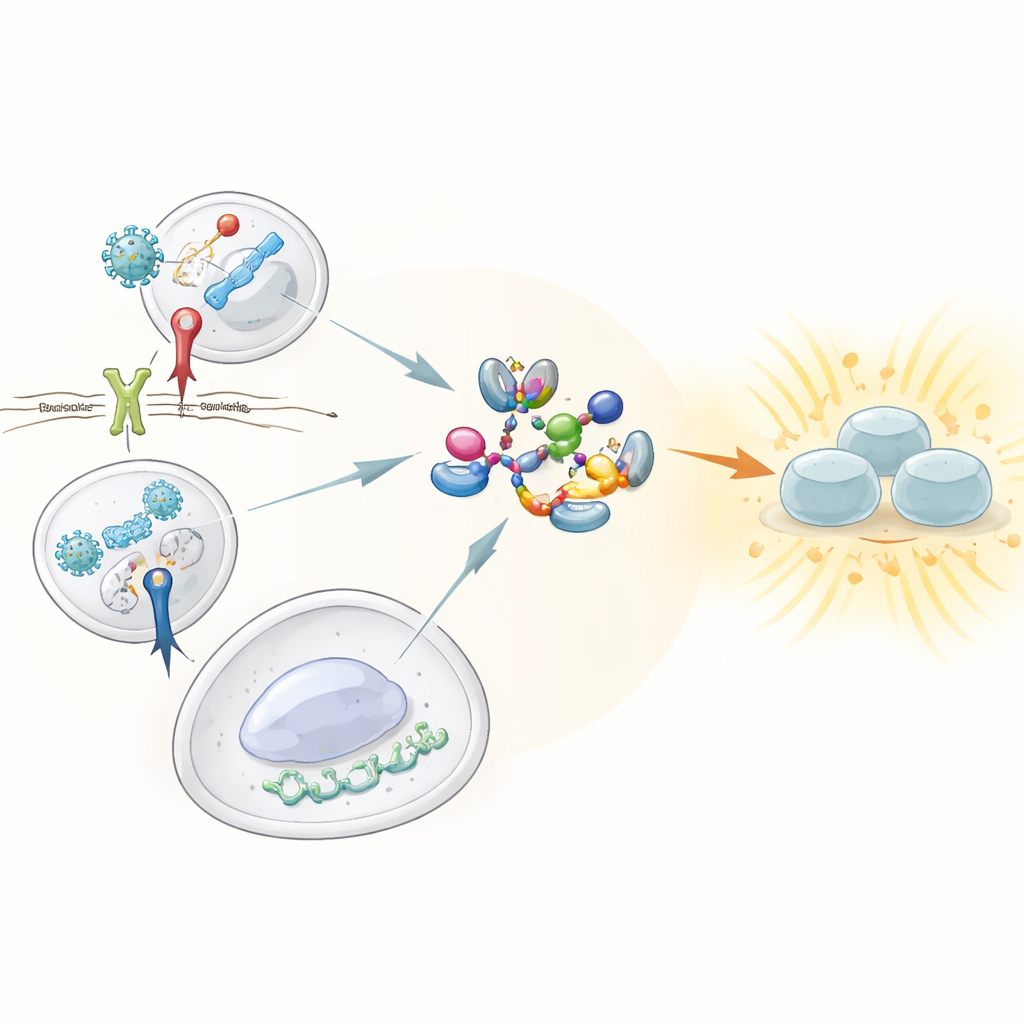
حراس يكتشفون الخطر
تعتمد مناعتنا الفطرية على حراس معروفين بمستقبلات التعرف على الأنماط، التي تجوب بحثاً عن سمات مميزة للفيروسات والبكتيريا. من بينها، تبرز ثلاثٌ لإمكانياتها على تحفيز استجابات إنترفيرونية قوية: مستقبل Toll-like 3 (TLR3) الذي يكتشف الحمض النووي الريبي مزدوج السلسلة للفيروسات؛ ومَستَقبِل Toll-like 4 (TLR4) الذي يستشعر مكوّناً في جدران الخلايا البكتيرية؛ ومسار cGAS–STING الذي يكشف عن الحمض النووي المتواجد في أماكن خاطئة داخل الخلايا. يجب على الثلاثة أن ينشّطوا إنزيمًا مركزياً يُدعى TBK1، الذي بدوره يفعل العامل النسخي IRF3 لقيادة إنتاج الإنترفيرونات من النوعين I وIII. وحتى الآن، لم يكن مفهوماً كيف تتلاقى هذه المستشعرات على TBK1 لتحويله إلى حالته النشطة.
موصِل جزيئي خفي
اكتشف الباحثون أن بروتيناً يسمى ANKIB1 يعمل كوصِل حاسم بين هذه المستشعرات وTBK1. ANKIB1 هو إنزيم يلحق وسومًا جزيئية صغيرة تُعرف بسلاسل اليوبيكويتين إلى بروتينات أخرى. والأهم أنه يبني نوعاً معيناً من السلاسل مبني على رابطة تُدعى «K11»، والتي كانت معروفة سابقاً بدورٍ أكبر في انقسام الخلايا منها في المناعة. في خلايا بشرية تفتقر إلى ANKIB1، لم يؤدِ تنشيط TLR3 أو تفعيل STING إلى تفعيلٍ سليم لكل من TBK1 وIRF3، ولم تُشغّل جينات الإنترفيرون إلا بالكاد. إعادة ANKIB1 أعادت الاستجابة، مما يظهر أن هذا الإنزيم الواحد ضروري وكافٍ لتحريك هذا الفرع من الإنذار المضاد للفيروسات.
بناء منصة ارتكاز لبروتينات النقل
كشفت فحوص أدق كيف يمارس ANKIB1 تأثيره. عندما يشعر TLR3 أو STING بالخطر، يجمعان منصات متعددة البروتينات تُسمى سِغمَونات الإشارة (signalosomes). يُستدعى ANKIB1 إلى هذه المنصات عبر منطقة تتعرف على اليوبيكويتين. وبمجرد وجوده هناك، يزوّق عدة مكونات رئيسية—بما في ذلك بروتينات الموصّل TRIF وSTING ذاتها، فضلاً عن جزيئات إشارية أخرى—بِسلاسل يوبيكويتين مرتبطة عبر K11. هذه السلاسل لا تعلّم البروتينات بالضرورة للتدمير؛ بل تعمل كأنها فيلكرو جزيئي. بروتين آخر، أوبتينورين (OPTN)، يُجذب خصوصاً إلى هذه المواقع المعدلة. وبصفته موصِلاً ناقلاً، يجلب OPTN بعد ذلك TBK1 إلى المجمع حتى يمكن تنشيطه وتمرير الإشارة إلى IRF3 وجينات الإنترفيرون. عندما أُزيح OPTN، انهار تنشيط TBK1، ما يؤكد أن وسم K11 بواسطة ANKIB1 وربط OPTN يشكلان محوراً واحداً وضرورياً.
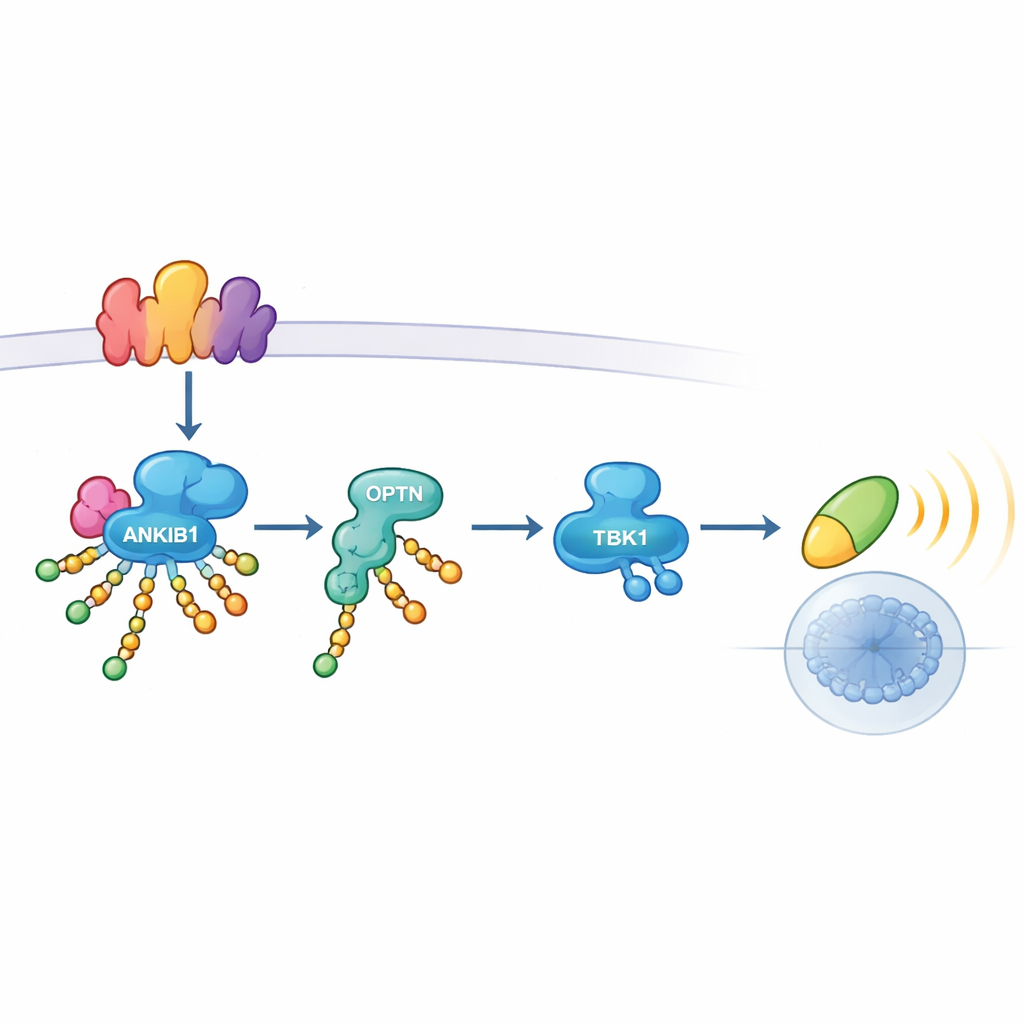
متى يكون هذا المسار مهماً—ومتى لا يكون
سأل الفريق بعد ذلك ما إذا كانت هذه الآلية عامة عبر جميع مستشعرات مكافحة الفيروسات. وجدوا أن ANKIB1 حيوي لاستحثاث الإنترفيرون عبر TLR3، والذراع المعتمدة على TRIF من TLR4، ومسار cGAS–STING، وكلها تستخدم OPTN كالموزع الرئيسي إلى TBK1. بالمقابل، مستشعر آخر، RIG-I، الذي يلتقط الحمض النووي الريبي الفيروسي، يعتمد على مجموعة مختلفة من بروتينات الموصِل ولا يحتاج إلى ANKIB1 أو OPTN لتنشيط TBK1. توافقت التجارب في الفئران مع هذه النتائج الخلوية. الحيوانات التي تفتقر إلى Ankib1 أنتجت كمية أقل بكثير من الإنترفيرون بعد تفعيل TLR3 أو STING، وكانت محمية من متلازمة التهابية مميتة يقودها الإنترفيرون، لكنها أصبحت أكثر عرضة للعدوى بفيروس الهِربِس البسيط 1، وهو فيروس DNA يعتمد بشدة على إنترفيرون مُحفَّز عبر cGAS–STING للسيطرة عليه. بقيت الاستجابات لفيروس الإنفلونزا، الذي يُكشف عنه بشكل رئيسي عبر RIG-I، سليمة إلى حد كبير.
موازنة الحماية والضرر
تظهر هذه النتائج معاً أن سلاسل اليوبيكويتين المرتبطة بـK11 التي يُولّدها ANKIB1 هي عملة مركزية في فرعٍ كبير من إشارة المقاومة الفطرية للفيروسات. من خلال خلق مواقع ارتكاز لـOPTN، يساعد ANKIB1 في تجميع ناقل جزيئي دقيق يحول الخطر الذي تكتشفه TLR3 وTLR4 (عبر TRIF) وcGAS–STING إلى إنتاج قوي للإنترفيرون. هذا المحور ذو حدين: فهو ضروري للدفاع ضد بعض الفيروسات، لكنه أيضاً يغذي أمراضاً التهابية يقودها الإنترفيرون عند الإفراط في تنشيطه. ونظراً لأن الفعالية التحفيزية لدى ANKIB1 والمجالات الخاصة به مطلوبة لهذه الوظيفة، فإنها تمثل أهدافاً واعدة لأدوية مستقبلية تهدف إما إلى تخفيف استجابات الإنترفيرون الضارة في الحالات المناعية الذاتية أو لتعزيز المناعة المضادة للفيروسات حيث تكون ضعيفة.
الاستشهاد: Betrancourt, A., Cinko, M.T., Varanda, A.B. et al. Lysine-11 ubiquitination drives type-I/III interferon induction by cGAS–STING and Toll-like receptors 3 and 4. Nat Cell Biol 28, 608–621 (2026). https://doi.org/10.1038/s41556-026-01886-z
الكلمات المفتاحية: المناعة الفطرية, إشارة الإنترفيرون, اليوتبيكوتينيشن, مسار cGAS–STING, العدوى الفيروسية