Clear Sky Science · ar
النسيج الدهني المحيط بالأورام يدفع للاختفاء المناعي في سرطان القولون والمستقيم عبر التحول الدهني–الميزنكيمي
لماذا تهم دهون البطن المحيطة بالأورام
ينمو سرطان القولون والمستقيم داخل جدار الأمعاء، لكنه يجلس بجوار وسادة سميكة من دهون البطن. يظن معظم الناس أن هذه الدهون تعمل كحشو سلبي. تكشف هذه الدراسة عن أمر مفاجئ: الدهون الملفوفة حول الورم يمكنها بهدوء أن تسرق خلايا المناعة المقاتلة للسرطان بعيدًا عن الورم، مما يساعد السرطان على الاختفاء من الجهاز المناعي. إن فهم هذا الصراع الخفي يوفر طرقًا جديدة للتنبؤ بمن سيستجيب للعلاج المناعي وكيفية جعل هذه العلاجات أكثر فعالية.
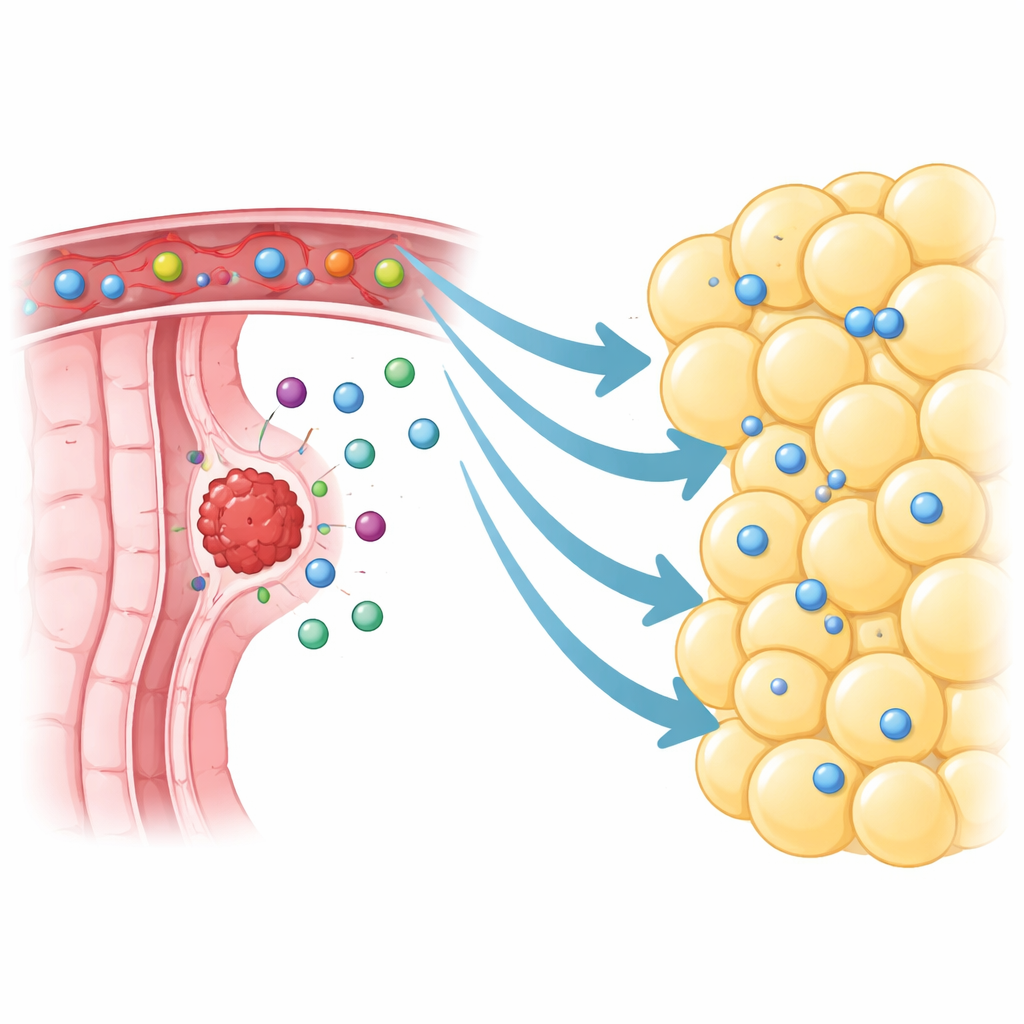
حَيّ مناعي نشط بجوار الورم
ركز الباحثون على الدهون الحشوية المحيطة مباشرة بالأورام القولونية المستقيمة، المسماة النسيج الدهني الحشوي المحيط بالورم. باستخدام تسلسل الرنا المفرد الخلوي، خريطة أكثر من 370,000 خلية فردية من الأورام والدهون المجاورة والدهون البعيدة والنسيج الطبيعي. بدلاً من أن تكون صامتة وخاملة، كانت الدهون المجاورة للأورام تعج بالخلايا المناعية، خاصة الخلايا التائية والخلايا البائية. ووجدوا حتى تجمعات منظمة تشبه العقد اللمفاوية الصغيرة، وهي دلائل على أن هذا النسيج قادر على استضافة ردود مناعية نشطة. بالمقارنة مع الدهون المأخوذة من مواقع أبعد، احتوت الدهون المحيطة بالورم على عدد أكبر بكثير من الخلايا اللمفاوية، بما في ذلك خلايا الذاكرة والخلايا التائية القاتلة المحددة للورم التي من المفترض أن تقوم بدوريات ضد السرطان.
عندما تنتهي الخلايا المناعية المفيدة في المكان الخاطئ
لمعرفة ما إذا كانت هذه الدهون الغنية بالمناعة تساعد أو تضر، استخدم الفريق نماذج فأرية حيث زُرعت الأورام بالقرب من وسادة دهنية تشبه الحالة البشرية. ثم أزالوا هذه الدهون المجاورة جراحيًا أو ذابوها كيميائيًا. بشكل معاكس للحدس، أدى نزع النسيج الدهني المحيط إلى إبطاء نمو الورم. احتوت أورام الفئران التي فقدت هذه الدهون على عدد أكبر من خلايا CD4 وCD8 التائية، بما في ذلك الخلايا التائية التي تتعرف على مستضدات الورم. أظهرت تجارب إضافية تتبع خلايا مناعية مانحة أنه عندما كانت الدهون موجودة، تراكمت العديد من هذه الخلايا في الوسادة الدهنية بدلًا من الورم. أعاد إزالة الدهون توجيه هذه الخلايا إلى الورم، معززة الاستجابة المضادة للسرطان. بكلمات أخرى، عملت الدهون كمخزون تنافسي يمتص الخلايا المناعية ويمنعها من الوصول إلى هدفها الحقيقي.
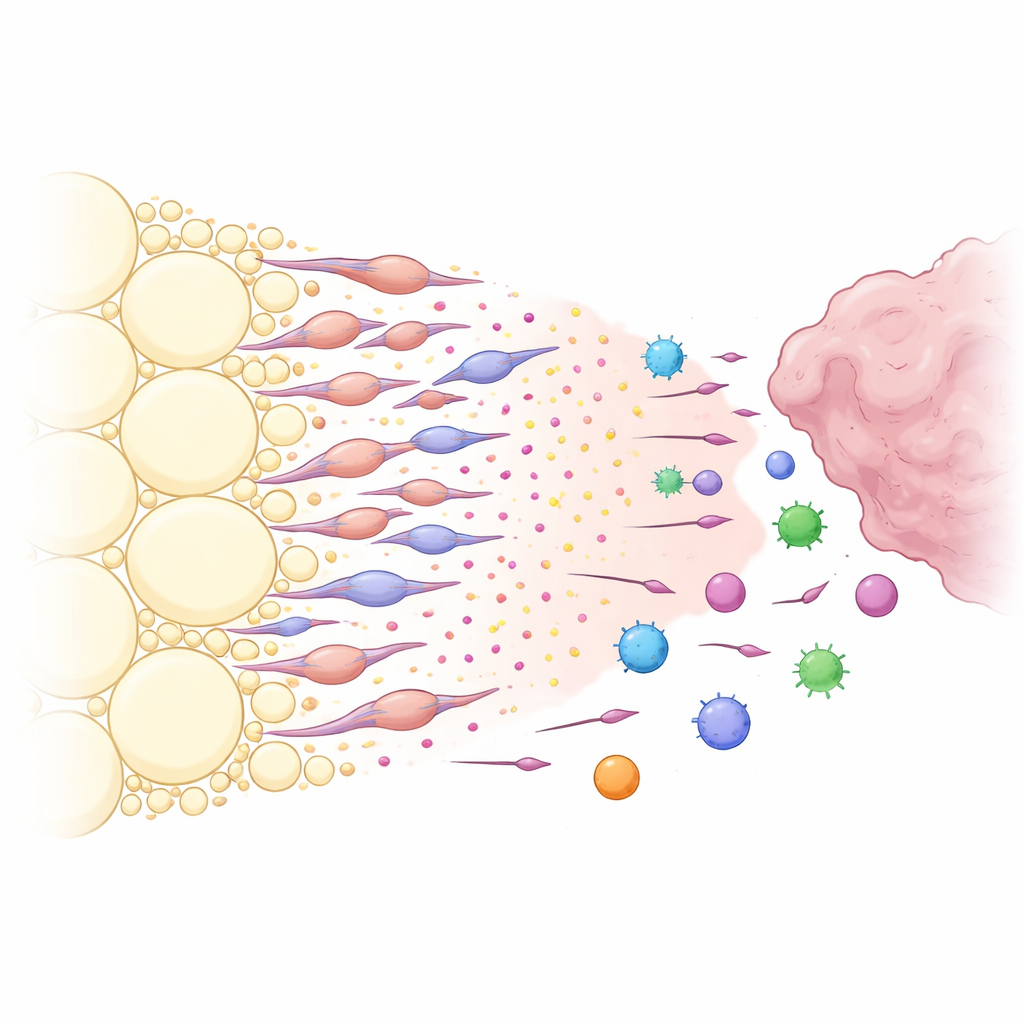
طُعم كيميائي تبنيه خلايا دهنية متحولة
ما الذي جعل النسيج الدهني المحيط بالورم جيدًا جدًا في أسر الخلايا المناعية؟ من خلال تحليل إشارات الاتصال بين أنواع الخلايا، حدد الباحثون مسارًا كيميائيًا قويًا يتمحور حول جزيء CXCL12 ومستقبله CXCR4. أفرزت الخلايا الستروماسية في الدهون القريبة من الورم مستويات عالية من CXCL12، بينما عبّرت العديد من الخلايا المناعية عن CXCR4، مما جعلها حساسة لهذه الإشارة. أدى حجب CXCL12 موضعيًا في الدهون، أو حذفه وراثيًا في ستروما الدهون، إلى تقلص الأورام والسماح لعدد أكبر من الخلايا المناعية الإيجابية لـ CXCR4 بدخول الورم بدلًا من أن يتم تحويلها. ثم اكتشف الفريق أن المنتجين الرئيسيين لـ CXCL12 لم يكونوا خلايا دهنية عادية، بل مجموعة خاصة من الخلايا الشبيهة بالليفية المنشأ من الدهون أطلقوا عليها اسم الخلايا الليفية المرتبطة بالسرطان المشتقة من النسيج الدهني. دفعت عوامل مطلقة من الورم، وخاصة عامل النمو TGF-β1، خلايا الستروما الدهنية المحلية للتحول إلى هذه الخلايا الشبيهة بالليفية، والتي بدورها أفرزت كميات كبيرة من CXCL12 وإشارات أخرى محفزة للنمو.
تحويل درع إلى نقطة ضعف
لأن هذه الخلايا المتحولة تساعد في تحويل الخلايا المناعية بعيدًا عن الأورام، اختبر الباحثون ما إذا كان تفكيك هذا «المصرف المناعي» يمكن أن يحسن العلاج المناعي. في فئران مهندسة بحيث يمكن استئصال الخلايا الليفية المرتبطة بالسرطان المشتقة من النسيج الدهني انتقائيًا، أصبح العلاج بمضاد يحجب PD-1 أكثر فعالية بكثير: نمى الورم أقل، ودخلت المزيد من الخلايا التائية المحددة للورم والإيجابية لـ CXCR4 إلى الورم. بالمثل، عملت الأدوية أو الأجسام المضادة التي حجبت إما CXCL12 أو مستقبلها CXCR4 بتآزر مع حجب PD-1 في كل من نماذج سرطان القولون والمستقيم تحت الجلد وفي النماذج المتوضعة في موضعها الأصلي. لم تقلل هذه التركيبات حجم الورم فحسب، بل أعادت أيضًا تشكيل المشهد المناعي داخل الورم.
دلائل من صور المرضى وما التالي
سأل الفريق بعد ذلك ما إذا كانت نتائجهم ذات أهمية لدى المرضى الحقيقيين. في مجموعة من الأشخاص المصابين بسرطان القولون والمستقيم متقدم موضعيًا ويتلقون علاجًا مدمجًا من الكيمياء الإشعاعية والعلاج المناعي المناعي عبر PD-1، كان أولئك الذين أظهروا استجابة كاملة يميلون إلى أن يكون لديهم حجم أصغر من الدهون الحشوية المحيطة بالورم في تصوير الرنين المغناطيسي قبل العلاج. وكمّيًا، تنبأت مساحة هذه الدهون باستجابة العلاج بشكل أفضل من بعض العلامات النسيجية المعيارية، وكان لدى المرضى ذوي أحجام الدهون المحيطية الكبيرة معدلات استجابة أقل بكثير. للمتخصص غير المتخصص، الاستنتاج لافت: ليس الورم فقط، بل أيضًا الدهون المحيطة به مباشرة يمكن أن تحدد مدى فعالية العلاج المناعي. عبر التركيز على هذه الدهون — سواء بقياسها لتوجيه قرارات العلاج أو استهداف خلايا الستروما المتحولة فيها وإشارة CXCL12–CXCR4 — قد يكون من الممكن تحويل درع وقائي للورم إلى نقطة ضعف علاجية.
الاستشهاد: Wang, JH., Zheng, YQ., Qian, ZY. et al. Peritumoural adipose tissue drives immune evasion in colorectal cancer via adipose–mesenchymal transformation. Nat Cell Biol 28, 581–595 (2026). https://doi.org/10.1038/s41556-026-01885-0
الكلمات المفتاحية: سرطان القولون والمستقيم, المحيط المصلي للورم, الدهون الحشوية, المناعة المناعية, CXCL12 CXCR4