Clear Sky Science · ar
إعادة تشكيل الشبكة الإندوبلازمية سمة من سمات الشيخوخة وتعتمد على ER-phagy
لماذا تهم طيات الخلايا الداخلية مع تقدمنا في العمر
تمتلئ خلايا أجسامنا بشبكة غشائية متشابكة تُدعى الشبكة الإندوبلازمية (ER). تساعد هذه البنية في بناء الدهون والبروتينات، وتدير السكر والكالسيوم، وتتواصل باستمرار مع أجزاء خلوية أخرى. ونظرًا لأن العديد من الوظائف الحيوية تمر عبر هذا الشبكة، فإن أي إعادة تشكيل طويلة الأمد للـER قد تؤثر على كيفية شيخوخة أنسجتنا، ومدى تحملها للضغط، وفي النهاية على مدة بقائنا بصحة جيدة. تطرح هذه الدراسة سؤالًا يبدو بسيطًا: هل تتقدّم الشبكة الإندوبلازمية نفسها في العمر بطريقة محددة ومنظمة، وإذا كان الأمر كذلك، فهل هذا التغيير تلف ضار أم استراتيجية وقائية مدمجة؟
تحول خفي في ورشة عمل الخلية
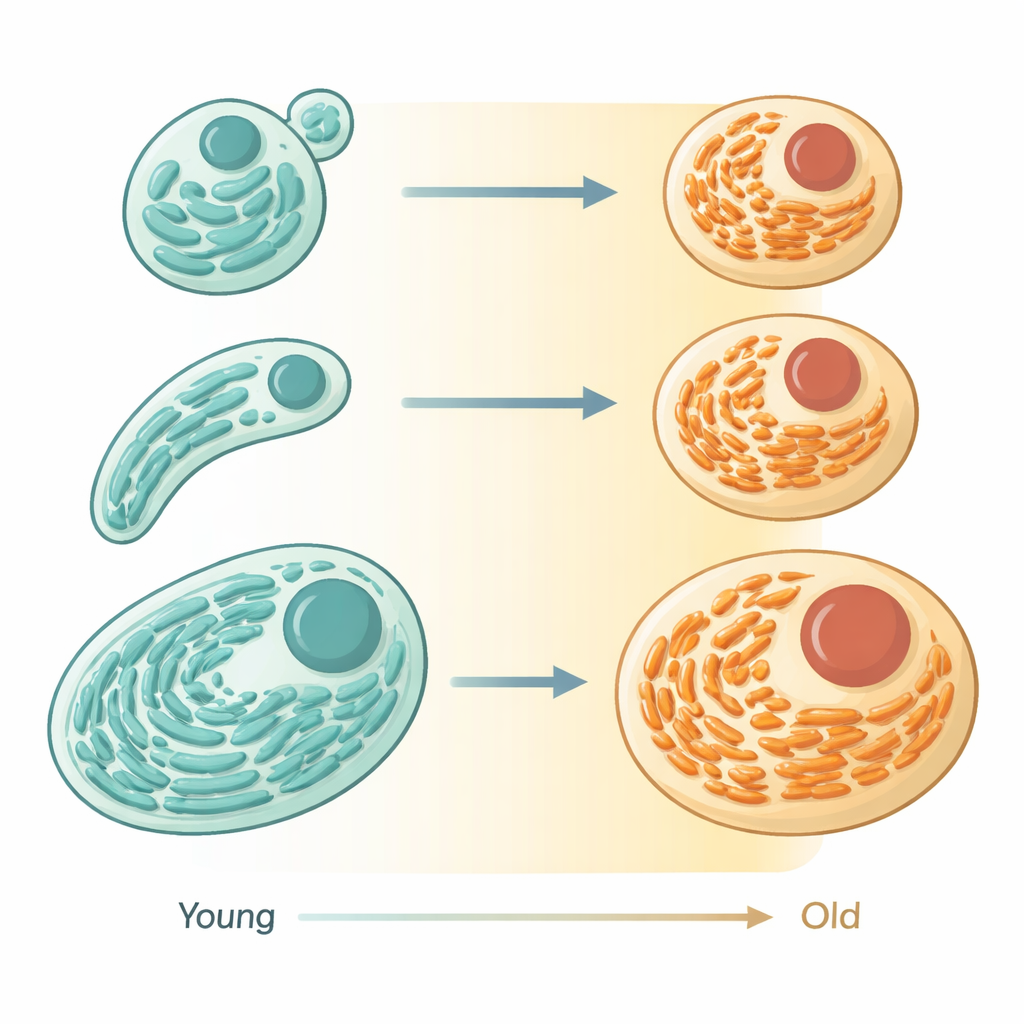
باستخدام مجاهر متقدمة ووسوم فلورية في الدودة الصغيرة Caenorhabditis elegans، تتبّع الباحثون الـER داخل حيوانات حية أثناء انتقالها من شباب البلوغ إلى الشيخوخة. في الخلايا الشابة، يشكل الـER صفائح عريضة متراصة مزدانة بآليات تصنيع البروتين، تشبه أرضيات مصانع مرتبة بعناية. مع تقدّم الديدان في العمر، تتقلص تلك الصفائح في الحجم وتفسح المجال لشبكة أرفع وأكثر أنبوبية تشغل مساحة أقل. أظهرت القياسات أن محتوى الـER الكلي ينخفض بشكل ملحوظ بينما يتغير الشكل، مما يشير إلى أنه ليس مجرد تلف عشوائي بل انكماش وإعادة تكوين منسق للعضية.
من صنع البروتينات إلى إدارة الدهون
غالبًا ما يشير الشكل في علم الأحياء إلى الوظيفة، وهذا ما تحقق هنا أيضًا. قارن الباحثون كيف تتغير البروتينات المتعلقة بالـER مع مرور الوقت عبر أنسجة الدودة. تراجعت البروتينات المشاركة في بناء وطي وفحص البروتينات الأخرى مع العمر، بالتوازي مع فقدان الـER ذي الصفائح. بالمقابل، بقيت العديد من بروتينات الـER المرتبطة باستقلاب الدهون والغشاء ثابتة أو ازدادت. توحي هذه الأنماط بأن الخلايا المسنة تقلل من الإنتاج الكتلي للبروتينات وتعيد توجيه موارد الـER نحو إدارة الدهون والأغشية. ولافت للنظر أنه عند فحص مجموعات بيانات كبيرة من فئران مسنة، رَصَد الباحثون قصة مماثلة: تميل بروتينات الـER المشاركة في الإفراز ومعالجة البروتينات إلى الانخفاض، بينما ظلت تلك المرتبطة باستقلاب الدهون والبلعمة الذاتية محفوظة نسبيًا أو زادت.
مسار إعادة التدوير الخلوي وراء إعادة التشكيل
ما الذي يقود هذا التشكيل على نطاق واسع؟ تتبعت المجموعة التغيرات إلى ER-phagy، شكل من أشكال الأكل الذاتي الانتقائي حيث تغلف الخلية أجزاء من الـER في حويصلات إعادة التدوير لتحللها في الليسوسومات. منعت تعطيل جينات البلعة الذاتية الأساسية في الديدان الفقدان الطبيعي المرتبط بالعمر في كتلة الـER والتحول من صفائح إلى أنابيب، مما يُظهر أن هذا المسار لا يكتفي بتنظيف البقايا بل يشكل العضية بنشاط. أكدت تجارب مستقلة في الخميرة أن مكونات الـER تُعاد توجيهها إلى مركز إعادة التدوير الخلوي مع تقدم الخلايا في العمر، مرة أخرى بطريقة معتمدة على البلعة الذاتية. كشفت الميكروسكوبي الإلكتروني عن شظايا من الـER داخل حاويات تحلُّليَّة، ما يقدّم دليلًا مادّيًا على أن أجزاء من الشبكة تُزال عمدًا.

التحكم الخاص بالأنسجة في برنامج شيخوخة مشترك
على الرغم من أن إعادة تشكيل الـER لوحظت في العديد من أنسجة الدودة — الأمعاء، والطبقة الشبيهة بالجلد (hypodermis)، والعضلات، والخلايا العصبية — تبين أن المحفزات كانت خاصة بالأنسجة. في الطبقة الشبيهة بالجلد، ربط بروتين غشائي كان قليل المعرفة سابقًا يُسمى TMEM-131 دوران الـER بمعالجة الكولاجين. عندما قلَّ TMEM-131، تم منع الفقدان المرتبط بالعمر للـER في هذه النسيج إلى حد كبير، مما يوحي بأن الـER يُصغر عندما تقل "عملائه" من الكولاجين. في الأمعاء، على النقيض، كان المنظم الرئيسي هو محور IRE-1–XBP-1 من استجابة البروتين المفرد (UPR)، وهو مسار محوري لاستشعار الضغط. أدى تعطيل هذا الفرع الإشاري إلى الحفاظ على الـER المعوي أثناء الشيخوخة، مما يشير إلى أن إشارة إجهاد الـER في هذا العضو تساعد على تحديد متى ينبغي التضحية بأجزاء من الـER.
إعادة توصيل الـER من أجل عمر أطول
تربط الدراسة أيضًا إعادة تشكيل الـER بالطول الافتراضي للحياة. في الديدان، حفزت عدة تدخلات معروفة بتمديد العمر — كَتباطؤ إشارات شبيهة بالإنسولين، وخفض تحسس المغذيات عبر mTOR، وإزالة الخط الجرثومي، أو تبطيء تركيب البروتين بشكل طفيف — تقليص الـER وزيادة الشبكات الأنبوبية في وقت مبكر من البلوغ بدلًا من الانتظار حتى الشيخوخة. والأهم من ذلك أن تعطيل ER-phagy حدَّ بشكل حاد أو ألغى طول العمر الطويل الذي تنتجه مثبطات mTOR في كل من الخميرة والديدان. هذا يشير إلى أن تقليم الـER المدار بعناية ليس مجرد أثر جانبي للشيخوخة أو العلاج، بل هو أحد الآليات التي تحقق بها الخلايا حالة أكثر متانة.
ما الذي يعنيه هذا للشيخوخة الصحية
قد يبدو لفرد غير مختص أن فقدان جزء كبير من بنية خلوية رئيسية أثناء الشيخوخة أمرًا ضارًا بحتًا. يرسم هذا العمل صورة أكثر تمايزًا. يبدو أن الـER يُعاد تشكيله بنشاط — عبر أكل ذاتي انتقائي ومنظمات خاصة بالأنسجة — بحيث تنتج الخلايا المسنة بروتينات جديدة أقل، وتستثمر أكثر في إدارة الدهون والأغشية، وقد تقلل من خطر الإجهاد المزمن. يبدو أن هذا التشكيل محفوظ عبر الكائنات من الخميرة إلى الثدييات، وهو مطلوب على الأقل لبعض أشكال تمديد العمر. ومع ذلك، على المدى الطويل قد يحمل تقلص الـER تبعات ومقايضات، تؤثر على مدى قدرة الخلايا على إصلاح عضيات أخرى وإدارة الانخفاض المتأخر في الأداء. من خلال الكشف عن ER-phagy وديناميكيات الـER كسمات أساسية للشيخوخة الطبيعية والمؤجلة، تبرز هذه الدراسة مجموعة جديدة من الروافع التي قد يُمكن ضبطها في المستقبل لتعزيز أنسجة أكثر صحة ومقاومة.
الاستشهاد: Donahue, E.K.F., Hepowit, N.L., Ruark, E.M. et al. ER remodelling is a feature of ageing and depends on ER-phagy. Nat Cell Biol 28, 449–464 (2026). https://doi.org/10.1038/s41556-025-01860-1
الكلمات المفتاحية: الشبكة الإندوبلازمية, البلعمة الذاتية, الشيخوخة الخلوية, توازن البروتينات, استقلاب الدهون