Clear Sky Science · ar
علم الجينوم الوظيفي الموقوت باستخدام التعلم العميق يكشف السيطرة الهرمية الشاملة على البلعمة الذاتية
كيف تعيد الخلايا تدوير نفسها — وكيف تعرف متى تتوقف
تبقى خلايانا على قيد الحياة في أوقات القحط من خلال إعادة تدوير مكوناتها عبر عملية تُسمى البلعمة الذاتية — حرفياً «أكل الذات». القليل جدًا من إعادة التدوير يؤدي إلى تراكم المكونات التالفة؛ والكثير يؤدي إلى التهام الخلية لنفسها. تسأل هذه الدراسة سؤالاً يبدو بسيطًا لكنه ذو عواقب كبيرة على الشيخوخة والمرض: كيف تُشغِّل الخلية الحية البلعمة الذاتية وتطفئها في اللحظات المناسبة مع تذبذب مستوى المغذيات؟
مراقبة آلاف الخلايا خلال دورة من الشبع إلى المجاعة
لمعالجة هذا السؤال، استخدم الباحثون خميرة الخبز كنموذج ورصدوا ما يقرب من ستة آلاف سلالة طفيلية مختلفة أثناء تعرضها للحرمان ثم الانتعاش. حملت كل سلالة علامات فلورية تميّز البنى المشاركة في البلعمة الذاتية، ما أتاح لمجهر عالي القدرة التقاط صور كل ساعة أثناء إزالة المغذيات ثم إعادتها. بدلًا من تصنيف هذه الصور يدويًا، درّب الفريق خوارزميات تعلم عميق للتعرّف متى تكون الخلية في حالة بلعمة ذاتية، اعتمادًا كليًا على خصائص الصورة بدلاً من حكم الإنسان. أنتج ذلك منحنيات زمنية دقيقة لنشاط البلعمة الذاتية لمعظم جينات الخميرة، كاشفًا مدى سرعة وشدة استجابة كل طفرة لتغيرات المغذيات. 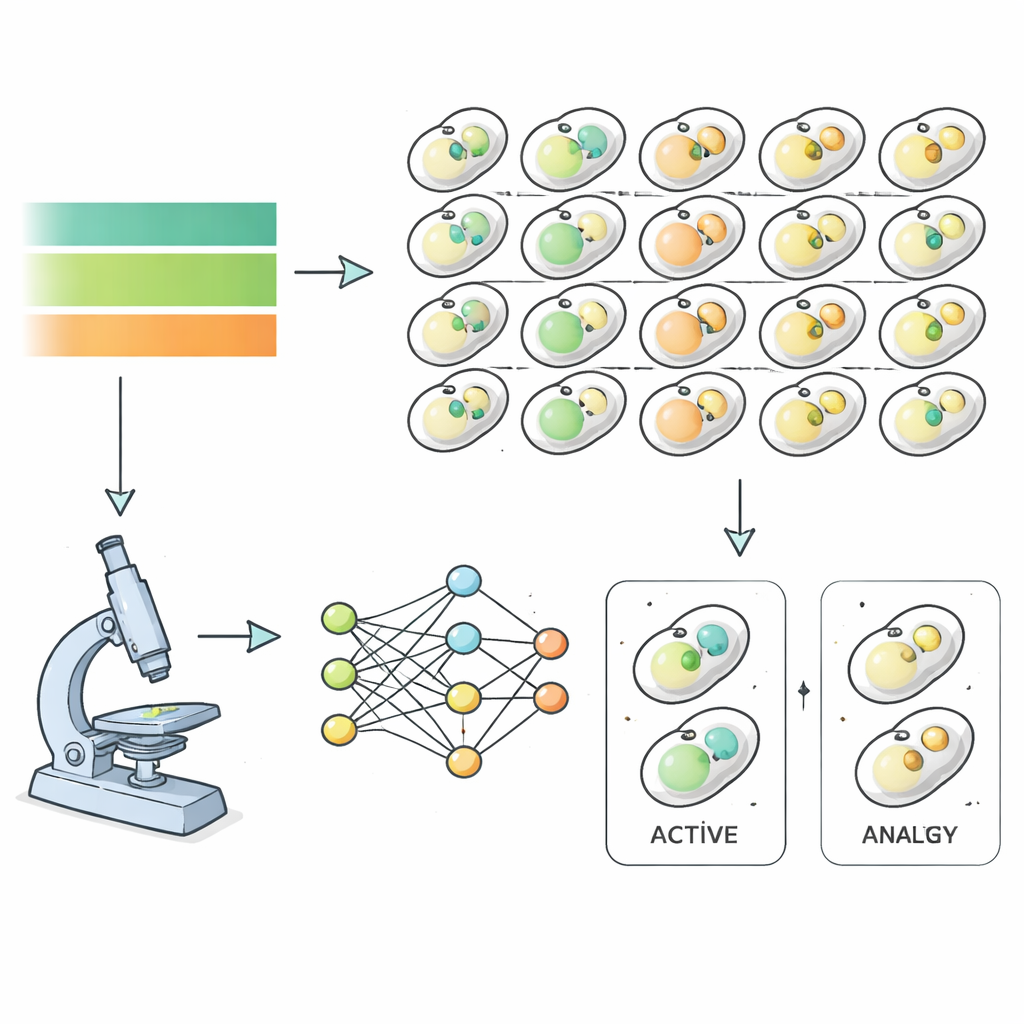
ست طرق مميزة تسيء الخلايا فيها التعامل مع إعادة التدوير
من خلال ملاءمة هذه المنحنيات رياضيًا، استخلص المؤلفون «بصمات حركية» مفصَّلة لكل طفرة — مدى سرعة تشغيل البلعمة الذاتية، وكم استمر ارتفاعها، ومدى حدة إيقافها. كشف تجميع هذه التواقيع عن ستة أنواع سلوكية واسعة. كانت بعض الطفرات «فائقة الحساسية»، تستجيب بسرعة كبيرة للجوع وعودة المغذيات. وأخرى كانت «نقص الحساسية»، تتفاعل ببطء. أظهر مجموعة «مفرطة النشاط» مستوى عالٍ شاذًا من إعادة التدوير القاعدي، في حين فشلت مجموعات أخرى بدرجات متفاوتة في إطلاق استجابة مناسبة على الإطلاق. ومن المهم أن الجينات الأساسية المعروفة للبلعمة الذاتية وُجدت ضمن الفئات الأكثر شدة، مما يثبت أن الطريقة تلتقط بيولوجيا حقيقية بدلًا من ضوضاء القياس.
رسم خريطة هرمية للسيطرة على البلعمة الذاتية
البلعمة الذاتية لا تحدث بمعزل؛ بل هي مدمجة في شبكات التنظيم الأوسع للخلية. وضع الفريق ملفاتهم الديناميكية على خرائط كبيرة للتفاعلات الجينية والبروتينية في الخميرة. تميل الجينات التي تسبب فقدانها عيوبًا قوية في البلعمة الذاتية لأن تكون قريبة من «الآليات الأساسية» المعروفة للبلعمة الذاتية في هذه الشبكات، بينما كانت الطفرات الأدق أبعد، متسقة مع سيطرة أكثر غير مباشرة. ومن خلال فحص العمليات الخلوية التي تتراكم في كل فئة سلوكية، وجدوا أن تنشيط البلعمة الذاتية المحفز بالجوع يتشكل بقوة عبر المسارات المسؤولة عن الحمض النووي الريبوزي، وإنتاج البروتين، واستقلاب الطاقة، في حين يعتمد إيقاف البلعمة الذاتية بعد عودة المغذيات أكثر على حركة الغشاء وخطوات الاندماج التي تنظف الحويصلات المخصصة لإعادة التدوير.
تكبير كيفية تكوّن الحويصلات وتنقيتها
تتقدم البلعمة الذاتية عبر مرحلتين رئيسيتين: بناء حويصلات محملة بالحِمل ثم دمجها مع أجزاء الخلية المخصصة للتفكيك. لتفكيك هاتين المرحلتين، استخرج الباحثون «المساحة الكامنة» داخل شبكتهم العصبية — التمثيل المضغوط الذي تستخدمه لتمييز الصور. عبر إسقاط هذا التمثيل الداخلي على خريطة ثنائية الأبعاد، أمكنهم رؤية تحرك تجمعات الخلايا من منطقة بلا حويصلات، مرورًا بمنطقة تحوي العديد من الحويصلات الحرة، وأخيرًا إلى منطقة تم تنظيف الحويصلات فيها. باستخدام مقارنات إحصائية مقابل طفرات مرجعية محبوسة في مراحل مختلفة، قضوا على كل جين ما إذا كان يؤثر بشكل رئيسي على تشكيل الحويصلات، أو تنظيفها، أو كلاهما. أظهرت هذه التحليلات أن التحكم في تكوين الحويصلات حساس للغاية لمستويات النيتروجين عبر الزمن، بينما تعمل آلية التنظيف بثبات أكبر وغالبًا ما تكون المقيد الرئيسي لتدفق إعادة التدوير الكلي. 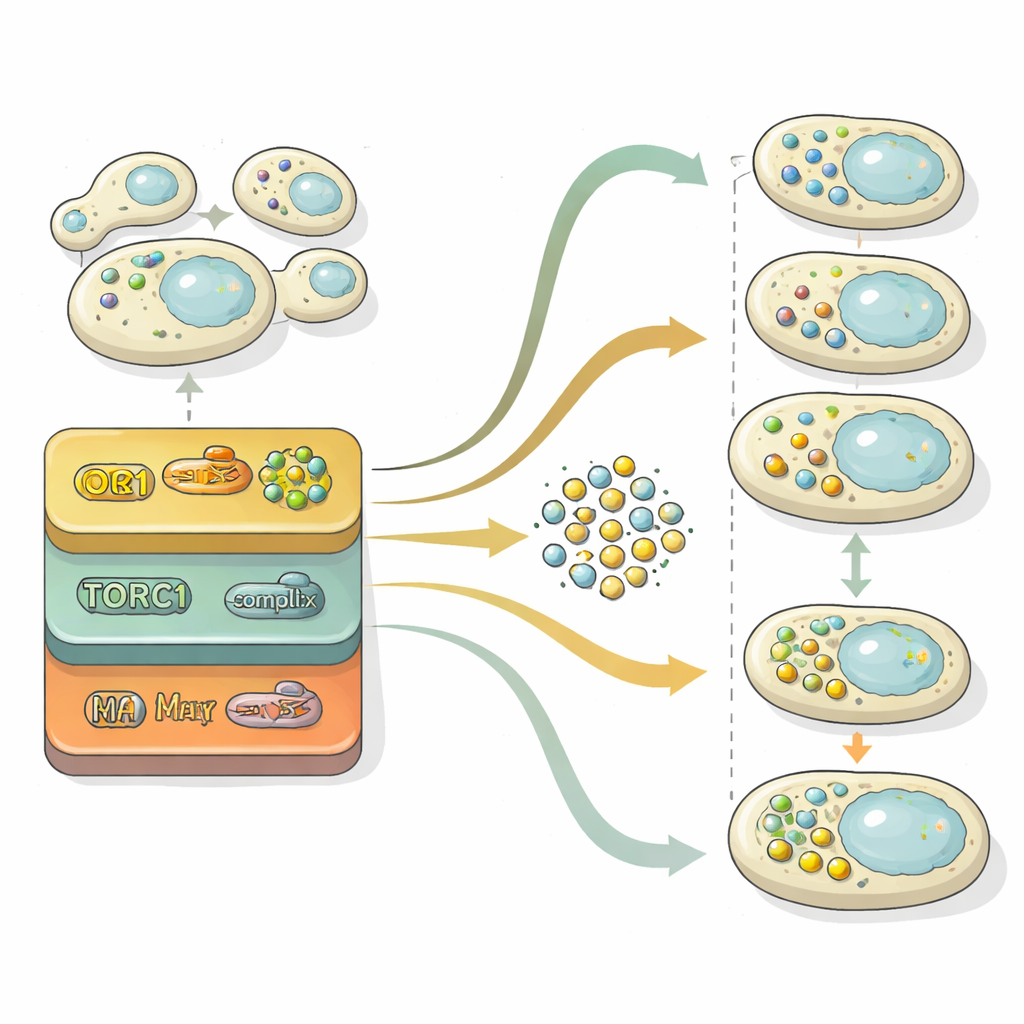
مكابح خفية لإعادة التدوير: المسار الرجعي
كان من أبرز الاكتشافات ما يتعلق بالمسمى بمسار الرجعة (RTG)، الذي ينقل الإشارات من الميتوكوندريا إلى النواة. أنتجت خلايا الخميرة التي تفتقد مكونات RTG عددًا مفرطًا من الحويصلات البلعمية حتى عندما كانت المغذيات متوفرة، وكافحت لتنظيفها بمجرد عودة المغذيات. أظهرت تجارب متابعة مفصّلة أن هذا المسار يسيطر على تعبير جينات البلعمة الذاتية الأساسية، لا سيما المنشط الرئيسي ATG1، إلى حد كبير بشكل مستقل عن حساس المغذيات المعروف TORC1 المستهدف بأدوية مثل الرابامايسين. في الواقع، يعمل إشارة RTG كمكبح متغيّر مع الزمن يمنع اندفاع البلعمة الذاتية في الظروف الغنية ويساعد على إنهاء الاستجابة عندما تتحسن الظروف.
لماذا يهم هذا للصحة والعلاج
بالمجمل، يقدم هذا العمل خريطة جينومية موقوتة توضح كيف تضبط الخلايا البلعمة الذاتية عبر تغير ظروف المغذيات. يكشف أن التشغيل والإيقاف ليسا صورتين معكوسَتين: تؤثر جينات أكثر بكثير على كيفية بدء إعادة التدوير مقارنة بكيفية إيقافها، والتوازن طويل الأمد يعتمد بقوة على تنظيف الحويصلات ومكابح النسخ مثل مسار RTG. بالنسبة للقارئ العام، الخلاصة الأساسية هي أن أكل الخلية لذاتها يخضع لسيطرة متعددة الطبقات والهرمية، وأنه بإمكاننا الآن رسم خريطة هذه الطبقات بدقة عالية. قد يوجّه هذا النوع من الرؤية على مستوى النظم مستقبلاً علاجات أكثر دقة تضبط البلعمة الذاتية في مراحل محددة — تعزيز إعادة التدوير المفيدة دون تحفيز الآثار الضارة للاستهلاك الذاتي المزمن وغير المسيطر عليه.
الاستشهاد: Chica, N., Andersen, A.N., Orellana-Muñoz, S. et al. Time-resolved functional genomics using deep learning reveals global hierarchical control of autophagy. Nat Cell Biol 28, 465–479 (2026). https://doi.org/10.1038/s41556-025-01837-0
الكلمات المفتاحية: البلعمة الذاتية, التعلم العميق, وراثة الخميرة, استشعار المغذيات, إعادة تدوير الخلايا