Clear Sky Science · ar
تعزيز العرض المتقاطع للمستضد كمعزز لقاح السرطان لتوسيع الخلايا التائية والتآزر مع مضاد PD-1
تحويل الجهاز المناعي إلى مقاتل دقيق للأورام
غالبًا ما توصف لقاحات السرطان بأنها تُعلّم الجهاز المناعي التعرف على الأورام وتدميرها، لكن في الواقع نادرًا ما وفّت هذه اللقاحات بهذا الوعد. تستكشف هذه الدراسة طريقة جديدة لـ"شحن" مثل هذه اللقاحات بحيث تولّد خلايا تائية قاتلة أقوى وأطول أمدًا وتعمل بشكل أفضل مع أدوية العلاج المناعي الشائعة مثل مضادات PD‑1. للقراء المهتمين بكيفية جمع علاجات السرطان المستقبلية بين الأدوية البيولوجية واللقاحات والهندسة المناعية، تقدّم هذه الورقة لمحة عما قد تبدو عليه جولات جديدة من العلاج المناعي المستهدفة بدقة.
لماذا تحتاج لقاحات السرطان إلى تعزيز أفضل
تهدف لقاحات السرطان العلاجية إلى معالجة الأشخاص الذين لديهم أورام بالفعل لا إلى الوقاية من المرض، من خلال إثارة استجابات مناعية قوية ومحددة ضد الورم. اللاعبون الرئيسيون هم خلايا CD8 "القاتلة"، التي يمكنها التعرف على الخلايا السرطانية وتدميرها عندما تعرض مستضدات مميزة. للأسف، تكون مستضدات الورم ذات قدرة تحفيزية ضعيفة لأنها تشبه في الغالب نسخًا معدّلة من بروتينات الجسم نفسها. كما أن التعرض المستمر أثناء تطور السرطان قد يترك الخلايا التائية مستنفدة أو متسامحة، مما يضعف تأثير اللقاح. للتغلب على ذلك، يجب إقران اللقاحات بمعززات—مكونات مساعدة توقظ الجهاز المناعي الفطري، وتحسّن عرض المستضدات، وتبني تجمعًا كبيرًا ومرنًا من الخلايا التائية المحددة للورم.
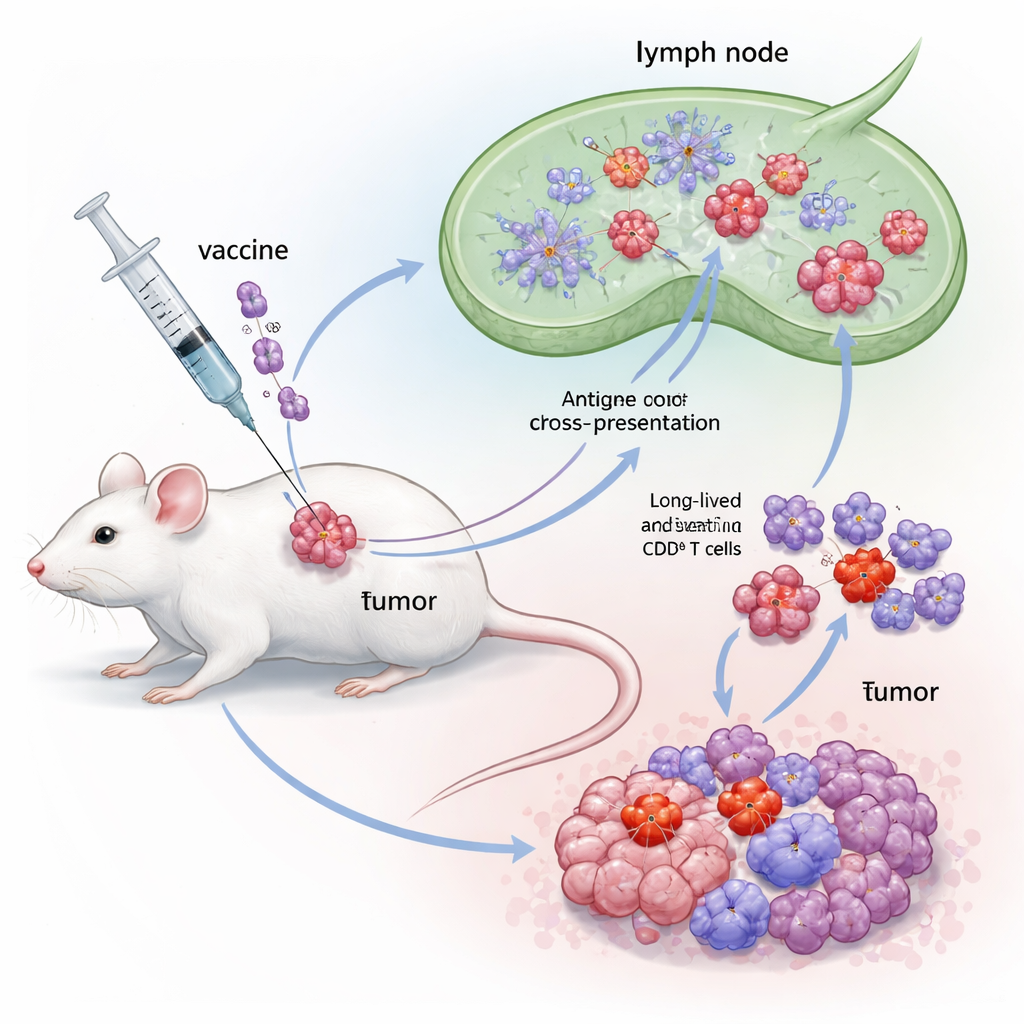
معزز مناعي هجين مبني من إشارتين قويتين
صمّم الباحثون معززًا هجينًا أطلقوا عليه Flt3L‑FlaB أو FB، بدمج جزيئين منشّطين للمناعة في بروتين واحد. النصف الأول، Flt3L، هو عامل نمو طبيعي يوسع مجموعة متخصّصة من خلايا التغصن تُعرف باسم cDC1. هذه الخلايا متفوقة في "العرض المتقاطع"—أخذ أجزاء من مادة الورم وعرضها على خلايا CD8 بطريقة تثير استجابات قوية. النصف الآخر، FlaB، هو جزء من سوط بكتيري ينشط مستقبلًا فطريًا يسمى TLR5 ويعمل كإشارة خطر قوية. بربطهما، هدف المؤلفون إلى توسيع cDC1 وتحويلها إلى حالة نشطة للغاية، محسنين كيفية عرض مستضدات الورم للخلايا التائية ومدة هذا التحفيز.
اختبار المعزز الجديد في نماذج الأورام
لاختبار FB، استخدم الفريق نموذج ورم فأر معتاد قائم على خلايا مُهندَسة لحمل بروتينات ممرضة من فيروس الورم الحليمي البشري (HPV). تلقّت الفئران أولًا زرعة ورمية صغيرة ثم لقاحًا علاجيًا يحتوي على مستضد E7 من HPV، مدموجًا إما مع Flt3L وحده أو FlaB وحده أو مع الاندماج الجديد FB. أعطيت كل اللقاحات قرب الورم. بينما كل معزز منفرد أبطأ نمو الورم بعض الشيء، تميّز لقاح قائم على FB: فقد أخر تقدم الورم بشكل أكبر، وطوّل البقاء بشكل ملحوظ، وترك نسبة ملحوظة من الفئران خالية تمامًا من الورم. أظهرت التحليلات المناعية أن تطعيم FB ولّد استجابات CD8 محددة لـE7 غير معتادة في الدم والعقد اللمفاوية والطحال، مع مستويات عالية من إنترفيرون‑غاما وتكاثر قوي للخلايا التائية—دليل على أن الاندماج فعل أكثر من جمع تأثيري مكونيه.
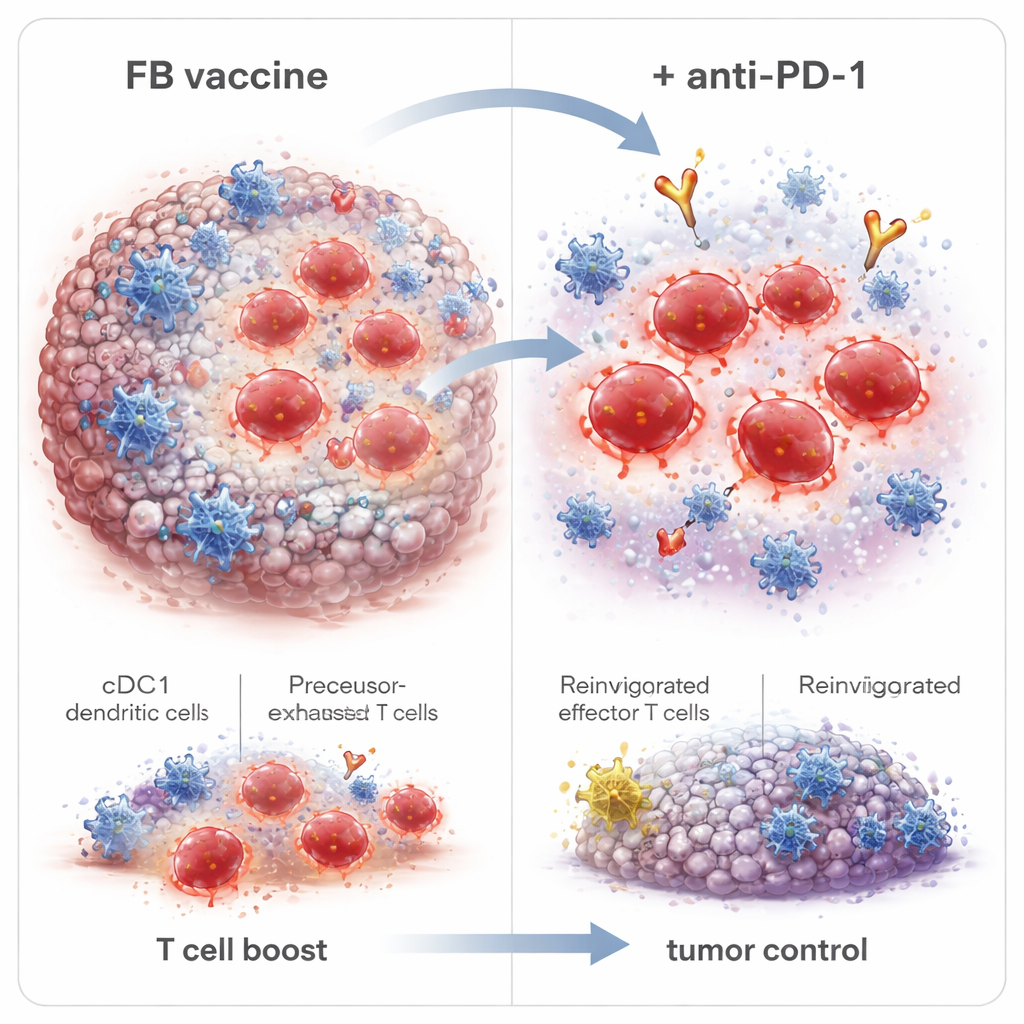
بناء ذاكرة مناعية دائمة وشريك أفضل لـمضاد PD‑1
بتعمق أكبر، وجد العلماء أن FB غيّر ليس فقط كمّية خلايا CD8 التي ظهرت، بل نوعيتها. عزز خلايا تأثيرية قصيرة العمر تهاجم الأورام فورًا، بالإضافة إلى خلايا مسار الذاكرة والخلايا الشبيهة بجذع الذاكرة التي يمكن أن تستمر وتستجيب لاحقًا. والأهم من ذلك، وسّع FB مجموعة تُعرف بالخلايا التائية ما قبل المستنفدة (Tpex) داخل الأورام—وهي خلايا تقع عند الحدود بين الإجهاد الوظيفي والنشاط الكامل وتكون مستجيبة بشكل خاص لأدوية مضاد PD‑1. عندما تحدوا الحيوانات الناجية الخالية من الورم بجرعات أعلى من الخلايا السرطانية بعد وقت طويل من التطعيم، أمكن لمعظمها مقاومة إعادة النمو، مظهرة ذاكرة مناعية دائمة. إعاقة خروج الخلايا المناعية من العقد اللمفاوية ألغت فوائد FB، مما يشير إلى أن الخلايا التائية القاتلة للورم تُهيَّأ في تلك العقد بواسطة cDC1 ثم هاجرت إلى الورم.
أقوى معًا: اللقاحات بالإضافة إلى حجب نقاط التفتيش
بما أن علاج مضاد PD‑1 يعمل بصورة أفضل عندما يوجد مسبقًا تجمع من الخلايا التائية القابلة للاستجابة، جمع الفريق التطعيم المعزّز بـFB مع مضاد PD‑1 أحادي النسيلة. في نموذج ورم HPV، أدى إضافة مضاد PD‑1 على قمة تطعيم FB إلى إبطاء نمو الورم أكثر، وزيادة عدد الفئران التي نقّت أورامها تمامًا، وتوفير حماية كاملة ضد تحدٍ ثانٍ بجرعة عالية جدًا من الورم. وكان توقيت العلاج مهمًا: بدء مضاد PD‑1 بعد الجرعة الثانية من اللقاح بدلًا من الأولى حسّن بدرجة طفيفة الاستئصال التام للورم، متوافقًا مع الانتظار حتى تتوسع خلايا Tpex. كما حسّن معزز FB الاستجابات للقاحات قائمة على الببتيدات، بما في ذلك المستضدات الطافرة الخاصة بالورم في نموذج سرطان القولون، ما يشير إلى أن هذه الاستراتيجية قد تُطبق على نطاق أوسع يتجاوز الأمراض المرتبطة بـHPV.
ماذا قد يعني هذا لرعاية السرطان المستقبلية
للغير متخصصين، الرسالة الأساسية هي أن هذا العمل يصقل طريقة "تعليم" الجهاز المناعي لمحاربة السرطان. عبر دمج عامل نمو خلايا التغصن مع إشارة خطر قوية في بروتين واحد ومستقر، يخلق معزز FB المزيد من خلايا عرض المستضد المناسبة، ويساعدها على عرض مستضدات الورم بفاعلية أكبر، ويشكّل تجمعًا من الخلايا التائية القاتلة التي هي قوية الآن ومهيأة للاستجابة لاحقًا لعلاج نقاط التفتيش. بينما أجريت النتائج في فئران وما تزال خطوات كثيرة تفصلها عن الاستخدام البشري، ترسم الدراسة خارطة طريق واضحة: معززات أذكى تُنظّم العرض المتقاطع وجذعية الخلايا التائية قد تجعل لقاحات السرطان العلاجية شريكًا أقوى بكثير لأدوية مثل مضاد PD‑1، مما قد يؤدي إلى سيطرة أعمق وأطول أمداً على الأورام لدى المرضى.
الاستشهاد: Dang, G.C., Loeurng, V., Pa, P. et al. Antigen cross-presentation potentiating cancer vaccine adjuvant for T cell expansion and synergy with anti-PD-1. npj Vaccines 11, 56 (2026). https://doi.org/10.1038/s41541-026-01376-1
الكلمات المفتاحية: لقاحات السرطان, العلاج المناعي, خلايا التغصن, حجب PD-1, أورام مرتبطة بفيروس الورم الحليمي البشري