Clear Sky Science · ar
تصميم لقاح مخاطي واسع الطيف لفيروسات كورونا البشرية مستوحى من الأجسام المضادة الاصطناعية
لماذا لا يزال لقاح كورونا الأفضل مهمًا
حتى مع تحول كوفيد-19 إلى عدوى موسمية، تستمر موجات من السلالات الجديدة في الظهور، ولا تزال عدة فيروسات كورونا بشرية أخرى تسبب أمراضًا خطيرة. اللقاحات الحالية تحدّ من المرض الشديد بشكل جيد لكنها أقل فعالية في منع العدوى والانتقال، لا سيما في الأنف والحلق حيث تستقر هذه الفيروسات أولاً. تصف هذه الدراسة نوعًا جديدًا من لقاح الأنف المستوحى من الأجسام المضادة المصممة هندسيًا، ويهدف إلى تقديم حماية طويلة الأمد وواسعة النطاق عبر العديد من فيروسات الكورونا عند خط المواجهة المخاطي في الجسم.
بناء هيكل لقاح أكثر ذكاءً
بدأ الباحثون من جزيء مألوف: IgG1 البشري، نوع الجسم المضاد الرئيسي المستخدم في العديد من أدوية الأجسام المضادة المعتمدة. أعادوا تصميم السلسلة الثقيلة بحيث يمكن أن تعمل كـ "هيكل" مرن لعرض مجالات ارتباط المستقبلات في بروتين السنبلة للفيروس (RBDs) — الأجزاء التي يستخدمها الفيروس لالتقاط خلايانا. عبر إزالة السلسلة الخفيفة المعتادة وإضافة طفرات محددة، خفّضوا الارتباط بمستقبلات الجهاز المناعي المرتبطة بآثار جانبية مثل عواصف السيتوكين، بينما عززوا الارتباط بمستقبل الـ Fc الوليدي (FcRn). FcRn وفير على الأسطح المخاطية ويساعد في نقل الأجسام المضادة عبر الحاجز وإبقائها لفترات أطول. على هذا العمود الفقري المحسّن، أرفق الفريق واحدًا أو اثنين أو ثلاثة أو أربعة RBDs مختلفة من SARS وMERS وفيروسات كورونا الموسمية وعدة متغيرات من SARS‑CoV‑2، بما في ذلك سلالات أوميكرون، مما أدى إلى إنشاء مرشحين للقاح أحادي وثنائي وثلاثي ورباعي التكافؤ.
عبور الحاجز المخاطي وتنشيط الدفاعات المحلية
لكي يعمل اللقاح كرذاذ أنفي، يجب أن تصل المستضدات وتستمر في بطانة المسالك الهوائية وأن يتم ملاحظتها بكفاءة من قبل الخلايا المناعية. في أنظمة زراعة الخلايا، ارتبطت التركيبات الحاملة لـ Fc بقوة بكل من ACE2 (مستقبل دخول SARS‑CoV‑2) وFcRn البشري أو الفأري، ونُقلت بنشاط عبر طبقة من الخلايا المخاطية. فشل ثنائي RBD مماثل يفتقد جزء Fc في العبور. عندما نُفّذت نسخ فلورية من اللقاحات في أنوف الفئران، بقيت المستضدات الحاملة لـ Fc في مخاط الرئة لساعات، بينما اختفى ثنائي RBD الخالص بسرعة. أظهرت الميكروسكوبية أن اللقاحات المعدّلة بـ Fc جذبت ونشّطت الخلايا العارضة للمستضد مباشرة تحت السطح المخاطي، كما دلّت المستويات الأعلى من علامة المناعة CD80 والتعايش مع FcRn على ذلك.
تعزيز الأجسام المضادة والخلايا التائية حيثما يلزم
قارن الفريق بعد ذلك الاستجابات المناعية بعد الحقن العضلي مقابل الإعطاء عبر الأنف في الفئران. عبر عدة تركيبات، أثارت اللقاحات القائمة على Fc مستويات عالية جدًا من الأجسام المضادة IgG في الدم ضد كل من السلالة الأصلية لـ SARS‑CoV‑2 وأوميكرون XBB.1.5. برزت الجرعات الأنفية، خاصة عند دمجها مع مُحفّز حديث منبّه لنظام STING (CF501)، في توليد استجابات قوية من IgA ليس فقط في الدم بل أيضًا في إفرازات الأنف وغسولات الرئة — بالضبط حيث تكون الحماية المخاطية أكثر أهمية. كما دفعت التركيبات الحاملة لـ Fc استجابات خلوية أقوى من ثنائيات RBD العارية، موسعة خلايا T المساعدة، وخلايا T القاتلة، وخلايا الذاكرة المقيمة طويلة الأمد في الأنسجة بالرئتين. وتُعد هذه الأنواع من الخلايا حاسمة على ما يُعتقد لإخراج فيروسات الجهاز التنفسي ومنع انتشارها إلى أعضاء حساسة مثل الدماغ.
حماية واسعة ضد العديد من المتغيرات والأنواع
كان اختبار مركزي هو ما إذا كان لقاح ثنائي التكافؤ يجمع RBDs من الفيروس النموذجي وأوميكرون XBB.1.5 (المسمى XBB.1.5 + PT‑Fc) يمكن أن يحمي الحيوانات من تحديات فيروسية متعددة. في فئران معبّرة عن ACE2 البشري أعطيت جرعتين منخفضتين عبر الأنف، حفز هذا المرشح أجسامًا محايدة قوية وحمى الحيوانات تمامًا من عدوى مميتة بكل من الفيروس الأصلي وXBB.1.16: حافظت الفئران الملقّحة على وزنها وبقِيَت حية ولم يُكتشف فيروس في المخ أو الرئتين أو أنسجة الأنف، بينما مرضت الحيوانات الضابطة وماتت. حجب نفس اللقاح المرض والوفاة عندما تحدّت الفئران بمتغيرات رئيسية أخرى بما في ذلك بيتا ودلتا وعديد من الفروع الفرعية لأوميكرون. في الهامستر، المناسبة لدراسات الانتقال، كان لدى الحيوانات الملقّحة أحمال فيروسية أقل بكثير بعد التحدي المباشر، وفي تجارب التعايش كانت محمية إلى حد كبير من الانتقال الجوي. بقيت مستويات الأجسام المضادة وخلايا الذاكرة التائية في كل من الفئران والهامسترات مرتفعة لمدة لا تقل عن 48 أسبوعًا، وبقيت الحيوانات محمية تمامًا من التحديات المميتة تقريبًا بعد سنة من التلقيح.
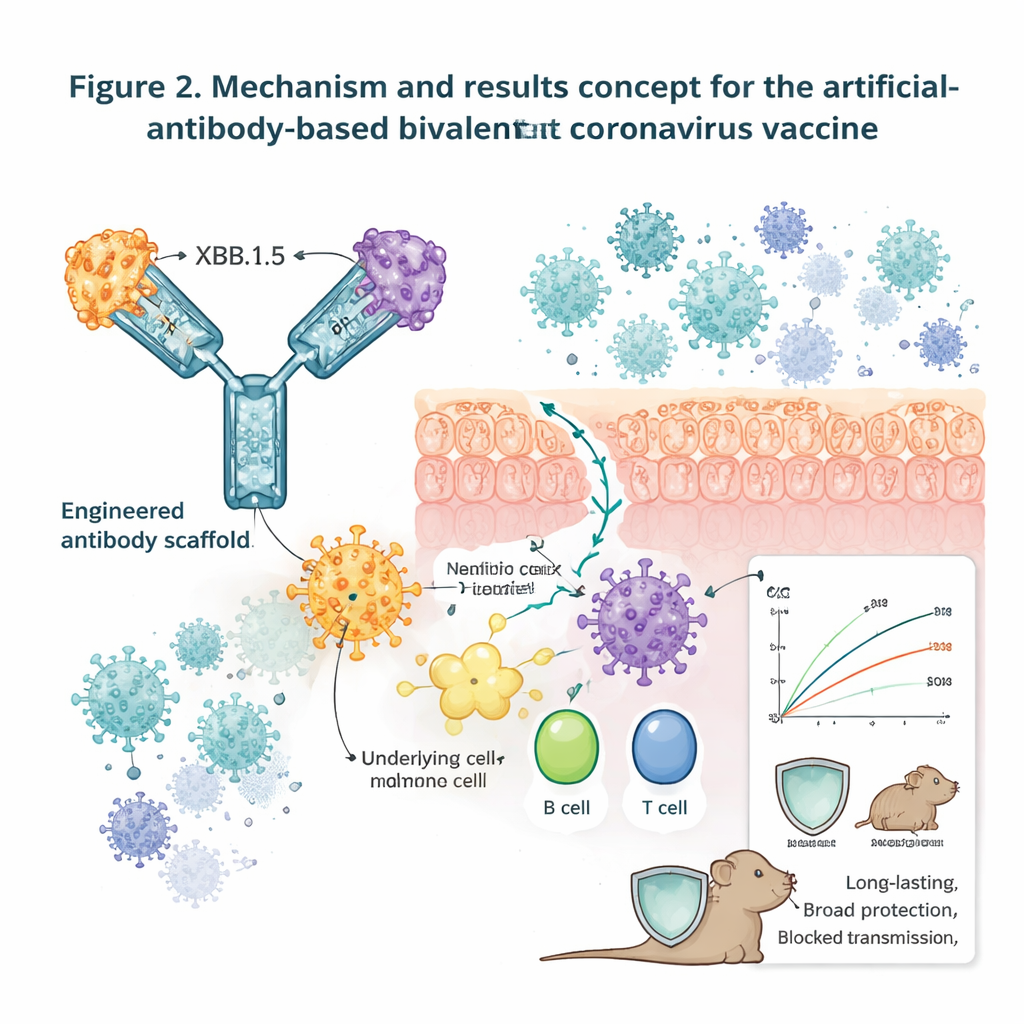
نحو رذاذ أنفي عالمي لفيروسات الكورونا
أخيرًا، دفع الباحثون المنصة نحو تصميم عالمي حقًا. مزجوا عدة تركيبات ثنائية التكافؤ تغطي SARS‑CoV‑2 وSARS وMERS والعديد من فيروسات كورونا الموسمية، وبنوا أيضًا جزيئات رباعية التكافؤ تحمل أربعة RBDs مميزة أو شظايا سنبلة على هيكل واحد. رفعت هذه التركيبات أجسامًا مضادة تعرف مجموعة واسعة من فيروسات كورونا البشرية وفي تجارب تحدي الفئران خفّضت الأحمال الفيروسية لعدة ممثلين، بما في ذلك فيروس مستوطن (NL63). بالرغم من الحاجة لمزيد من الاختبارات في نماذج أقرب إلى البشر ومن ثم في تجارب سريرية، تظهر الدراسة أن عمودًا فقريًا من جسم مضاد مصمَّم يمكنه نقل مستضدات مختلفة لفيروسات كورونا بأمان عبر حاجز الأنف، وتنشيط مناعة محلية ومنهجية قوية، وتوفير حماية واسعة ومتينة. للقراء غير المتخصصين، الرسالة هي أن معززات كورونا المستقبلية "الشاملة" قد لا تكون حقنًا على الإطلاق، بل رذاذات أنفية لطيفة مبنية على نفس أطر الأجسام المضادة التي أثبتت سلامتها في العديد من الأدوية.
الاستشهاد: Wu, Y., Lu, J., Fang, L. et al. Universal broad-spectrum mucosal vaccine design for human coronaviruses inspired by artificial antibodies. npj Vaccines 11, 55 (2026). https://doi.org/10.1038/s41541-026-01375-2
الكلمات المفتاحية: لقاح عبر الأنف, فيروس كورونا واسع الطيف, المناعة المخاطية, هيكلية جسم مضاد اصطناعي, سلالات SARS-CoV-2