Clear Sky Science · ar
التغلب على مقاومة مثبطات التيروسين كيناز التي يساهم بها الحيز الوعائي في اللوكيميا النخاعية الحادة من خلال تثبيط miR-126
لماذا هذا مهم لمرضى السرطان
اللوكيميا النخاعية الحادة (AML) هي أحد أكثر أورام الدم عدوانية، وحتى مع الأدوية المستهدفة الحديثة يواجه العديد من المرضى نكسًا. تسأل هذه الدراسة سؤالًا يبدو بسيطًا لكنه ذو تداعيات كبيرة: هل المشكلة ليست فقط خلايا السرطان نفسها، بل أيضاً «الحي» الذي تعيش فيه داخل نخاع العظم؟ من خلال بناء نموذج حاسوبي مفصل مستند إلى بيانات مخبرية، يستكشف المؤلفون كيف يمكن للأوعية الدموية الدقيقة أن تحجب خلايا جذعية اللوكيميا عن الأدوية—وكيف أن حجب إشارة رنا صغيرة واحدة قد يفتت هذا الحِماية.
الملجأ الخفي في نخاع العظم
تنشأ AML في نخاع العظم، حيث تحتل الخلايا الطافرة الخبيثة مكان إنتاج الدم الطبيعي. داخل هذا التجمع تختبئ مجموعة أصغر من خلايا جذع اللوكيميا القادرة على تجديد نفسها والبقاء على قيد الحياة بعد العلاج، مما يؤدي إلى النكس. هذه الخلايا الجذعية لا تطفو بحرية؛ بل تستقر في جيوب متخصصة حول الشرايين الصغيرة والشعيرات الدموية، المعروفة مجتمعة باسم الحيز الوعائي. تركز الدراسة على المرضى الذين تحمل خلاياهم الطافرة طفرات FLT3-ITD، والتي تُعالج بمثبطات التيروسين كيناز (TKIs). وعلى الرغم من أن هذه الأدوية قد تقلص عبء الورم بشكل حاد، إلا أن العديد من المرضى يعودون بالنكس، ما يشير إلى أن بعض الخلايا تُخفي أو تُحمى.
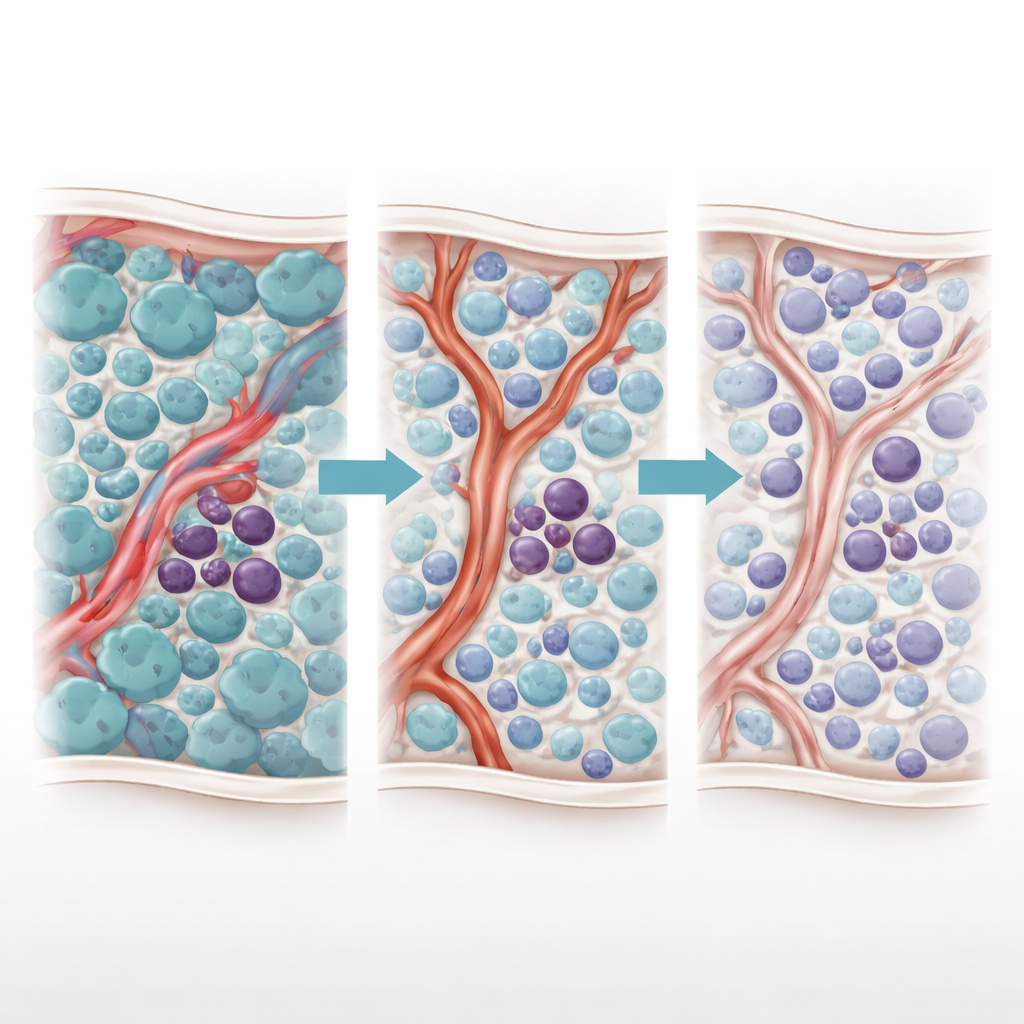
تأثير علاجي ذو وجهين
كشف المؤلفون سابقًا عن «ظاهرة جانوس» المحيرة—استجابة ذات وجهين للعلاج بمثبطات التيروسين كيناز. بينما تقضي هذه المثبطات على الخلايا الطافرة سريعة الانقسام، تنخفض مستويات جزيء التهابي، TNF-α. هذا الانخفاض يسمح بشكل غير متوقع لخلايا الأوعية القريبة بزيادة إنتاج رنا تنظيمي صغير يُسمى miR-126. ينتقل هذا miR-126 من الخلايا البطانية إلى خلايا جذع اللوكيميا، ويحثها على الدخول في حالة هدوء وعدم انقسام تجعلها شديدة المقاومة للأدوية. بعبارة أخرى، العلاج الذي يزيل معظم خلايا السرطان يعيد تشكيل نخاع العظم بطريقة تحمي أخطر الخلايا.
بناء نخاع عظم افتراضي
لتفكيك هذا الديناميك، أنشأ الفريق نموذجًا حاسوبيًا معتمدًا على عملاء لوصف نخاع عظم AML. كل لاعب رئيسي—الخلايا الطافرة، وخلايا جذع اللوكيميا، والخلايا البطانية المبطنَة للأوعية—ممثّل كـ"عميل" فردي يتبع قواعد مستنِدة إلى البيولوجيا. تنتشر جزيئات متفَسِّحة مثل TNF-α وmiR-126 والمثبط AC220 ودواء مانع لـmiR-126 يسمى miRisten عبر النسيج المحاكَى. تم معايرة النموذج ببيانات تصوير من الفئران تُظهر نمطًا وعائيًا حقيقيًا، بما في ذلك مناطق غنية أو فقيرة بالأوعية المنتجة لـmiR-126. في المحاكاة، أعاد العلاج القياسي بالمثبط الظاهرة الجانوسية بشكل موثوق: تراجعت الطافرات، انخفض TNF-α، ارتفع miR-126 المنتج من الأوعية، تراجعت الخلايا الجذعية إلى ملاجئ واقية، ثم عاد المرض لاحقًا.
إطفاء الدرع بتوقيت دقيق
مسلَّحين بهذا النظام الافتراضي، اختبر الباحثون طرقًا لكسر هذه الحلقة المفرغة. إضافة miRisten في الوقت نفسه مع المثبط ساعدت لكنه نادرًا ما قضت على المرض في النموذج. كان نهج أكثر استراتيجية أقوى: "معالجة تمهيدية" قصيرة بـmiRisten وحده لخفض miR-126 الوعائي، تلتها إما مثبط وحده أو استمرار العلاج المزدوج. عبر تخطيطات وعائية محاكاة متعددة، قلّلت حتى بضعة أيام من المعالجة التمهيدية بـmiRisten قبل بدء AC220 بشكل كبير أو أزالت النكس مع تقليل التعرض الإجمالي للأدوية. كما كشف النموذج أن مدى قرب خلايا جذع اللوكيميا من الأوعية يؤثر بقوة على مصيرها—فالخلايا الملتحمة مباشرة بالأوعية تكتسب أكبر قدر من الحماية ما لم يُحظر miR-126.
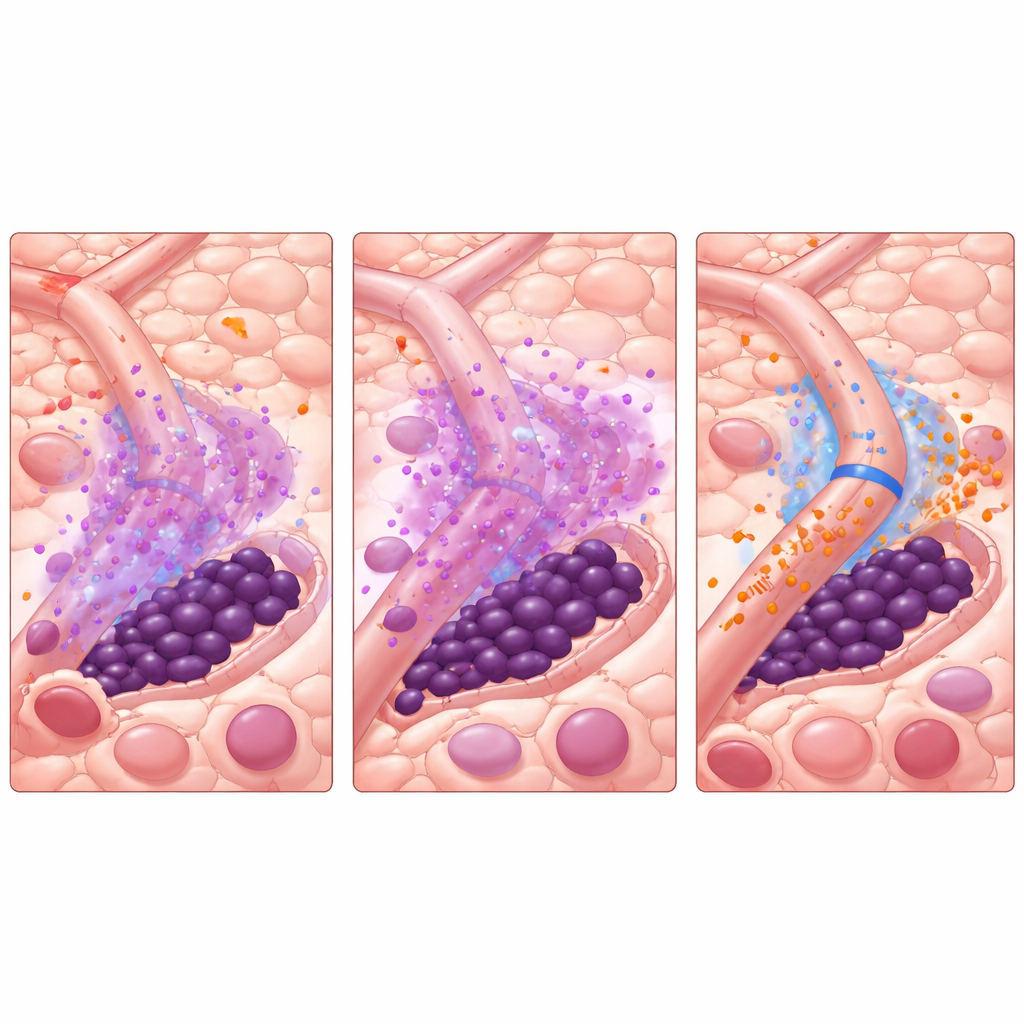
ما الذي قد يعنيه هذا للرعاية المستقبلية
بعبارة بسيطة، تقترح الدراسة أن بعض خلايا جذع اللوكيميا تبقى على قيد الحياة ليس لأن مثبطات التيروسين كيناز ضعيفة، بل لأن الأوعية الدموية الصغيرة في نخاع العظم تتحول مؤقتًا إلى «وضع الحماية» أثناء العلاج. من خلال إيقاف إشارة واحدة، miR-126، لفترة وجيزة قبل إعطاء المثبط، قد يكون من الممكن نزع هذا الدرع، وإجبار الخلايا الجذعية على الخروج من اختبائها، وجعلها قابلة للقضاء بواسطة الأدوية الموجودة. وبينما يستند هذا العمل إلى محاكيات حاسوبية مرتبطة ببيانات مخبرية—وليس بعد تجارب سريرية—فإنه يقدم استراتيجية ملموسة: توقيت دواء يستهدف البيئة الدقيقة قبل وخلال العلاج القياسي. إذا ثُبِّتت فعاليتها، فقد تحسّن هذه الطريقة النتائج لمرضى AML الحاملين طفرة FLT3، وقد تُلهم أيضاً تكتيكات مماثلة في سرطانات دموية وصلبة أخرى حيث تساعد بيئة الورم على تفادي العلاج.
الاستشهاد: Froid, M., Branciamore, S., Chen, Z. et al. Overcoming vascular niche–mediated TKI resistance in acute myeloid leukemia through miR-126 inhibition. npj Syst Biol Appl 12, 38 (2026). https://doi.org/10.1038/s41540-026-00675-6
الكلمات المفتاحية: اللوكيميا النخاعية الحادة, خلايا جذعية ليمفاوية ابيضاض الدم, البيئة الدقيقة لنخاع العظم, مقاومة مثبط التيروسين كيناز, تثبيط miR-126