Clear Sky Science · ar
تطوير نموذج حاد لمتلازمة إعادة التغذية في الجرذان والنمذجة الرياضية للنقص المصاحب في الفوسفور بالدم
لماذا يمكن أن يكون تناول الطعام مجدداً خطيراً
عندما يتلقى أشخاص مصابون بسوء تغذية شديد طعاماً أخيراً أو تغذية وريدية، يجب على الأطباء التقدّم بحذر. تدفق السعرات المفاجئ قد يثير «متلازمة إعادة التغذية»، وهي مضاعفة تعطل توازن الأملاح في الجسم وقد تضر القلب والعضلات والرئتين. لاعب رئيسي في ذلك هو الفوسفور، المعدن الضروري لإنتاج الطاقة في كل خلية. استخدمت هذه الدراسة جرذاناً ونمذجة حاسوبية لتوضيح سبب انهيار مستوى الفوسفور في الدم بشكل حاد أثناء إعادة التغذية، وكيف يمكننا منع هذا الانخفاض الخطير بشكل أفضل.
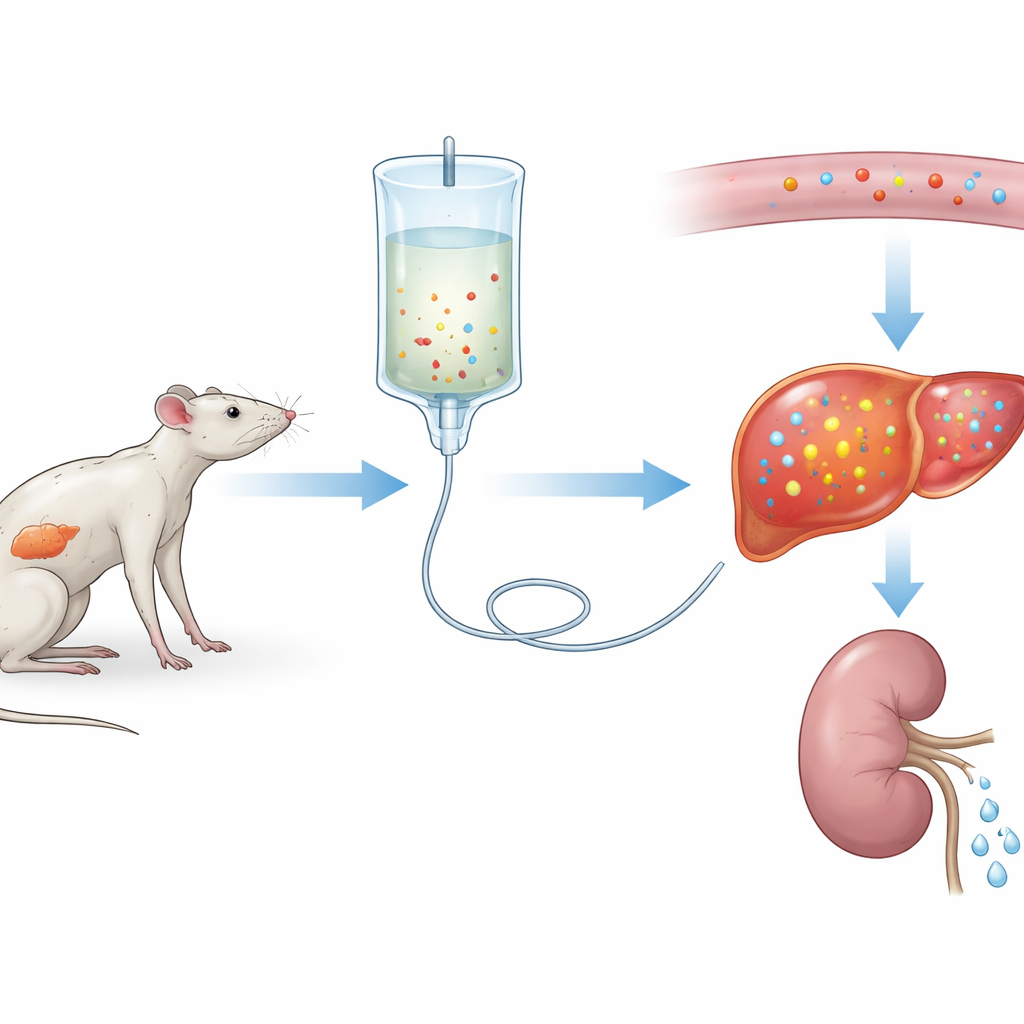
نظرة أعمق على مشاكل إعادة التغذية
ابتكر الباحثون أولاً نسخة شديدة من متلازمة إعادة التغذية في الجرذان. على مدى ثلاثة أسابيع، تناولت مجموعة حمية عادية بينما تلقت مجموعة أخرى بروتيناً قليلاً جداً، محاكاة لسوء التغذية طويل الأمد. ثم خُصّصت المجموعتان لتغذية وريديّة مماثلة لثلاثة أيام. أظهرت الجرذان التي كانت على حمية منخفضة البروتين هبوطاً حاداً في فوسفور الدم — نحو 75% انخفاض — إلى جانب تحولات في أملاح أخرى وعلامات ضرر في الأعضاء، خاصة في الكبد والعضلات. شبّهت هذه التغيرات متلازمة إعادة التغذية الخطيرة لدى المرضى، مما يوحي بأن الفريق بنى نموذجاً تجريبياً موثوقاً.
ماذا يحدث للفوسفور أثناء إعادة التغذية
لفهم كيفية تحرك الفوسفور في الجسم مع مرور الزمن، أخذ العلماء عينات متكررة من الدم والبول لنفس الجرذان. وجدوا أن مستويات فوسفور الدم انخفضت في كل من الحيوانات العادية والمحرومة من البروتين بعد بدء التغذية، لكن الانخفاض كان أعمق وأكثر استمرارية في المجموعة المصابة بسوء التغذية. والمفاجئ أن الكليتين قلّلتا بالفعل فقدان الفوسفور في البول فور إعادة التغذية، لذا لم يكن المعدن يُطرح خارج الجسم. بدلاً من ذلك، سحب الفوسفور من مجرى الدم إلى الأنسجة، خصوصاً الكبد، حيث كانت مخازنه قد استُنفدت خلال أسابيع من الحمية السيئة. أكدت الحسابات الحاسوبية أن الجرذان المحرومة بدأت بمستويات داخل خلوية من الفوسفور أقل بكثير ثم امتصتها بقوة بمجرد وصول المغذيات.
الأنسولين ليس القصة كلها
بما أن إعادة التغذية ترفع سكر الدم والهرمون الأنسولين، فقد ألقى الأطباء باللوم طويلاً على الأنسولين في دفع الفوسفور إلى داخل الخلايا. اختبر الفريق هذه الفكرة بتخفيض إفراز الأنسولين باستخدام هرمون السوماتوستاتين. كما كان متوقعاً، ارتفع سكر الدم، لكن الانخفاض في فوسفور الدم كاد ألا يتحسن. وفي الوقت نفسه، ارتفعت مستويات الأحماض الأمينية الحرة — لبنات البناء للبروتينات. في تجربة منفصلة، أزال العلماء الأحماض الأمينية من المحلول المُعطى. الآن، بقيت مستويات الفوسفور أكثر استقراراً، ومنع الانهيار الشديد، على الرغم من أن مستويات الأنسولين كانت متشابهة. تشير هذه النتائج إلى تأثير مركب: الأنسولين والأحماض الأمينية معاً، وليس الأنسولين وحده، يدفعان الخلايا إلى امتصاص فوسفور إضافي أثناء إعادة التغذية.
شبكة تحكم خفية في الكبد والكليتين
بالتعمق أكثر، فحص الباحثون بروتينات الكبد المشاركة في استشعار المغذيات، مع التركيز على مسار معروف باسم mTOR، الذي يستجيب للأنسولين والأحماض الأمينية. في الجرذان منخفضة البروتين، نشطت إعادة التغذية هذا المسار بقوة وزادت مستويات ناقل الفوسفات المسمى Pit2، الذي يساعد خلايا الكبد على سحب الفوسفور. طابقت النمط سلوك النموذج الرياضي لديهم، الذي جمع هذه الشبكة في إشارة تحكم واحدة أطلقوا عليها «simTOR». كما تطلب النموذج عامل تغذية راجعة منفصل ليشرح كيف تضبط الكلى فقدان الفوسفور في البول. ولعبت قياسات هرمون منشأ من العظام، FGF-23، هذا الدور جيداً: فقد انهارت مستوياته عند بدء التغذية، محدودةً طرح الفوسفور، ثم تباينت بين الجرذان العادية والمحرومة بطريقة انعكست في إشارة التغذية الراجعة المحاكاة.
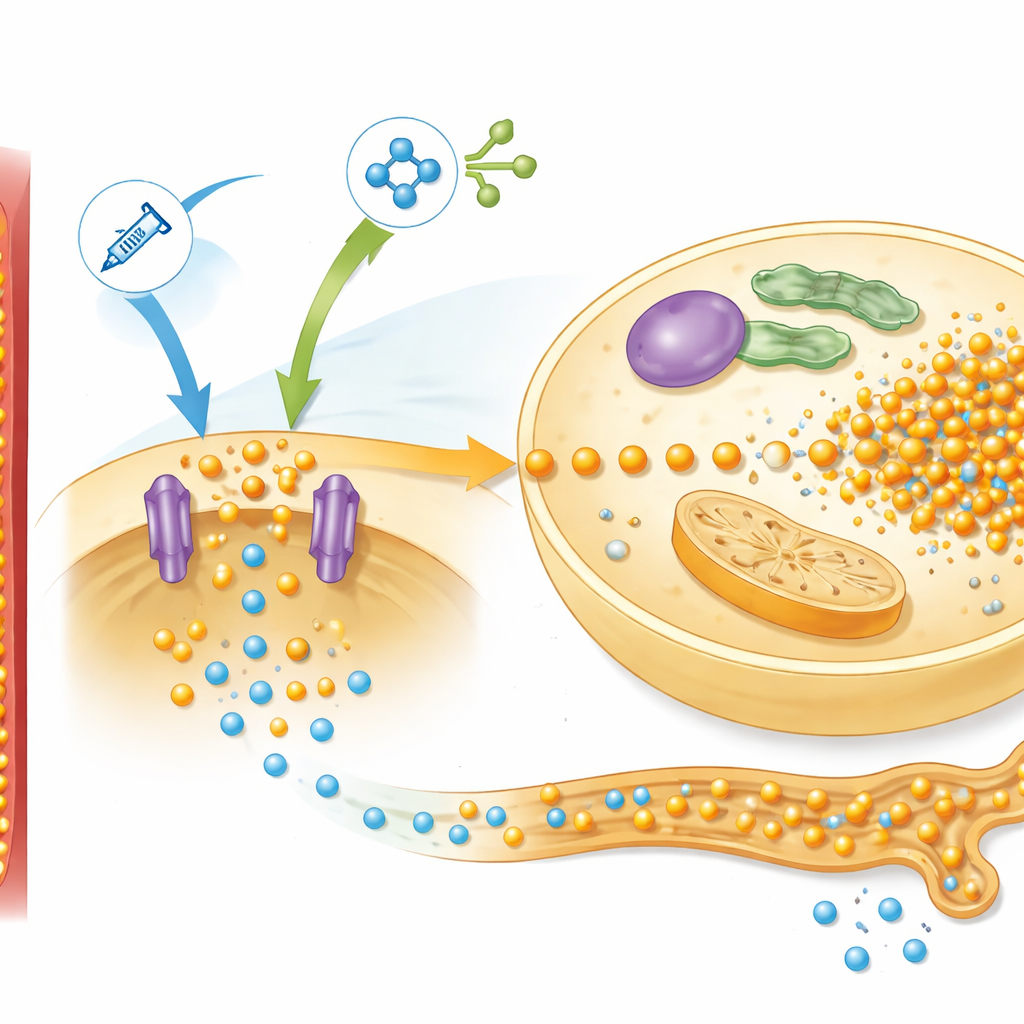
استخدام الرياضيات لاختبار استراتيجيات الوقاية
من خلال ضبط مؤشرات مختلفة في نموذجهم الحاسوبي، استطاع المؤلفون طرح أسئلة «ماذا لو» التي قد تكون صعبة أو محفوفة بالمخاطر لاختبارها مباشرة في المرضى. أبرز التحليل ثلاثة مؤثرات رئيسية على عمق ووقت تعافي انخفاض الفوسفور: الفوسفور الداخلي الابتدائي داخل الخلايا، قوة نظام الامتصاص المدفوع بـ mTOR، ومعدل دخول الفوسفور من التغذية. أشارت المحاكاة إلى أن إضافة كمية كبيرة من الفوسفات في وقت إعادة التغذية ستكون صعبة الموازنة بأمان. ومع ذلك، فإن إعطاء فوسفور إضافي قبل إعادة التغذية — مما يسمح للأعضاء بإعادة بناء مخازنها الداخلية بهدوء — قد يخفف من الانهيار اللاحق في مستويات الدم. كما بدا أن تقليل حمولة الأحماض الأمينية، لا سيما تلك التي تنشط mTOR والأنسولين بشدة، حماية فعالة في التجارب الحيوانية.
ماذا يعني هذا للمرضى
بالنسبة للأشخاص المعرضين لمتلازمة إعادة التغذية — مثل من لديهم اضطرابات غذائية طويلة الأمد أو هزال شديد — تشير هذه الدراسة إلى أن الخطر لا ينشأ من ارتفاع سكر الدم فقط. تدخل الأعضاء الجائعة إعادة التغذية بخزانات فوسفور فارغة، ثم تحت الدفع المشترك من الأنسولين والأحماض الأمينية، تمتص المعدن بسرعة من الدم بينما تحتفظ الكليتان به مؤقتاً. النتيجة نقص حاد ومؤقت في الدورة الدموية يمكن أن يضر الأنسجة الحيوية. يشير نموذج الجرذان والإطار الرياضي المطور هنا إلى سبل وقاية أكثر استهدافاً: استخدام حذر ومبكر لمكملات الفوسفور، التحكم الدقيق بالمغذيات الغنية بالأحماض الأمينية، والانتباه إلى الهرمونات التي تحكم طرح الكلى. معاً، قد تساعد هذه المقاربات الأطباء على تغذية المرضى الضعفاء بأمان أكبر.
الاستشهاد: Kato, H., Yamaoka, I. & Kubota, H. Development of a severe rat refeeding syndrome model and mathematical modeling of the associated hypophosphatemia. npj Syst Biol Appl 12, 34 (2026). https://doi.org/10.1038/s41540-026-00658-7
الكلمات المفتاحية: متلازمة إعادة التغذية, نقص فوسفاط الدم, تمثّل الفوسفور, إشارات mTOR, التغذية الوريدية