Clear Sky Science · ar
تحليل التدفق الفراغي يكشف عن جيوب واربُرغ متغايرة في أورام الكلى واستهلاك اللاكتات في سرطان القولون والمستقيم
لماذا يهم استقلاب الورم في الفضاء
لا تتصرف خلايا السرطان جميعها بنفس الطريقة، حتى داخل ورم واحد. بعضها يعيش قرب الأوعية الدموية، وبعضها الآخر في مناطق بعيدة ضعيفة التروية، وهذه المواضع تشكل كيفية حصولها على الوقود واستخدامه. تقدّم هذه الدراسة طريقة جديدة لقراءة «الخريطة الأيضية» الخفية من بيانات التعبير الجيني المكاني المتقدمة. ومن خلال ذلك، يكتشف المؤلفون نمطيات مفاجئة في كيفية تعامل الأورام المختلفة مع جزيء محوري هو اللاكتات، مما يتحدى الرؤية الكلاسيكية القائلة بأن السرطانات تتخلص من اللاكتات كنفايات فقط.
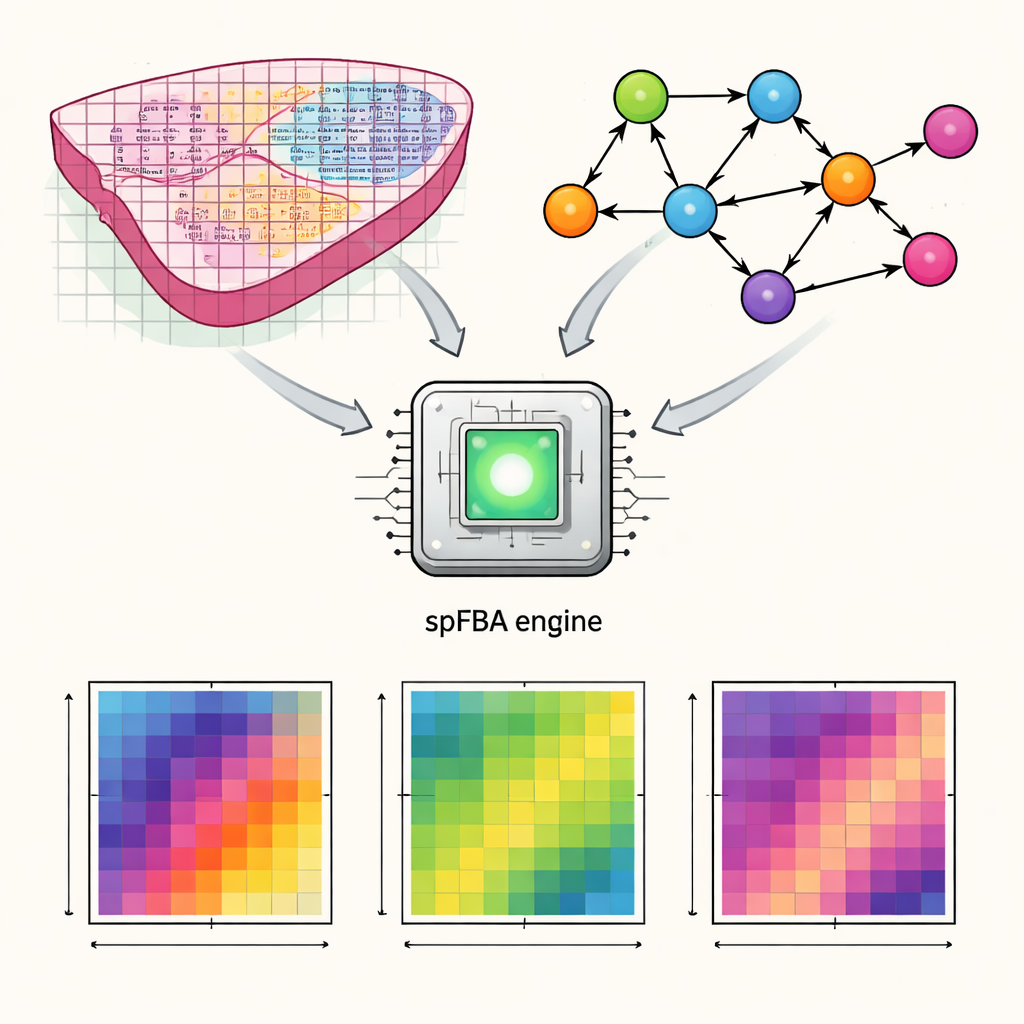
تحويل خرائط الجينات إلى نشاط أيضي
طوّر المؤلفون إطارًا حاسوبيًا يسمونه تحليل التوازن التدفقي المكاني، أو spFBA. تقيس تقنيات النسخية المكانية أي الجينات نشطة في آلاف النقاط الصغيرة عبر شريحة رقيقة من النسيج. يجمع spFBA هذه خرائط نشاط الجينات المكانية مع نماذج مفصّلة لاستقلاب الإنسان، التي تصف كيف تُحوَّل المغذيات مثل الغلوكوز والأكسجين والأحماض الأمينية داخل الخلايا. بدلاً من افتراض أن كل منطقة من النسيج تشترك في هدف أيضي واحد، يعالج spFBA كل نقطة بشكل مستقل، مستكشفًا أنماط التفاعلات الممكنة هناك بموجب قوانين الكيمياء وتوازن الكتلة. الناتج هو مجموعة من «درجات إغناء التدفق» التي تشير، لكل موضع، إلى مدى احتمال تدفّق تفاعلات أيضية مختلفة وبأي اتجاه.
اختبار المنهج في أورام الكلى
لاختبار ما إذا كان spFBA يعطي نتائج منطقية بيولوجيًا، لجأت المجموعة أولاً إلى سرطان الخلايا الكلوية الشفّاف، وهو سرطان كُلوَي معروف بالاعتماد القوي على تحلل السكر (التحلل السكري) وإفراز اللاكتات، وهي ظاهرة تُعرف بتأثير واربُرغ. باستخدام بيانات مكانية منشورة من عشرة عينات أورام كلوية، تساءل الباحثون عما إذا كانت الأنماط الأيضية المتوقعة تتوافق مع البنية المعروفة للنسيج. وجدوا أن النقاط المصنفة وفق تدفقات الأيض المستنتجة اتفقت جيدًا مع التنظيم النسيجي المرئي تحت المجهر ومع العناقيد المستندة إلى تعبير الجينات وحده. ومن المهم أن spFBA استعاد التباين الأيضي المتوقع بين الورم ونسيج الكلية الطبيعي: أظهرت مناطق الورم استخدامًا أعلى للغلوكوز، وإنتاجًا أقوى للكتلة الحيوية (كمؤشر على نمو الخلايا)، وإفرازًا متينًا للاكتات. وفي الوقت نفسه، ظل استهلاك الأكسجين كبيرًا، مما يكشف أن أجزاءً مختلفة من نفس الورم يمكن أن تمزج بين التخمر والتنفس اعتمادًا على الإمداد الدموي المحلي.
سرطانات القولون والمستقيم تكشف قصة لاكتات مختلفة
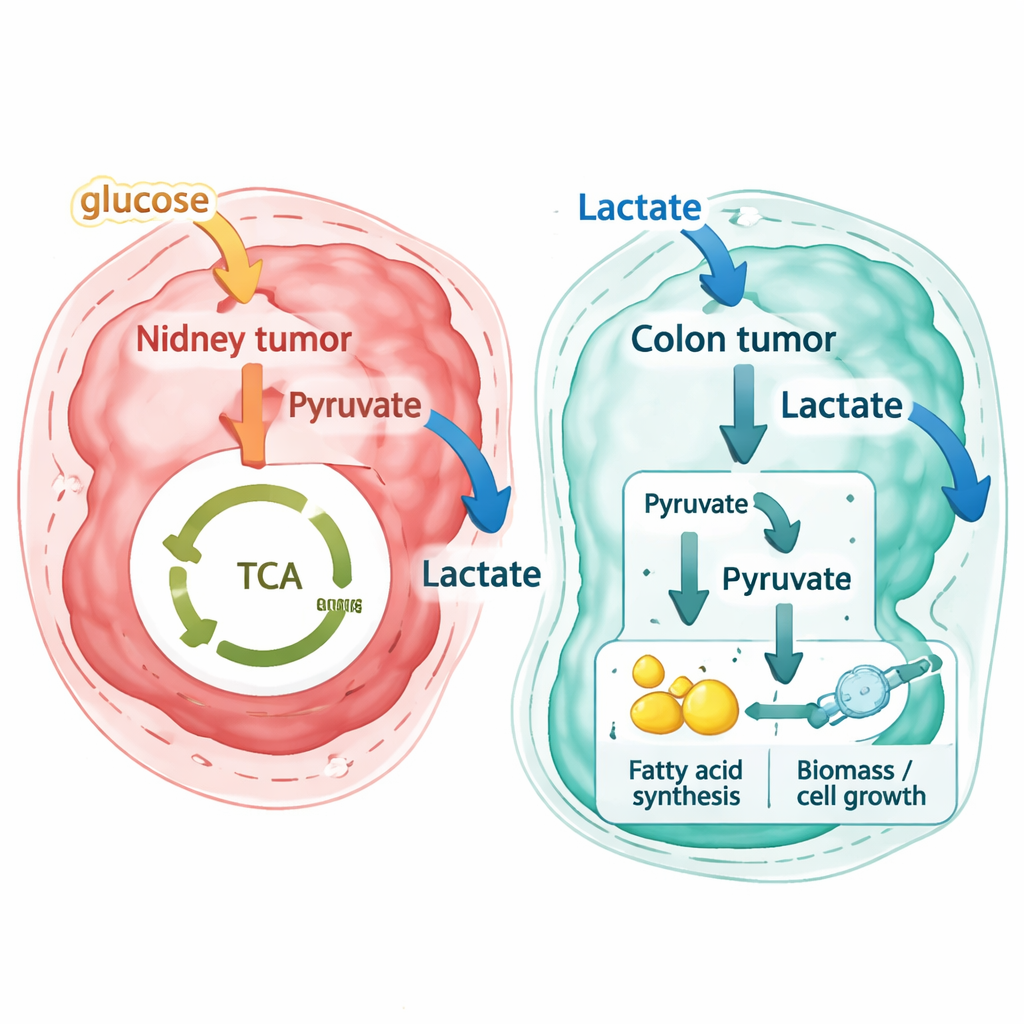
ثم طبّق الباحثون نفس المسار التحليلي على مجموعات بيانات مكانية عالية الدقة جديدة من مريض يعاني سرطان قولون أولي ونقائل كبدية متطابقة، وكذلك على مجموعة بيانات مستقلة عامة لسرطان القولون والمستقيم مولّدة بتقنية أخرى. هنا، كانت النتائج مختلفة بشكل لافت. بدلًا من تصدير اللاكتات كنفاية، كان من المتوقَّع أن تستورد معظم مناطق سرطان القولون والمستقيم—في الورم الأولي بالقولون وفي النقائل الكبدية—اللاكتات من محيطها. تميل الخلايا النسيجية الداعمة في الأنسجة المجاورة إلى إطلاق كميات صغيرة من اللاكتات، بينما تعمل خلايا الورم كمستهلك قوي. من خلال تتبع أنماط التدفق على مستوى التفاعلات، يظهر المؤلفون أن هذه الخلايا النقيلية لا تقتصر على حرق اللاكتات في دورة إنتاج الطاقة المعتادة داخل الميتوكوندريا. بل تُحوّل اللاكتات إلى لبنات بناء تدخل مسارات لصنع الدهون ومكونات أخرى مطلوبة لنمو الخلايا، وهو ما يمكن تسميته «تأثير واربُرغ العكسي الشبهّي» حيث يصبح اللاكتات مادة خام للتخليق الحيوي.
الجيوب الأيضية وحدود الورم-النسيج الداعم
لأن spFBA يحتفظ بالتخطيط المكاني، يمكنه تحديد مواقع تبادلات أيضية محددة. في أورام الكلى، كشف المنهج عن «أحياء» أيضية متعايشة: واجهات أكثر تأكسجًا وغنية بالدم حيث تتنفس الخلايا السرطانية وتخمر في آن واحد، ونُواة أعمق فقيرة الأوعية تعتمد أقوى على التخمر. في نقائل القولون بالمعدة إلى الكبد، أبرز spFBA تباينات حادة على الحدود بين الورم والنسج الداعمة، حيث تغير تعامل الجلوتامات واللاكتات اتجاهه، مما يشير إلى تبادل مكثف على الجبهة الغازية. عبر جميع مجموعات البيانات، ارتبطت التدفقات المتوقعة المتعلقة بالنمو بمقاييس مستقلة مستندة إلى الجينات للتكاثر، داعمة لواقعية النموذج البيولوجية. والأهم أن نفس الخوارزمية توقعت إفراز اللاكتات في سرطان الكلى لكن امتصاص اللاكتات في سرطان القولون والمستقيم، مما يدل على أن الاختلافات الملحوظة تنبع من البيانات لا من تحيّز مدمج في النموذج.
ما الذي يعنيه ذلك لفهم وعلاج السرطان
لغير المتخصصين، الرسالة الأساسية هي أن استقلاب السرطان ليس شذوذًا فحسب—إنه محلي للغاية أيضًا. يمكن أن يؤوي نفس الورم عدة جيوب أيضية، وقد تستعمل الأورام المتشابهة بصريًا في أعضاء مختلفة نفس الجزيئات بطرق متعاكسة. تُظهر هذه العملة أنه من خلال تغليف تعبير الجينات المكاني فوق نماذج أيضية مفصّلة، يمكن للباحثين استنتاج أماكن احتياج الأورام المغلوية لمغذيات محددة مثل اللاكتات. في سرطان القولون والمستقيم، يثير الاكتشاف بأن خلايا الورم تستهلك اللاكتات على نطاق واسع وتحوّلها إلى مسارات مرتبطة بالنمو أسئلة جديدة حول كيفية تأثير النظام الغذائي، والميكروبات المعوية، واستقلاب الكبد نفسه على تطور المرض، وما إذا كان حجب استخدام اللاكتات قد يجعل هذه الأورام أكثر عرضة للعلاج.
الاستشهاد: Maspero, D., Marteletto, G., Lapi, F. et al. Spatial FBA reveals heterogeneous Warburg niches in renal tumors and lactate consumption in colorectal cancer. npj Syst Biol Appl 12, 32 (2026). https://doi.org/10.1038/s41540-026-00654-x
الكلمات المفتاحية: استقلاب السرطان, نسخية مكانية, لاكتات, تأثير واربُرغ, سرطان القولون والمستقيم