Clear Sky Science · ar
النمذجة الحاسوبية لتحوّل بطانة القُصيّة الأمامية للوطاء نحو خلايا سلفية طلائية رئوية
تحويل الخلايا الجذعية إلى خلايا تبني الرئتين
يتعلّم العلماء كيفية إقناع خلايا المريض الجذعية بالتحول إلى نسيج رئوي بديل، ما قد يصلح في المستقبل الأضرار الناجمة عن أمراض مثل مرض الانسداد الرئوي المزمن والتليف أو العدوى الشديدة. يستعرض هذا المقال كيف استخدم الباحثون النمذجة الحاسوبية لرسم وضبط خطوة حاسمة في هذه المسيرة: تحويل نوع وسيط من الخلايا، يُسمى بطانة القُصيّة الأمامية للوطاء، إلى خلايا سلفية طلائية رئوية مبكرة — وهي الخلايا المبدئية التي يمكنها لاحقاً تكوين الممرات الهوائية وحويصلات الهواء في الرئة.
لماذا تهم خلايا البداية الرئوية
يمكن إعادة برمجة الخلايا الجذعية المحدثة ذاتياً (iPSCs) من أنسجة بالغة ثم توجيهها نحو أنسجة أجهزة مختلفة. لبناء نسيج رئوي، تمر هذه الخلايا أولاً بعدة نقاط تطورية. من بين هذه النقاط بطانة القُصيّة الأمامية للوطاء، وهي طبقة في الجنين تعطِي عادة أجزاء من الجهاز التنفسي والهضمي. منها، ومع الإشارات الكيميائية المناسبة، يمكن أن تتحول الخلايا إلى خلايا سلفية طلائية رئوية تحمِل مؤشرات رئوية مبكرة ويمكن أن تنضج لاحقاً إلى خلايا متخصصة للممرات الهوائية أو الحويصلات. وبما أن العلاجات الخلوية المستقبلية ستتطلب مليارات من هذه الخلايا، يحتاج الباحثون إلى طرق لزيادة الغلل بثقة وتكييف البروتوكولات مع خطوط خلايا مرضى مختلفة دون تجارب متكررة ولا نهائية في المختبر.
بناء نسخة افتراضية من تمايز الخلايا
وسّع الفريق إطاراً رياضياً سابقاً ليبني ما يعد، بحسب علمهم، أول نموذج على مستوى السكان لهذا الانتقال المحدد من بطانة القُصيّة إلى السلفيات الرئوية. نظروا في طريقتين لتمثيل الخلايا: نسخة مبسطة تتعقب فقط العدد الإجمالي للخلايا الحية، ونسخة أكثر تفصيلاً تتتبع خلايا القُصيّة الأمامية والسلفيات الرئوية بشكل منفصل. في كلتا الحالتين يتابع النموذج أيضاً الجلوكوز واللاكتيت في وسط الزرع، كمُمثلين للمواد المغذية والنفايات. باستخدام أدوات من بيولوجيا الأنظمة، بنى الباحثون العديد من المعادلات المرشحة لكيفية نمو الخلايا وموتها وتمايزها، ثم استخدموا اختبارات قابلية التعريف لاستبعاد النماذج التي لا يمكن ضبط معلماتها أبداً، حتى لو توفرت بيانات مثالية.
تصميم تجارب أكثر ذكاءً بمعاونة النموذج
بدلاً من ملاءمة أي بيانات متاحة فقط، ترك الباحثون للنموذج توجيه كيفية إجراء تجارب جديدة. استخدموا بيانات محاكاة لطرح سؤال كم مرة يحتاجون قياس أعداد الخلايا ومستويات المغذيات من أجل تقدير معلمات النموذج بدقة، موازنين الدقة الإحصائية مع تكلفة وجهد أخذ عينات متكرر. أدى ذلك إلى خطة عملية: قياسات يومية للجلوكوز واللاكتيت، وحسابات للخلايا كل يوم إلى يومين، تحت أربع ظروف اختلفت في مدى قسوة تقسيم الزرعات في اليوم العاشر وما إذا كان يتم تجديد وسط النمو يومياً. ثم نفّذوا هذه التجارب، مقيسين كل من إجمالي عدد الخلايا وبواسطة التألق الخيطي (flow cytometry) نسب الخلايا التي بقيت قُصية أو تحولت إلى سلفيات رئوية.
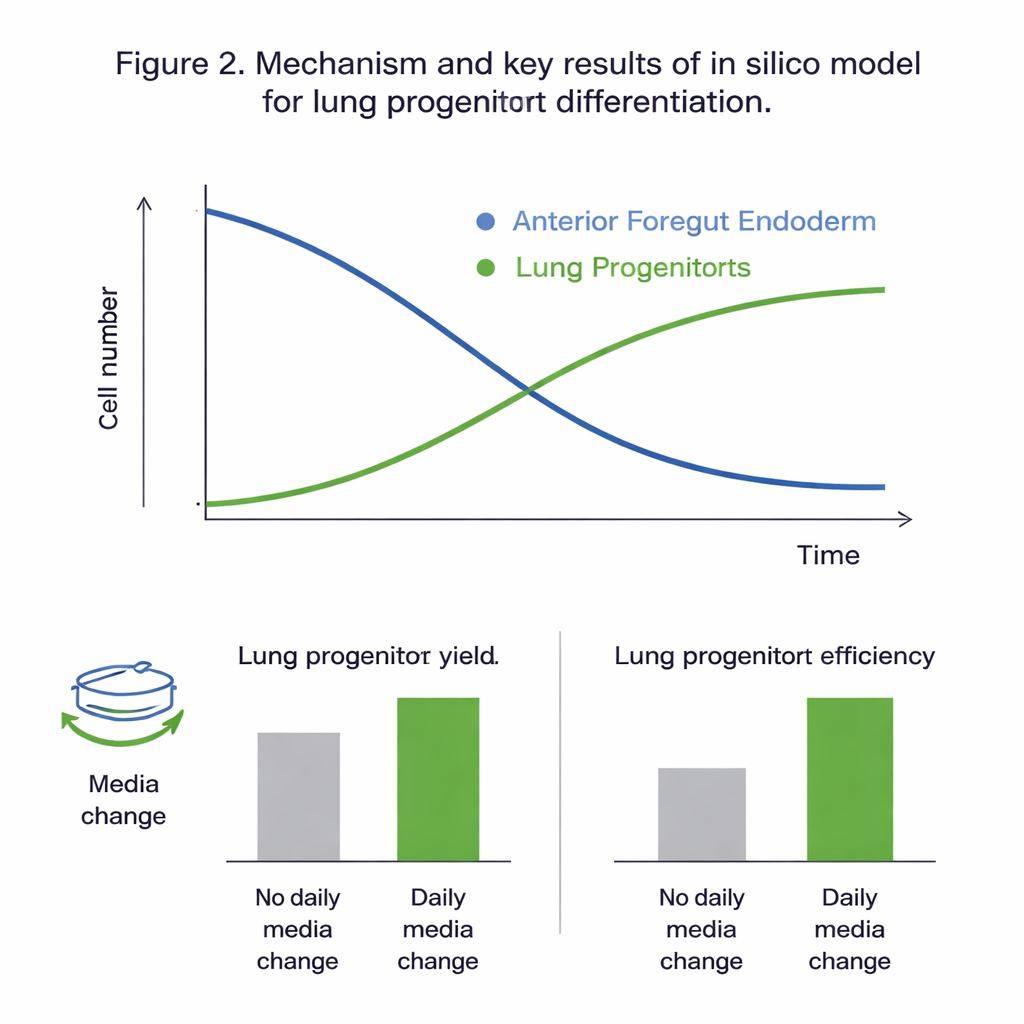
ما كشفته التجارب الافتراضية
أظهرت ملاءمة جميع النماذج المرشحة مع بيانات التجربة أن نموذج السكان الثنائي، الذي يتتبع خلايا القُصيّة والسلفيات الرئوية بشكل منفصل، يمكن معايرته بثبات ووصف السلوك المرصود على نحو أفضل. أشارت الفحوص الإحصائية إلى أنه خلال الفترة الزمنية المدروسة (الأيام 11 إلى 15 من البروتوكول)، كانت الديناميكيات مدفوعة بشكل رئيسي بتكاثر وتمايز خلايا القُصيّة، بينما كان لتكاثر السلفيات الرئوية نفسها إسهام ضئيل. عزز التحليل الحساس العالمي هذه الصورة، مبرزاً معدلات نمو وموت وتمايز خلايا القُصيّة — وتأثير الجلوكوز — كالمقابض الرئيسية التي تتحكم في النتيجة. أعاد النموذج المعاير بيانات لم تُستخدم في المعايرة بدقة أخطاء مقاربة للتفاوت الطبيعي للتجارب، مما يقترح أنه دقيق بما يكفي لاستكشاف سيناريوهات «ماذا لو» حاسوبياً.
تحسين تغييرات الوسط وتقسيم الخلايا
مع وجود نظام افتراضي موثوق، اختبر الفريق كيف تؤثر خياران عمليان في البروتوكول على النتائج: مدى تخفيف الزرع (نسبة التقسيم) في اليوم العاشر، وما إذا كان يتم استبدال وسط النمو يومياً. تنبأت المحاكاة بأن التغييرات اليومية للوسط تقربياً تضاعف عدد خلايا السلفية الرئوية والعائد لكل خلية بداية، وذلك أساساً بمنع نفاد المغذيات وتراكم النفايات والجزيئات الإشارية غير المستقرة. واتفقت التجارب بشكل وثيق مع هذه التنبؤات. كما أوضح النموذج أن استخدام نسب تقسيم أعلى — أي نشر الخلايا أرق في اليوم العاشر — يحسّن «العائد لكل خلية مدخلة» بنحو ربع، رغم أنه يقلل العدد المطلق للخلايا. في كلتا الحالتين، كان لتلك التغييرات تأثير طفيف على النسبة النهائية للسلفيات الرئوية داخل الزرع، إذ غيرت أساساً عدد الخلايا الممكن إنتاجه بكفاءة.
ماذا يعني هذا لعلاجات الرئة المستقبلية
لغير المتخصص، الرسالة الأساسية هي أن المؤلفين بنوا نوعاً من محاكي الطيران لخطوة حرجة في نمو خلايا الرئة من الخلايا الجذعية. من خلال الجمع بين تجارب مصممة بعناية ونمذجة رياضية صارمة، يوضحون كيف أن اختيارات بسيطة في البروتوكول — مثل تكرار تغيير وسط الزرع وكثافة زرع الخلايا — يمكن أن تؤثر بشكل كبير على عدد خلايا بناء الرئة المنتجة، دون أن تغير جودتها. يمكن لهذا النوع من النمذجة الحاسوبية أن يساعد في تبسيط البروتوكولات المستقبلية، وتقليل التكهنات التجريبية، ودعم إنتاج أكثر موثوقية وقابلاً للتوسع للخلايا السلفية الرئوية للبحث، ونمذجة الأمراض، وفي نهاية المطاف العلاجات التجديدية.
الاستشهاد: Mostofinejad, A., Romero, D.A., Brinson, D. et al. In silico modeling of anterior foregut endoderm differentiation towards lung epithelial progenitors. npj Syst Biol Appl 12, 29 (2026). https://doi.org/10.1038/s41540-026-00650-1
الكلمات المفتاحية: خلايا السلف الرئوية, الخلايا الجذعية المحدثة ذاتياً, النمذجة الحاسوبية, تمايز الخلايا, الطب التجديدي