Clear Sky Science · ar
ارتباط تغيرات عدد النسخ بالمشهد النسخي المناعي في السرطان
لماذا جيناتنا مهمة للعلاج المناعي للسرطان
يعمل العلاج المناعي للسرطان عن طريق مساعدة الجهاز المناعي على التعرف على الأورام ومهاجمتها، لكن عددًا قليلاً فقط من المرضى يحققون فائدة دائمة. تطرح هذه الدراسة سؤالًا أساسيًا ذو عواقب سريرية كبيرة: كيف يشكل الفوضى الجينية داخل خلايا الورم — وبالأخص الكسب والخسارة الواسعة للحمض النووي المعروفة بتغيرات عدد النسخ — رد الفعل المناعي ضد السرطان، وهل يمكننا قراءة تلك التأثيرات من أنماط نشاط الجينات؟
نظرة بانورامية على بيانات السرطان
لمعالجة هذا السؤال، جمع الباحثون مجموعة ضخمة مكونة من 294,159 ملفًا لنشاط الجينات من أورام وأنسجة أخرى. تلتقط هذه الملفات، المستمدة من عدة قواعد بيانات عامة رئيسية، الجينات التي تكون مفعلة أو مكبوتة في آلاف العينات التي تغطي أنواع سرطانات وظروف تجريبية متعددة. بدلًا من فحص جين واحد تلو الآخر، استخدم الفريق طريقة رياضية لتفكيك كل ملف إلى «مكونات» أساسية — أنماط متكررة من الجينات تميل إلى الارتفاع والانخفاض معًا، كل منها يعكس عملية بيولوجية مثل استجابة مناعية أو أثر تغيير في الحمض النووي.
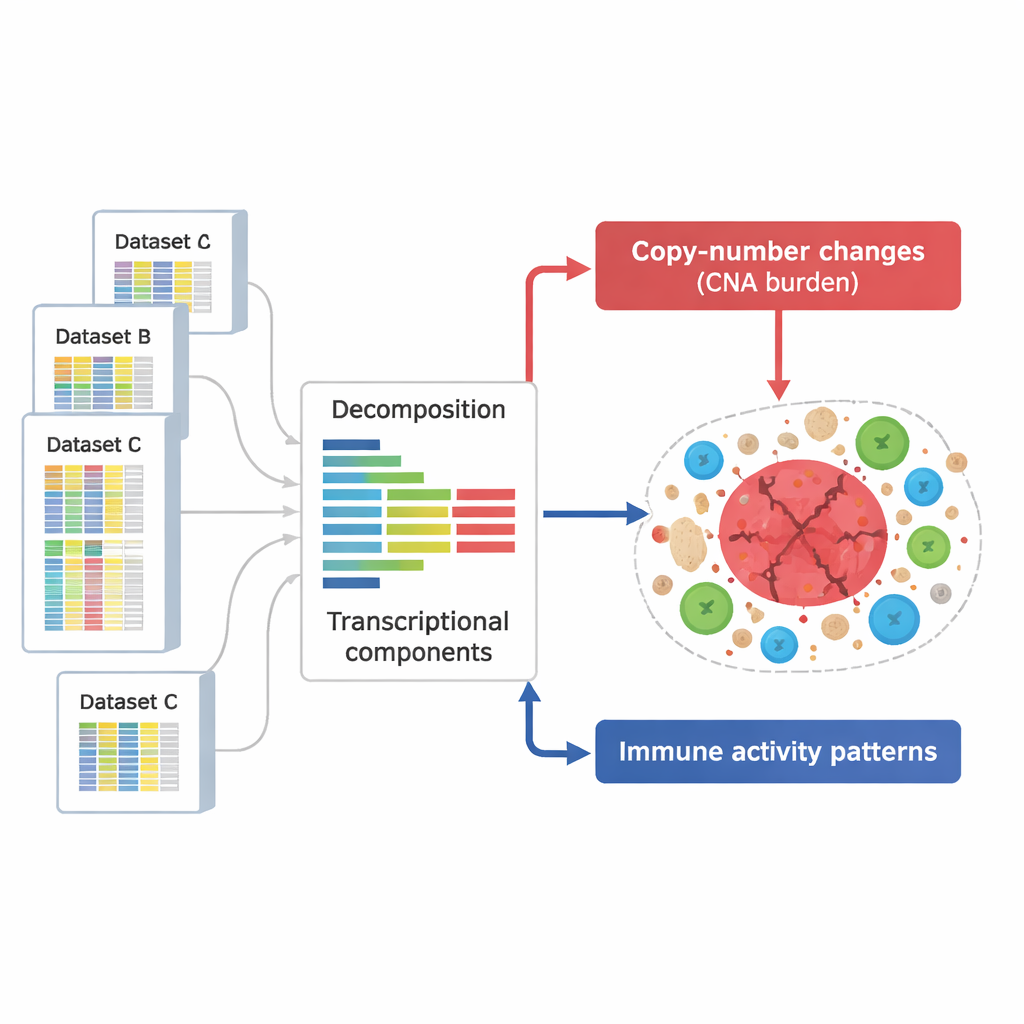
فصل إشارات تلف الحمض النووي عن إشارات المناعة
من هذه المكونات، عرّف العلماء مجموعتين رئيسيتين. سجلت مجموعة واحدة آثار تغيرات عدد النسخ — مقاطع من الكروموسومات تُكتسب أو تُفقد بشكل متكرر في خلايا السرطان. غطت هذه الأنماط تقريبًا كامل الجينوم، ما يشير إلى أن معظم المناطق المتأثرة بهذه التغيرات تترك بصمة قابلة للاكتشاف على نشاط الجينات. أما المجموعة الثانية فكانت غنية بجينات مشاركة في وظائف مناعية، مثل تفعيل الخلايا التائية، ونشاط الخلايا القاتلة الطبيعية، وعرض المستضدات. في المجمل، حدّدوا 657 مكوّنًا مرتبطًا بالحمض النووي و283 مكوّنًا مرتبطًا بالمناعة، ويمكن رؤية العديد منها بشكل متكرر عبر مجموعات بيانات وتقنيات مستقلة، مما يشير إلى أنها تمثل سمات متينة وعامة لبيولوجيا الورم.
ربط الأنماط بالاستجابة للعلاج
بعد ذلك تساءل الفريق عما إذا كانت هذه الأنماط المرتبطة بالمناعة يمكن أن تساعد في التنبؤ بمن يستجيب لمثبطات نقاط التفتيش المناعية، وهي فئة رئيسية من أدوية العلاج المناعي للسرطان. باستخدام بيانات من 13 دراسة سريرية شملت 1,167 مريضًا بسبعة أنواع من السرطان، درّبوا نماذج حاسوبية لتمييز المستجيبين من غير المستجيبين اعتمادًا فقط على نشاط المكونات المناعية في عينات الورم قبل العلاج. أظهرت بعض النماذج أداءً قويًا حتى عند اختبارها على مجموعات مرضى مستقلة تمامًا؛ على سبيل المثال، نموذج مدرّب على مجموعة سرطان ثدي واحد تنبأ بدقة بالاستجابات في مجموعة ثدي منفصلة وأظهر أداءً مفيدًا في عدة سرطانات أخرى. ساهمت مجموعة صغيرة من الأنماط المناعية، بما في ذلك الأنماط المرتبطة باستجابات الإنترفيرون، والخلايا القاتلة الطبيعية، وتفعيل الخلايا التائية، بأكبر قدر في هذه التنبؤات.
كيف تعيد الفوضى الجينية تشكيل مناعة الورم
بناءً على هذا الإطار، ربط الباحثون بشكل منهجي عبء تغيرات عدد النسخ الكلي — وهو مقياس لمدى اكتساب أو فقدان الحمض النووي في الورم — بنشاط كل نمط مناعي عبر أنواع سرطان متعددة. أظهرت معظم الأنماط المناعية علاقة عكسية: كانت الأورام ذات العبء العالي من تغيرات الحمض النووي تميل إلى انخفاض نشاط المكونات المرتبطة بوظائف مناعية مفيدة، مثل عرض المستضدات وتسلل الخلايا المناعية الرئيسية. ومع ذلك، تحركت أقلية ملحوظة من الأنماط بالاتجاه المعاكس. غالبًا ما كانت الأورام ذات العبء العالي تُظهر إشارات متزايدة من أنواع خلوية مُثبطة للمناعة، بما في ذلك الخلايا التائية المنظمة وبعض الخلايا البلعمية، بالإضافة إلى خلايا التهابية يمكن أن تعزز نمو الورم بدلاً من تدميره. أكدت تحليلات مكانية لشرائح الورم أن المناطق ذات التغيرات الجينية الكثيفة كثيرًا ما توافقت مع انخفاض نشاط الأنماط المناعية المفيدة ومع مناطق «مستبعدة مناعيًا» حيث حُصرت الخلايا المناعية عند حواف الورم.
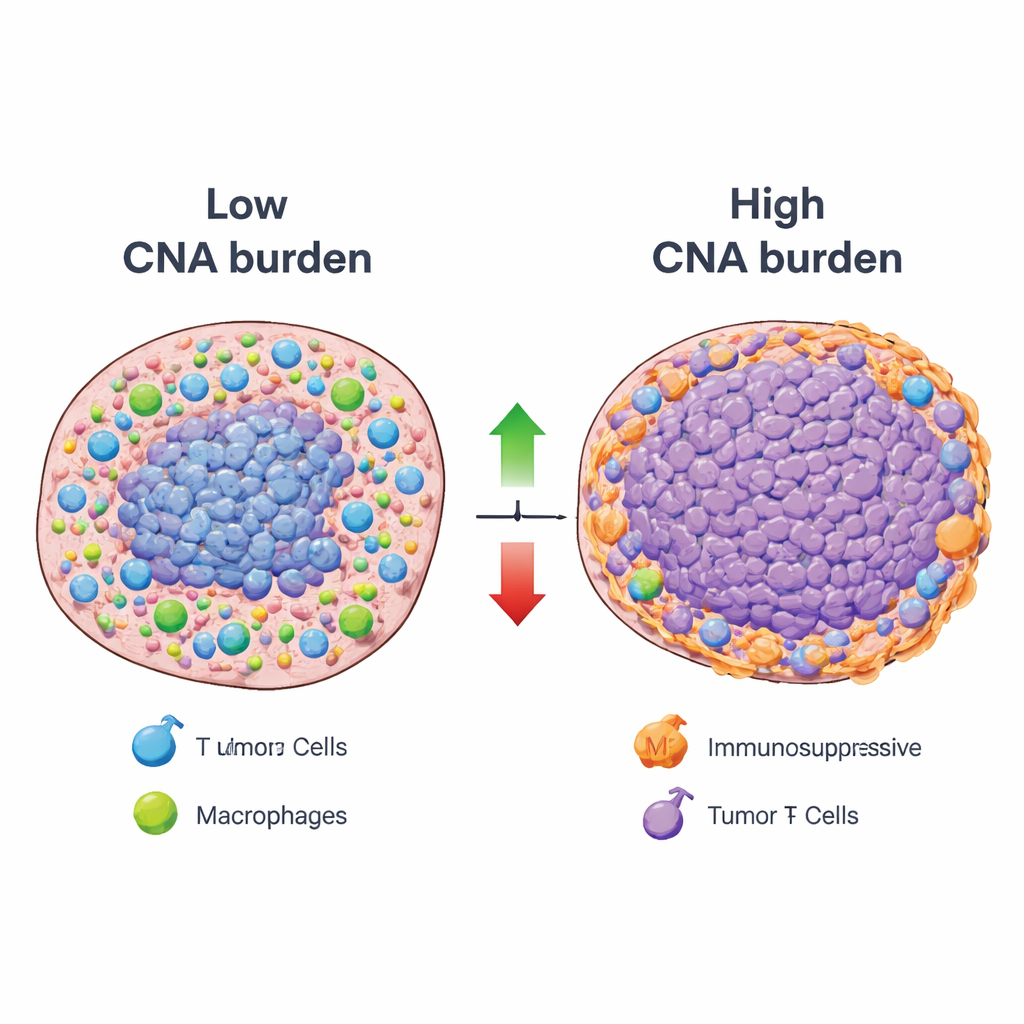
ما الذي يعنيه هذا لعلاج السرطان في المستقبل
بعبارات بسيطة، تُظهر الدراسة أن الأورام المثقلة بكسب وخسارة الحمض النووي على نطاق واسع تميل إلى كبت الاستجابات المناعية المفيدة وفي الوقت نفسه تهيئة بيئات مناعية مثبطة أو منشطة للورم. ومع ذلك، فهي ليست صامتة مناعيًا؛ بل تعرض حالات مناعية محددة ومتكررة قد تكون قابلة للاهداف العلاجية، مثل أدوية تحجب إشارة IL-17 أو IL-23 أو استراتيجيات تعيد برمجة أنواع معينة من الخلايا البلعمية. من خلال رسم هذه العلاقات بين الحمض النووي والمناعة عبر السرطانات وإتاحة المورد للعلن، يقدم العمل دليلًا مفصلًا لسبب مقاومة بعض الأورام غير المستقرة جينيًا للعلاجات المناعية الحالية ويقترح استراتيجيات علاجية تركيبية جديدة لمساعدة الجهاز المناعي على التغلب على هذه المقاومة.
الاستشهاد: Loipfinger, S., Bhattacharya, A., Urzúa-Traslaviña, C.G. et al. Association of copy number alterations with the immune transcriptomic landscape in cancer. npj Syst Biol Appl 12, 28 (2026). https://doi.org/10.1038/s41540-026-00649-8
الكلمات المفتاحية: العلاج المناعي للسرطان, تغيرات عدد النسخ, البيئة الميكروية للورم, مثبطات نقاط التفتيش المناعية, تحليل النسخ