Clear Sky Science · ar
الاستدلال القائم على المحاكاة لديناميكيات هجرة الخلايا في بيئات مكانية معقدة
كيف تجد خلايا الجهاز المناعي طريقها عبر أنسجة مكتظة
غالبًا ما تضطر خلايا جهازنا المناعي إلى الانضغاط عبر أنسجة كثيفة تشبه المتاهة للوصول إلى مواقع العدوى أو العقد اللمفاوية. يطرح هذا الدراسة سؤالًا يبدو بسيطًا لكنه ذو آثار كبيرة: كيف تتنقل هذه الخلايا في بيئات مزدحمة، وكيف يمكننا استنتاج سلوكياتها بثقة من بيانات المجهر الفوضوية؟ من خلال دمج “متاهات” مخبرية مصممة بدقة مع محاكيات حاسوبية متقدمة وأدوات تعلم آلي حديثة، يعرض المؤلفون طريقة جديدة لفك شفرة القواعد التي توجه حركة الخلايا في محيطات معقدة.
بناء متاهة صغيرة لخلايا الجهاز المناعي
لفحص كيف يشكل المحيط الحركة، ركز الباحثون على الخلايا التغصُّنية — الحراس المناعيون الذين يجب أن ينتقلوا من الأنسجة الطرفية إلى العقد اللمفاوية، موجهين بواسطة عوامل جذب كيميائية تُدعى الكيمياء الخلوية. بنوا شريحة ميكروصُنعت: «غابة أعمدة» مسطحة من أعمدة متباعدة بانتظام مصنوعة من مطاط السيليكون (PDMS)، مع فجوات ضيقة بعرض 10 ميكرومترات تحاكي المساحات الضيقة في الأنسجة الحقيقية. تمت تعبئة جانب واحد من الشريحة بعشرات الآلاف من الخلايا التغصُّنية؛ والجانب المقابل احتوى مصدرًا للكيموكين CCL19، الذي يخلق تدرجًا ثابتًا عبر الأعمدة. وباستخدام ميكروسكوب زمني متتابع، تتبعوا نوى الخلايا الفردية كل 30 ثانية أثناء محاولتها التحرك نحو مصدر الكيموكين. 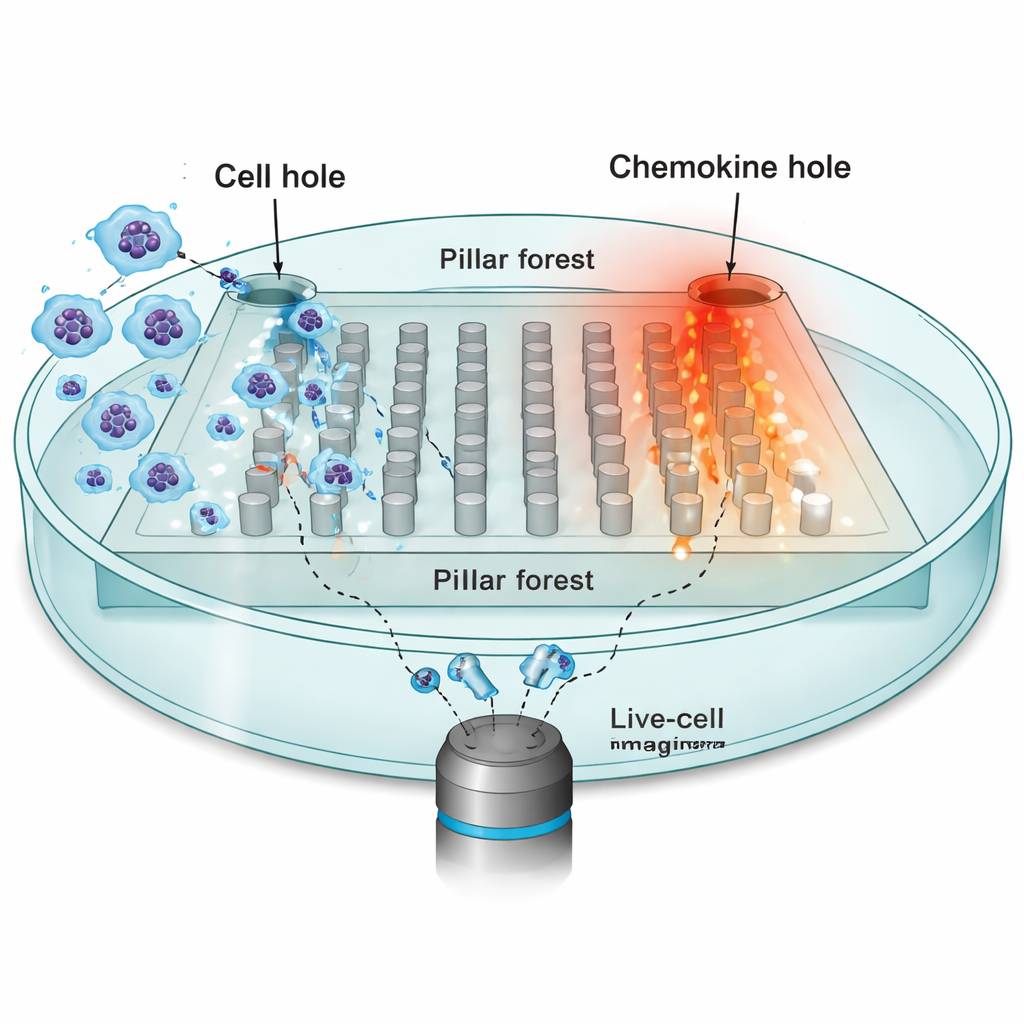
تحويل البيولوجيا إلى تجربة افتراضية
لفهم هذا التنوع، بنى الفريق نموذجًا حاسوبيًا مفصلاً لهجرة الخلايا باستخدام إطار عمل يُعرف بنموذج بوتز الخلوي (Cellular Potts model). بدلاً من تمثيل الخلية كنقطة بسيطة، يمثل هذا النهج كل خلية كبقعة ممتدة على شبكة، مما يسمح لها بتغيير الشكل، والانضغاط بين الأعمدة، والاستجابة للإشارات الكيميائية. يشمل النموذج أربعة مكونات رئيسية: مدى قوة انجذاب الخلية لتدرج الكيموكين (mdir)، مدى ميلها للثبات في اتجاه حركتها الحالي (mrand)، تواتر إعادة توجيهها (يمثله معدل λ)، وحجمها الفعلي (a). عن طريق ضبط هذه المعاملات وتشغيل المحاكاة، ينتج النموذج مسارات اصطناعية يمكن مقارنتها مباشرة بالمسارات المسجلة للخلايا في غابة الأعمدة.
لماذا تقيسات اليد تفشل أحيانًا
تقليديًا، يلخّص الباحثون بيانات الحركة هذه بمجموعة من الإحصاءات المألوفة — كم تقطع الخلية من مسافة (الإزاحة)، مدى سرعتها (السرعة)، وكيف يتغير اتجاهها مع الزمن (زوايا الالتفاف). استخدم المؤلفون أولًا هذه المقاييس المصممة يدويًا ضمن تقنية تسمى الحساب البايزي التقريبي (ABC)، التي تبحث عن مجموعات معاملات تجعل المسارات المحاكية تشبه التجريبية. وجدوا أن هذه الملخصات تلتقط الاتجاهات العامة، لكنها تفقد الكثير من البنية الدقيقة في البيانات. ونتيجة لذلك، ظل بعض معاملات النموذج، خصوصًا تلك المرتبطة بالثبات العشوائي وتوقيت إعادة التوجيه، غير محددة جيدًا أو حتى متحيزة. علاوة على ذلك، تطلبت ABC مئات الآلاف من المحاكاة وساعات عديدة من الحساب للوصول إلى تطابقات مقبولة.
سماح الشبكات العصبية بتعلّم ما يهم
لتجاوز هذه الحدود، لجأت الدراسة إلى عائلة أحدث من الأساليب تسمى تقدير الخلفية العصبي (NPE). هنا، تُدرّب شبكة عصبية مباشرة على أزواج كثيرة من البيانات المحاكاة والمعاملات الأساسية. جزء من الشبكة يتعلم تلقائيًا مجموعة مدمجة من «الملخصات» من مجموعات كاملة من مسارات الخلايا؛ وجزء آخر يتعلم كيف تُرجع تلك الملخصات إلى قيم المعاملات المحتملة. والأهم أن هذه الملخصات المتعلّمة مُحسّنة صراحة لاستدلال المعاملات بدقة، لا للتفسير البشري. أعاد المؤلفون بعد ذلك استخدام الملخصات المتعلّمة داخل إطار ABC، فخلقوا أنبوبًا هجينًا يجمع بين متانة ABC ومرونة الشبكات العصبية. 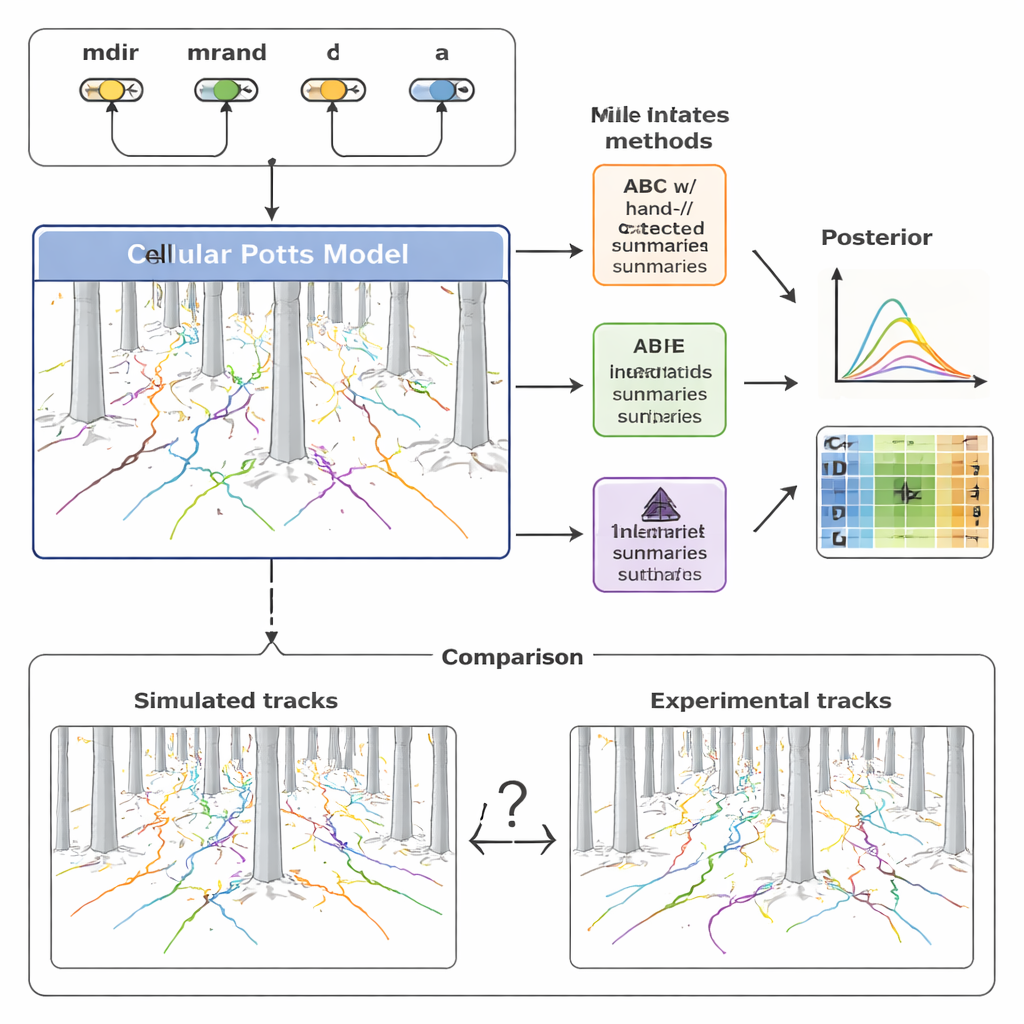
ما تكشفه المقاربة الجديدة عن توجيه الخلايا
مسلحين بهذا النموذج المعاير، استكشف الباحثون كيف تشكّل إشارات الكيموكين والعقبات الفيزيائية معًا الهجرة. أشار الحجم المستنتج للخلية إلى أن الخلايا التغصُّنية تنكمش وتتشوه بشكل فعال لتلائم الفجوات ذات العرض 10 ميكرومترات، متوافقًا مع مرونتها المعروفة. أشارت المحاكاة إلى أن الحركة العشوائية المستمرة هي عامل رئيسي في مدى انتشار الخلايا، حتى بدون توجيه كيموكيني، وأن غابة الأعمدة يمكن أن تحاصر الخلايا عندما تعمل إشارات الاتجاه القوية مع الثبات معًا. بشكل مفاجئ، يتنبأ النموذج أن إشارة كيموكين تكون نشطة لفترة وجيزة في وقت مبكر قد تساعد في بعض الحالات المزيد من الخلايا على الوصول إلى الهدف أكثر من إشارة ثابتة، لأن الجذب المستمر قد يبقي الخلايا تدور داخل العقبات بدلًا من الهروب منها.
لماذا هذا مهم للبيولوجيا والنمذجة
لغير المتخصصين، الرسالة الأساسية في جانبين. أولًا، هجرة خلايا المناعة في الأنسجة ليست مجرد تتبع أثر كيميائي؛ بل تنشأ من تداخل دقيق بين إشارات التوجيه، اتجاهات الحركة الذاتية للخلايا، والتخطيط الفيزيائي للمحيط. ثانيًا، استخراج هذه القواعد من بيانات التصوير يتطلب السماح للحاسوب بتعلّم أي الأنماط في البيانات هي الأكثر معلوماتية، بدلًا من الاعتماد حصريًا على مقاييس بسيطة مصممة من قبل البشر. من خلال دمج تجارب ميكرومهندسة، ومحاكاة تحترم الشكل، واستدلال قائم على الشبكات العصبية، يقدم هذا العمل قالبًا قويًا لدراسة كيفية تحرك أنواع عديدة من الخلايا عبر بيئات معقدة، مع تطبيقات محتملة تتراوح من فهم مراقبة المناعة إلى تصميم علاجات سرطان أفضل.
الاستشهاد: Arruda, J., Alamoudi, E., Mueller, R. et al. Simulation-based inference of cell migration dynamics in complex spatial environments. npj Syst Biol Appl 12, 20 (2026). https://doi.org/10.1038/s41540-026-00648-9
الكلمات المفتاحية: هجرة الخلايا, الخلايا التغصُّنية, تدرجات الكيمياء الخلوية, الاستدلال القائم على المحاكاة, غابات الأعمدة الميكروفلويدية