Clear Sky Science · ar
السيطرة المتأثرة بالربو على نمو ورم الغُليوما البصري عبر تفاعلات الخلايا التائية والميكروغليا: نموذج رياضي
عندما تتقاطع مشكلات التنفس مع أورام الدماغ
يبدو الربو وأورام الدماغ بعيدان عن بعضهما: أحدهما يؤثر على كيفية تنفسنا، والآخر على الرؤية والتفكير والحركة. ومع ذلك لاحظ الأطباء نمطًا محيرًا — الأطفال المصابون بالربو قد يكونون أقل عرضة لتطوير أنواع معينة من أورام العصب البصري. يستعرض هذا المقال كيف قد تدافع حالة رئوية مزمنة عن الدماغ بطرق غير متوقعة، مستخدمًا نموذجًا رياضيًا لتتبع المحادثات الكيميائية الخفية بين خلايا المناعة وخلايا الورم.
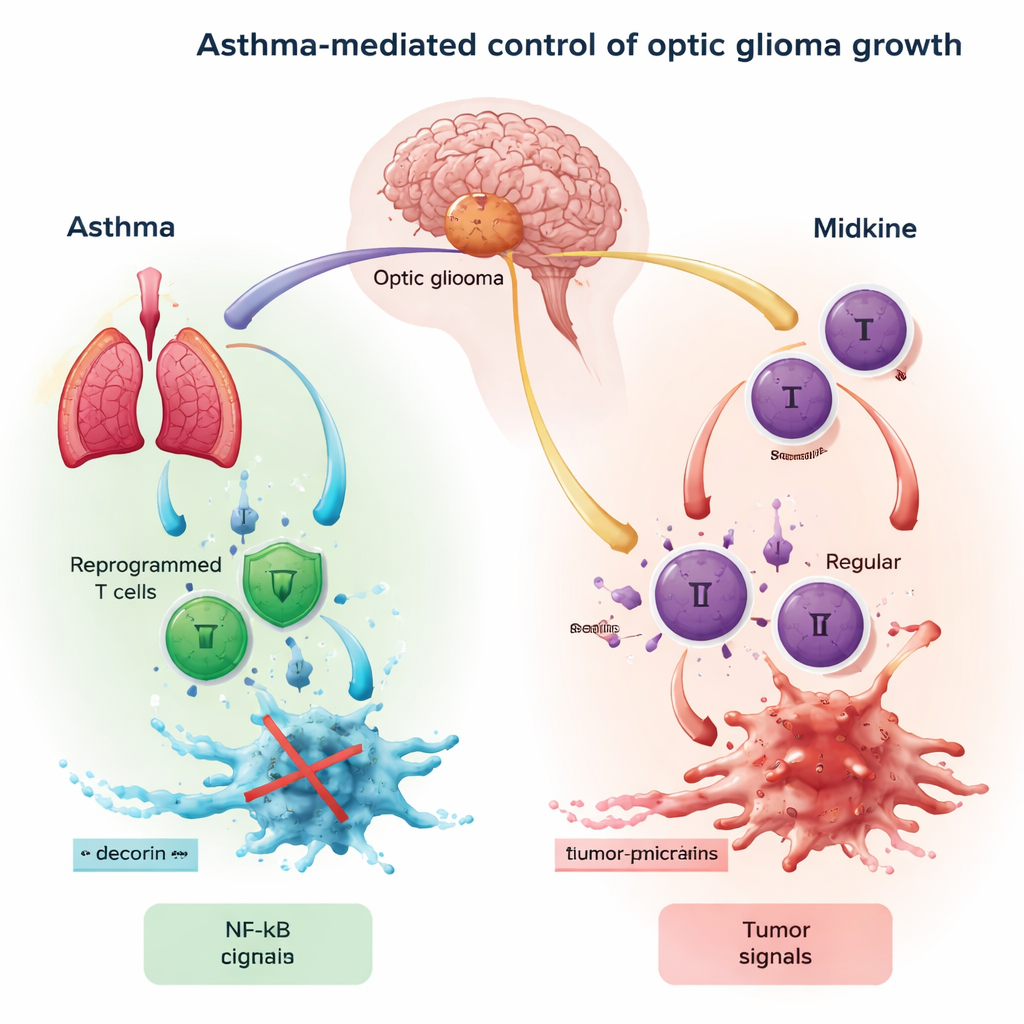
ورم بطيء النمو لكنه ذا تبعات كبيرة
تُعد أورام الغُليوما البصرية عادة أورامًا بطيئة النمو تتشكل على طول العصب البصري، وغالبًا لدى الأطفال المصابين بحالة وراثية تُسمى الورم العصبي الليفي من النوع الأول (NF1). وعلى الرغم من أن هذه الأورام تُصنَّف على أنها «منخفضة الدرجة»، إلا أنها قد تسبب فقدان الرؤية ومشكلات هرمونية. في NF1، يؤدي خلل جيني إلى فرط نشاط بروتين إشارة يدعى RAS. هذا النشاط الزائد يحفز إنتاج جزيء آخر، الميدكاين، الذي يعمل كأنبوب نداء في العصب البصري، يستقطب خلايا المناعة ويعيد تشكيل البيئة المحلية بطرق عادةً ما تفيد الورم بدلاً من محاربته.
حوار يغذي الورم بين الخلايا العصبية والمناعية
يركز المؤلفون على سلسلة أحداث تربط العصب البصري وخلايا المناعة ونمو الورم. الميدكاين القادم من العصب البصري يفعّل أولًا الخلايا التائية، وهي نوع من خلايا الدم البيضاء، فيدفعها لإفراز إشارة تُدعى CCL4. ترتبط هذه الإشارة بعد ذلك بمستقبلات (CCR5 وCCR8) على الميكروغليا، وهي خلايا المناعة المقيمة في الدماغ. عندما يرتبط ما يكفي من CCL4 بهذه المستقبلات، يُشغل ذلك مفتاحًا رئيسيًا داخل الميكروغليا يُعرف باسم NF-κB. بمجرد تفعيله، يدفع NF-κB إنتاج إشارة أخرى، CCL5، التي تشجع خلايا غُليوما العصب البصري على النمو والهجرة وتفادي الهجوم المناعي. عمليًا، يشكل محور الميدكاين–CCL4–NF-κB–CCL5 إشارة «انطلاق» دائرية لتوسع الورم.
كيف يعيد الربو برمجة الخلايا التائية لتقييد الورم
الربو معروف في المقام الأول كمرض التهابي مزمن للممرات الهوائية. لكن في الأشخاص المصابين بالربو، تُعاد برمجة بعض الخلايا التائية إلى حالة مختلفة: تفقد الكثير من قوتها القاتلة المباشرة للخلايا وبدلًا من ذلك تفرز جزيئات تعيد تشكيل محيطها. أحد هذه الجزيئات هو الديكورين، بروتين صغير معروف بخصائصه المضادة للأورام. الفكرة الأساسية في هذا العمل هي أن الخلايا التائية المشكَّلة بالربو يمكن أن تنتقل من الرئة إلى الدماغ وتفرز الديكورين في محيط ورم الغُليوما البصري. يتنافس الديكورين مع CCL4 على مستقبل CCR8 في الميكروغليا، مما يعيق فعليًا جزءًا من حوار تغذية الورم ويخفض نشاط NF-κB وCCL5 داخل خلايا المناعة الدماغية.
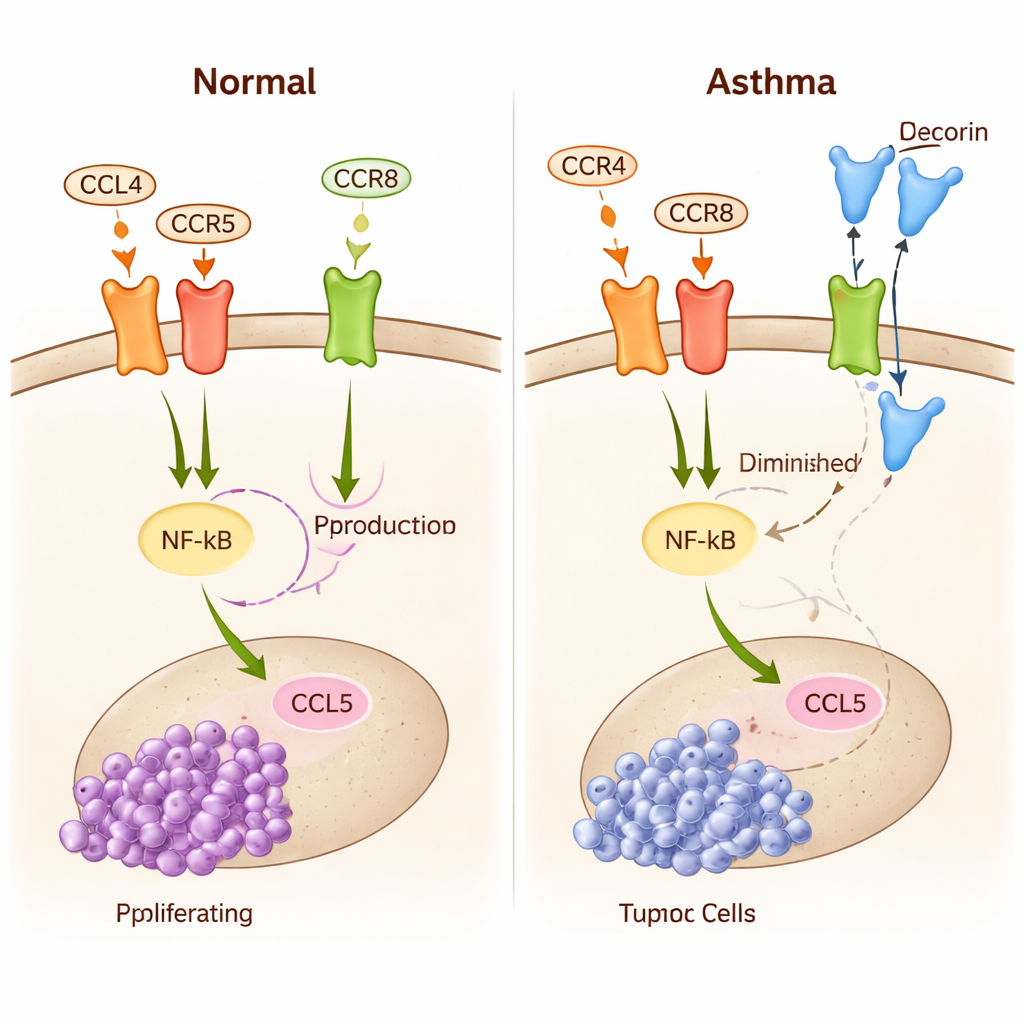
استخدام الرياضيات لتتبع شبكة غير مرئية
نظرًا لأن شبكة الإشارات هذه معقدة جدًا بحيث لا يمكن استيعابها بالحدس وحده، بنى الباحثون نموذجًا رياضيًا مفصلاً باستخدام المعادلات التفاضلية. يتتبع النموذج مستويات الجزيئات الأساسية (الميدكاين، CCL4، الديكورين، NF-κB، CCL5)، نشاط المستقبلات على الميكروغليا، ونمو خلايا الورم عبر الزمن. استخدموا بيانات تجريبية لمعايرة قوة كل تفاعل ثم قاموا بمحاكاة سيناريوهات متعددة. يبيّن النموذج كيف أنّ تغييرات بسيطة في قوة الارتباط — مدى سهولة ارتباط CCL4 أو الديكورين بمستقبلاتهما — يمكن أن تقلب حالة الميكروغليا بين نمطين: حالة محفزة للورم مع NF-κB وCCL5 عاليتين، وحالة مكبِّحة للورم مع ارتباط قوي للديكورين وإشارات CCL4 ضعيفة. مؤشر بسيط قائم على نسبة المستقبلات المرتبطة بالديكورين إلى تلك المرتبطة بـCCL4 يتنبأ بدقة بما إذا كان الورم سيميل إلى النمو أم التوقف.
تصميم علاجات مناعية أكثر ذكاءً
بعيدًا عن تفسير سبب قداسة حماية الربو ضد ورم الغُليوما البصري، يُستخدم النموذج أيضًا لاستكشاف استراتيجيات العلاج. يقترح أن العلاجات التي تعزز مستويات الديكورين أو تُضعف قبضة CCL4 على مستقبلاته قد تُبطئ نمو الورم. اختبر المؤلفون رقميًا مقاربات مثل ضخّ خلايا تائية منتجة للديكورين بشكل متكرر أو استخدام رسول مناعي مثل IL-2 لتوسيع هذه الخلايا المفيدة داخل الجسم. ومن المثير للاهتمام أن المحاكاة تكشف أن ليس الجرعة الكلية فحسب هي المهمة، بل توقيت تلك العلاجات أيضاً: يمكن للجرعات المعتدلة الموزعة جيدًا أن تحافظ على الميكروغليا في الحالة المانعة للورم بفعالية مشابهة لجرعات أكبر وأقل تكرارًا، مع آثار جانبية محتملة أقل.
ماذا يعني هذا للمرضى والأسر
لغير المتخصصين، الرسالة الأساسية هي أن الالتهاب المزمن في الربو، الذي يُنظر إليه عادةً على أنه ضار، يمكن أن يُعيد تشكيل الجهاز المناعي بطرق تعيق أحيانًا بعض أورام الدماغ. عبر تحويل الخلايا التائية إلى مصانع للديكورين، يبدو أن الربو يُزِن الميزان في العصب البصري نحو بيئة أقل ملاءمة للنمو السرطاني. لا يقترح أحد استخدام الربو كعلاج، لكن الآليات المكتشفة هنا قد تُلهم علاجات جديدة تُقلد جوانب الحماية تلك — باستخدام علاجات خلوية تائية موجهة أو أدوية تحاكي تأثير الديكورين في الحجب — لحماية الأطفال المعرضين لخطر ورم الغُليوما البصري.
الاستشهاد: Lee, D., Lawler, S. & Kim, Y. Asthma-mediated control of optic glioma growth via T cell-microglia interactions: A mathematical model. npj Syst Biol Appl 12, 26 (2026). https://doi.org/10.1038/s41540-026-00647-w
الكلمات المفتاحية: ورم الغُليوما البصري, الربو, ديكورين, الخلايا التائية, النمذجة الرياضية