Clear Sky Science · ar
خريطة الإحساس بالشّم تتعرّض للاضطراب في نموذج فأريّ معدل وراثيًا يفرط في تعبير ألفا-سينوكلين البشري والنّوِع البري لمرض باركنسون
لماذا خسارة الشم مهمة في باركنسون
يفكر كثير من الناس في مرض باركنسون كاضطراب حركي، لكن لدى معظم المرضى تكون أول وظيفة تتعطّل هي حاسة الشم. قد تظهر هذه الخسارة قبل عقود من ظهور الرعشة أو الصلابة، ما يجعلها علامة إنذار مبكّرة قوية. تطرح الدراسة الموصوفة هنا سؤالًا أساسيًا لم يُجب بعد: ما الذي ينهار بالضبط في دوائر الشم في الدماغ عندما تبدأ التغيّرات المتعلقة بباركنسون؟ من خلال فحص هذا السؤال في نموذج فأري مصمّم بعناية، يكشف الباحثون كيف يزعج بروتين رئيسي مرتبط بباركنسون "خريطة الشم" الداخلية في الدماغ ويشيرون إلى مصدر جديد وسهل الوصول لإشارات مبكرة للمرض.
خريطة الشم في الدماغ
تحوي أنوفنا ملايين الخلايا المتخصّصة بالشم التي تستجيب كلّ منها لجزيئات رائحة معيّنة. ترسل هذه الخلايا أليافًا طويلة رفيعة إلى مقدّمة الدماغ، حيث تتلاقى في مراكز صغيرة تُسمّى العُقيدات الشمّية داخل البُصيلة الشمّية. يُفعّل كل نوع من الروائح نمطًا محددًا من هذه العُقيدات، مكوّنًا خريطة حسّية دقيقة تتيح للدماغ التفريق بين القهوة والقرفة أو الدخان والعطر. في الفئران السليمة، تتجه الخلايا التي تحمل مستقبلًا واحدًا (يسمّى M72) وأخرى (تُسمّى P2) بثبات إلى عُقيدتين محدّدتين في كل بُصيلة، مكوِّنة خريطة منظمة وقابلة للتكرار بدرجة عالية.
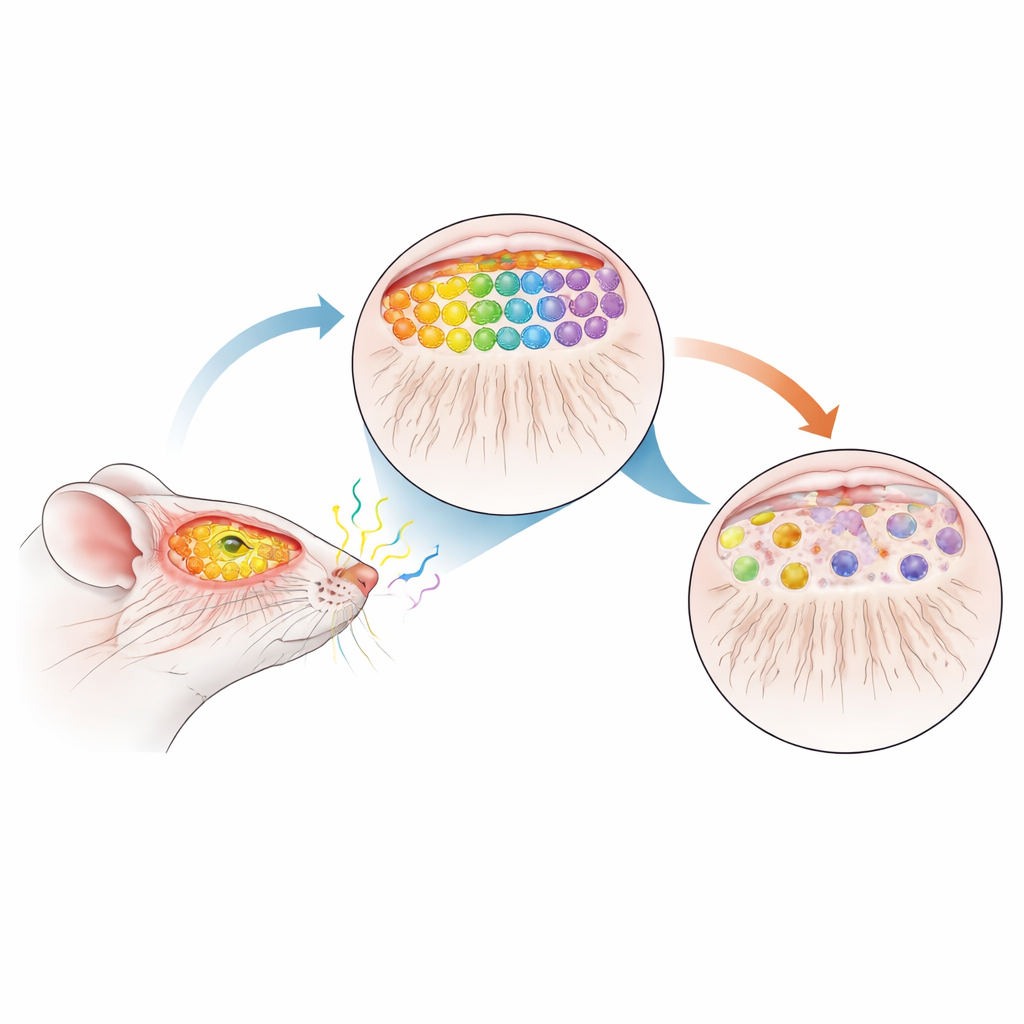
فأر بديل لمرحلة باركنسون المبكّرة
للاطّلاع على كيفية اضطراب هذه الخريطة بفعل مرض باركنسون، استخدم الفريق فئرانًا تُفرِط في إنتاج ألفا-سينوكلين البشري الطبيعي، وهو نفس البروتين الذي يتجمع في أدمغة المصابين بباركنسون. ثم قاموا بتقاطع هذه الحيوانات مع فئران موسوّمة لـ M72 وP2 حتى يتمكنوا من تتبع خلايا الشم المختارة وتوصيلاتها بصريًا. من المهم أن نذكر أن زيادة ألفا-سينوكلين تُفعّل فقط بعد الولادة وتتراكم تدريجيًا مع التقدّم في العمر، محاكيةً المسار البطيء والتقدّمي لمرض البشر. عند عمر 12 شهرًا—وهو منتصف العمر تقريبًا للفأر ومقارن بمرحلة ما قبل التشخيص لدى البشر—فحص الباحثون أجهزة الشم لدى الحيوانات بتفصيل.
عندما تنهار خريطة الشم
من خلال تلوين الخلايا الموسومة وتتبع مساراتها، وجد العلماء انهيارًا لافتًا في خريطة الشم لدى الفئران المفرطة التعبير عن ألفا-سينوكلين. انخفض عدد خلايا M72 وP2 في الأنف بشكل حاد—بنحو ثلاثة أرباع لفئة M72 وما يقارب النصف لفئة P2—بينما تقلّصت أليافها المتجهة إلى البصيلة بشكل كبير. بدلًا من أن تتلاقى بشكل منظم على عُقيدتين متينتين، شكلت الألياف المتبقية في كثير من الأحيان عُقيدات متعددة وأصغر بأحجام وأوضاع متباينة. لم تظهر هذه العُقيدات "الإضافية" في مواقع متسقة من فأر لآخر، ما يشير إلى فقدان الدقّة الطبوغرافية الطبيعية. كما انخفض مؤشر واسع لمهايئنة نهايات خلايا الشم، VGLUT2، بحوالي 44% في البصيلة، مما يدلّ على أن هذا الانحلال امتدّ إلى ما هو أبعد من نوعي المستقبل الموسومين.
ربط الدوائر المكسورة بفقدان الشم
ترجم التلف البنيوي إلى مشاكل قياسية في الشم. استغرق الفئران المسنة المُعبر عنها لألفا-سينوكلين وقتًا أطول للعثور على الطعام المخفي، وأظهرت قدرة أضعف على التمييز بين روائح مختلفة، وفشلت في تفضيل مناطق معلمة برائحتها الخاصة—اختبارات سلوكية تكشف معًا انخفاض حدّة الشم وضعف التمييز الشمي. كما احتاجت إلى تراكيز روائح أقوى بكثير للاستجابة، ما كشف عن حساسية مُنخفضة. لم تظهر هذه العُجزات في الفئران الأصغر سنًا، التي بدت خلاياها الموسومة وخرائطها سليمة إلى حدّ كبير، موحّدةً توقيت فقدان الوظيفة مع انهيار الخريطة الحسيّة لاحقًا بدلًا من مشكلات في التطور المبكّر. ومن الجدير بالذكر أن البروتين المعيب كان وفيرًا في البصيلة الشمّية، لكنه لم يكن قابلًا للكشف في بطانة الأنف الحسّية نفسها، ما يشير إلى أن التغيرات داخل دوائر البصيلة—وخاصةً في خلايا الميترا التي تنقل معلومات الشمّ إلى الأمام—هي المرجّح أن تكون المحرّك وراء اضطراب الخريطة.
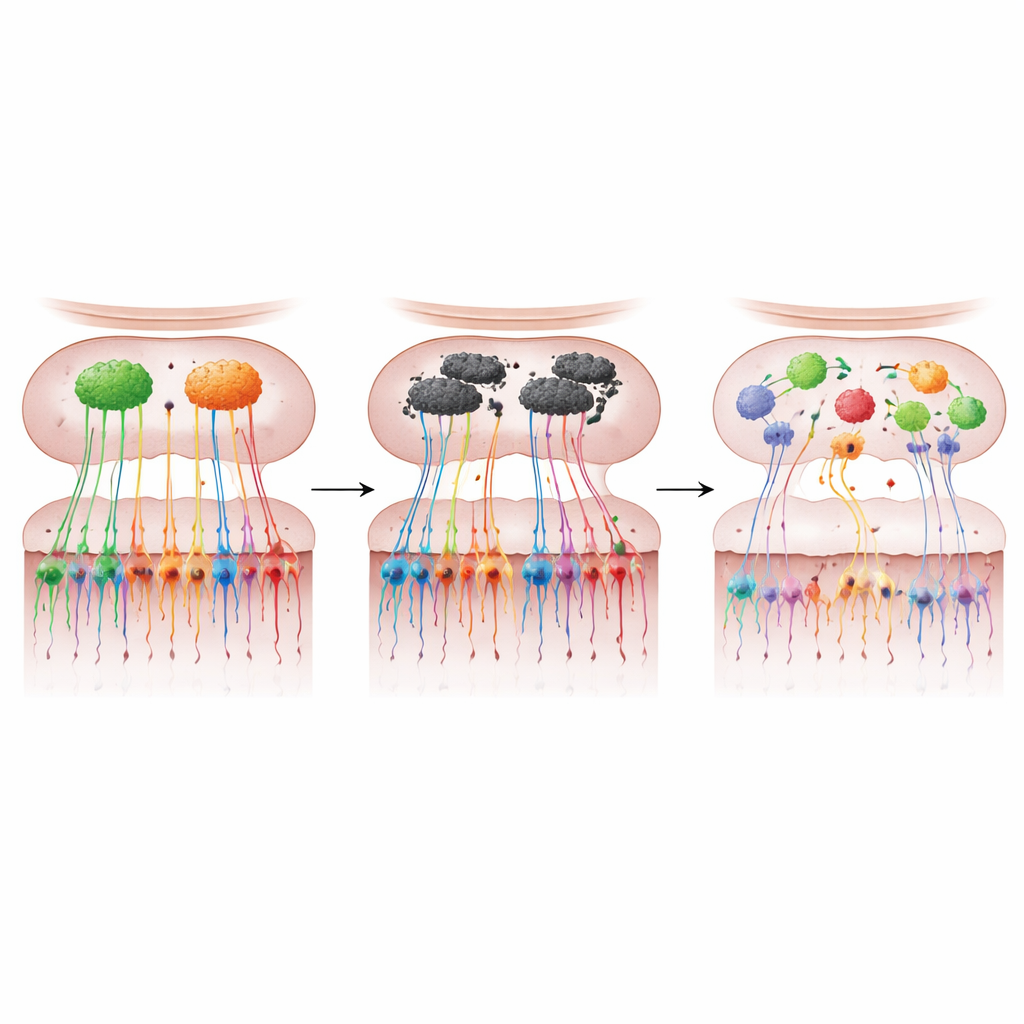
خلايا الشم نوافذ على المرض المبكّر
باختصار، تدعم هذه النتائج رسالة واضحة لغير المختصين: في نموذج فأري يشبه باركنسون، يؤدي فرط إنتاج ألفا-سينوكلين في البصيلة الشمّية إلى فقدان وسوء توصيل خلايا الشم، مشوّهًا خريطة الروائح في الدماغ ومسببًا مشاكل مبكرة في الشم. وبما أن خلايا الحسّ في الأنف مرتبطة نمائيًا بالدماغ ويمكن أخذ عينات منها بواسطة مسحات أو خزعات قليلة التوغّل، يجادل المؤلفون بأن تغيّرات مماثلة لدى البشر قد تقدّم علامة حيوية مبكرة قوية لمرض باركنسون. ويقترحون أن رسم بصمات هذه الخلايا الجزيئية قد يساعد ليس فقط في كشف الأشخاص المعرضين للخطر سنوات قبل ظهور الأعراض الحركية، بل أيضًا في تقديم رؤى جديدة حول كيفية بدء المرض وانتشاره—وكيف قد يتم إبطاؤه أو منعه.
الاستشهاد: Biju, K.C., Hernandez, E.T., Stallings, A.M. et al. Olfactory sensory map is perturbed in a human wild-type α-synuclein overexpressing transgenic mouse model of Parkinson’s disease. npj Parkinsons Dis. 12, 70 (2026). https://doi.org/10.1038/s41531-026-01288-w
الكلمات المفتاحية: مرض باركنسون, اضطراب حاسة الشم, ألفا-سينوكلين, خريطة حسّية, مؤشرات حيوية