Clear Sky Science · ar
تقييم منهجي لمُنظِّمي شكل الميتوكوندريا لتحسين اعتلال بروتين α-سينوكلين في الخلايا العصبية
لماذا تهم «المحطات الصغيرة للطاقة» في أمراض الدماغ
تُعدّ الميتوكوندريا «محطات الطاقة» داخل الخلايا ضرورية لبقاء الخلايا العصبية وعمل وصلاتها. في اضطرابات الدماغ مثل مرض باركنسون، تظهر هذه الهياكل الصغيرة في كثير من الأحيان متضررة أو متكسرة، لكن كان من الصعب تمييز أي التغيرات ضارة وأي المفاتيح يمكننا تبديلها بأمان لحمايتها. تفحص هذه الدراسة بشكل منهجي مُنظِّمي شكل الميتوكوندريا الرئيسيين في نموذج مختبري لتراكم البروتين المرتبط بمرض باركنسون، مستخدمة أداة تعتمد على الذكاء الاصطناعي لقياس أشكال الميتوكوندريا داخل أجزاء مختلفة من الخلايا العصبية. تشير النتائج إلى مُنظِّم بعينه، يُسمى Fis1، كهدف واعد للحفاظ على صحة الميتوكوندريا — والمشابك — دون التسبب في آثار جانبية جديدة.
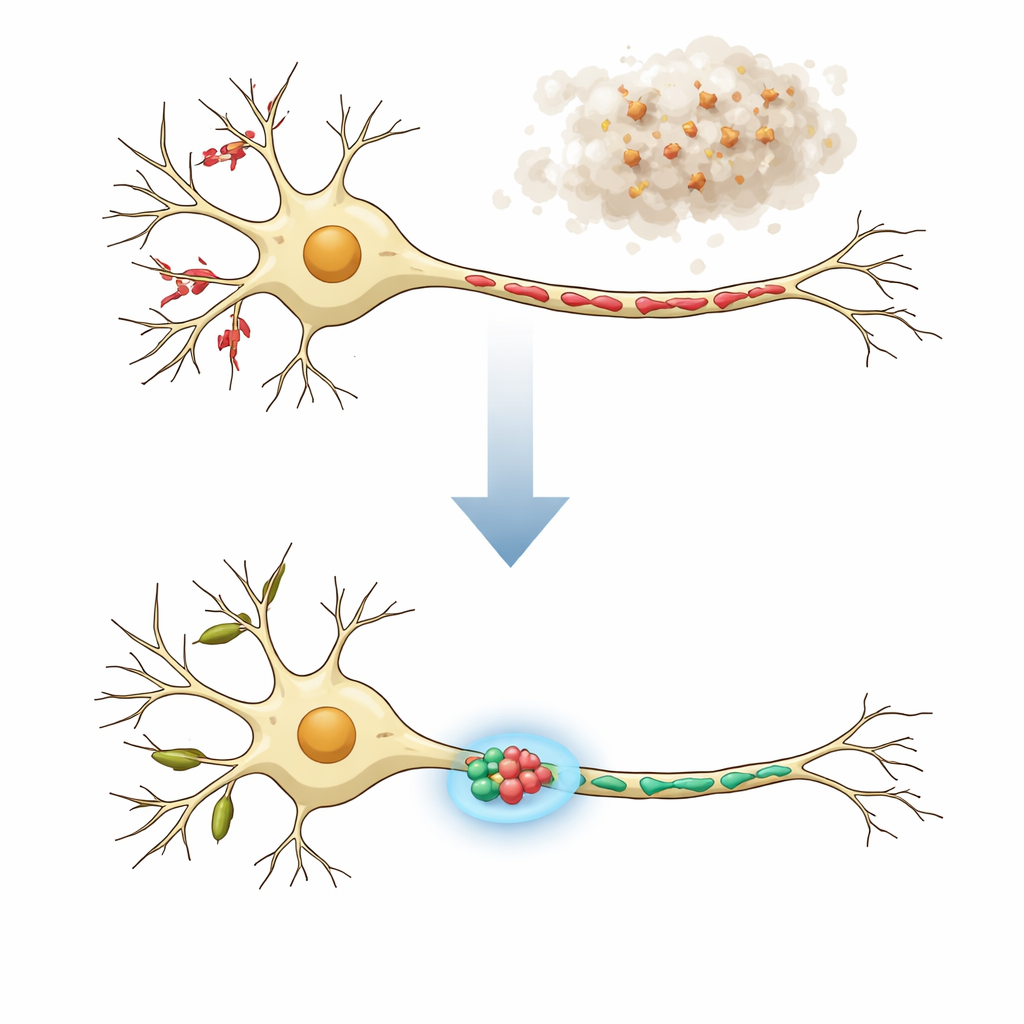
حَيّان مختلفان داخل خلية عصبية
الخلايا العصبية ليست متماثلة: ففروعها الشجرية (التغصنات) وأسلاكها الطويلة (المحاور) تقوم بمهام مختلفة وتحتوي على ميتوكوندريا ذات أشكال متباينة. في الخلايا العصبية السليمة، تميل التغصنات إلى احتواء ميتوكوندريا طويلة وأنبوبية تدعم الإنتاج المحلي للبروتين والتواصل المرن في مواقع الاستقبال المسماة نتوءات التغصن. أما المحاور، التي تبعث الإشارة، فتحمل ميتوكوندريا قصيرة عديدة تزود الطاقة وتساعد في تنظيم مستويات الكالسيوم عند النهايات قبل المشبكية. في الأمراض التنكسية العصبية يمكن أن تتعرض وظيفة وبنية هذه الميتوكوندريا للاضطراب، فتظهر كمقاطع متكسرة أو أشكال منتفخة أو سلاسل محببة. رأى المؤلفون أن العلاجات الفعالة حقًا يجب أن تعيد الميتوكوندريا في كل من التغصنات والمحاور إلى أشكالها الطبيعية الخاصة بكل حجرة من الخلية.
بناء اختبار إجهاد شبيه بمرض باركنسون
لمحاكاة سمة رئيسية من مرض باركنسون واضطرابات ذات صلة، عرّض الباحثون خلايا قشرية فأرية في الزراعة لألياف مُشكَّلة مسبقًا من بروتين ألفا-سينوكلين، وهو بروتين يمكن أن يتجمع إلى شُعَيات ضارة. خلال أيام قليلة، أدت هذه الشعيرات إلى تكوين تراكم غير طبيعي لألفا-سينوكلين داخل الخلايا وتسببت في تفتت واضح للميتوكوندريا في كل من التغصنات والمحاور. باستخدام MitoVis، نظام تحليل صور عميق التعلم، تمكن الفريق من فصل التغصنات عن المحاور تلقائيًا في صور الميكروسكوب وقياس طول ومساحة وشكل مئات الميتوكوندريا في كل صورة أسرع بحوالي عشرة أضعاف من التتبع اليدوي. أكدت هذه المقاربة عالية الإنتاجية أن الحالة الشبيهة بالمرض قلصت الميتوكوندريا وجعلتها أكثر استدارة، متممةً تقارير النماذج الحيوانية وأنسجة المرضى.
اختبار مفاتيح تعديل شكل الميتوكوندريا
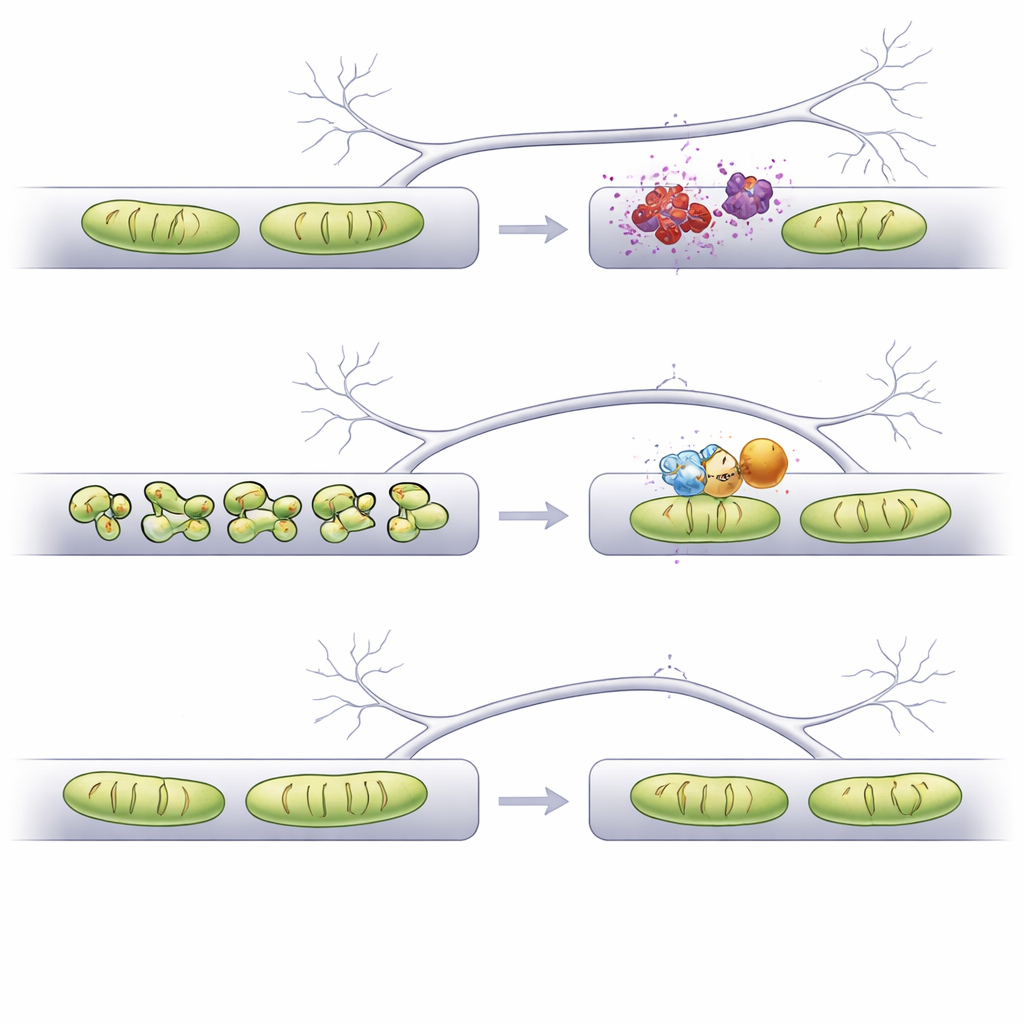
ثم تساءل الفريق ما إذا كان تحريك بروتينات الدمج والانقسام المحددة يمكن أن يمنع هذا الضرر. زيادة نشاط بروتينين مشاركين في الدمج (Mfn1 وMfn2) أو خفض بروتين انقسام (Mff) حمى ميتوكوندريا التغصنات من قصر الطول الناجم عن ألفا-سينوكلين وحافظ أيضًا على نتوءات التغصن من الفقدان. مع ذلك، جعلت هذه التعديلات نفسها ميتوكوندريا المحاور طويلة بصورة مفرطة، وهو ما ربطته دراسات سابقة بمشكلات في إطلاق الإشارات وتشعب المحور. بالمقابل، أدى تقليل بروتين انقسام مختلف، Fis1، إلى إعادة طول الميتوكوندريا في كل من التغصنات والمحاور إلى قيم قريبة من الطبيعي دون فرط استطالة. ومن المهم أن تقليل Fis1 في هذا الإعداد لم يتسبب في موت الخلايا العصبية، وكما في التدخلات الأخرى حافظ على كثافة نتوءات التغصن التي كانت لتنكمش تحت ضغط ألفا-سينوكلين.
المحافظة على توازن الكالسيوم
لأن الميتوكوندريا في المحاور تساعد على امتصاص الكالسيوم أثناء النشاط الكهربائي، اختبر الباحثون ما إذا كان تغيير شكلها يخل بهذا التوازن الدقيق. استعملوا حساسًا فلوريًا للكالسيوم موجهًا إلى الميتوكوندريا في العقيدات قبل المشبكية وحفزوا المحاور بنبضات قصيرة من جهود الفعل. في حالة ألفا-سينوكلين، بدا التعامل مع الكالسيوم في الميتوكوندريا المحورية المقصرة قليلًا مشابهًا للحالة الطبيعية. لكن عندما أصبحت ميتوكوندريا المحور طويلة للغاية نتيجة فرط التعبير عن Mfn1 أو خفض Mff، امتصت مزيدًا من الكالسيوم بعد التحفيز مقارنة بالمعتاد. قد يؤدي هذا الامتصاص المتزايد إلى تعطيل الوظيفة قبل المشبكية. على النقيض، حافظ خفض Fis1، الذي قام بتطبيع طول الميتوكوندريا دون إفراط، على استجابات الكالسيوم الميتوكوندرية بما يتطابق تقريبًا مع الضوابط الصحية، مما يشير إلى تنازلات خفية أقل.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
تُظهر الدراسة مجتمعة أن جعل الميتوكوندريا أطول ببساطة لا يكفي — فاستعادة شكلها إلى الحجم الصحيح في الحجرة الصحيحة هو الأمر الحاسم. باستخدام سير عمل تصوير مدعوم بالذكاء الاصطناعي، يحدد المؤلفون Fis1 كهدف جذاب بشكل خاص: انخفاض مستوياته يحافظ على استقرار البنية الميتوكوندرية في التغصنات والمحاور، ويمنع فقدان نتوءات التغصن، ويتجنب التعامل الشاذ مع الكالسيوم في النهايات قبل المشبكية. تدعم هذه النتائج فكرة أن تعديل شكل الميتوكوندريا بعناية، ربما عبر أدوية أو جزيئات مضادة للحمض النووي الريبوزي المرسال موجهة إلى Fis1، قد يساعد في حماية المشابك الضعيفة في اعتلال ألفا-سينوكلين المرتبط بمرض باركنسون وربما في أمراض دماغية أخرى تتعرض فيها الميتوكوندريا للخلل.
الاستشهاد: Kim, S.Y., Choi, J., Jang, D.C. et al. Systematic evaluation of mitochondrial morphology regulators for amelioration of neuronal α-synucleinopathy. npj Parkinsons Dis. 12, 58 (2026). https://doi.org/10.1038/s41531-026-01277-z
الكلمات المفتاحية: مرض باركنسون, الميتوكوندريا, ألفا-سينوكلين, خلل وظيفي في المشابك, التنكس العصبي