Clear Sky Science · ar
تثبيط التكوين الجديد للسيراميد يخفف من آفات ألفا‑سينوكلين في نموذج فأري لمرض باركنسون
لماذا تهم الدهون في الدماغ لمرض باركنسون
يشتهر مرض باركنسون بارتعاش اليدين وبطء الحركات، لكن في أعماق الدماغ تجري دراما أكثر هدوءًا. تموت الخلايا العصبية التي تتحكم في الحركة تدريجيًا بينما يتجمع بروتين يسمى ألفا‑سينوكلين في كتل لزجة. تكشف هذه الدراسة أن فئة معينة من الدهون، تسمى السيراميدات، تسهم في دفع هذا الضرر—وأن منع إنتاجها يمكن أن يحمي خلايا الدماغ في الفئران ونماذج الخلايا البشرية. العمل يشير إلى مسار غير متوقع وقابل للاستهداف دوائيًا قد يبطئ أو يمنع باركنسون يومًا ما بدلاً من مجرد تخفيف أعراضه.
دلائل من أدمغة بعد الوفاة
لفهم ما إذا كانت السيراميدات متورطة في باركنسون والحالات المرتبطة به، فحص الباحثون أولًا أنسجة دماغية بعد الوفاة لأشخاص كانوا يعانون من خرف أجسام ليوي، وهو اضطراب يشارك نفس كتل البروتين السامة التي تُرى في باركنسون. باستخدام قياسات كيميائية حساسة، وجدوا أن العديد من أنواع السيراميد كانت أعلى بكثير في منطقة الدماغ المتوسط مقارنةً بالأدمغة السليمة، خاصة الأشكال ذات الذنوب الدهنية الطويلة. ثم أعادوا تحليل مجموعات بيانات جينية كبيرة من خلايا الدماغ البشرية واكتشفوا أن الجينات المسؤولة عن بناء ومعالجة السيراميدات كانت أكثر نشاطًا في الخلايا المنتجة للدوبامين لدى مرضى باركنسون، وكذلك في خلايا داعمة معينة مثل النجميات والخلايا قليلة التغصن. تشير هذه النتائج مجتمعة إلى أن توازن السيراميدا مضطرب عبر عدة أنواع خلوية في الدماغ المريض.
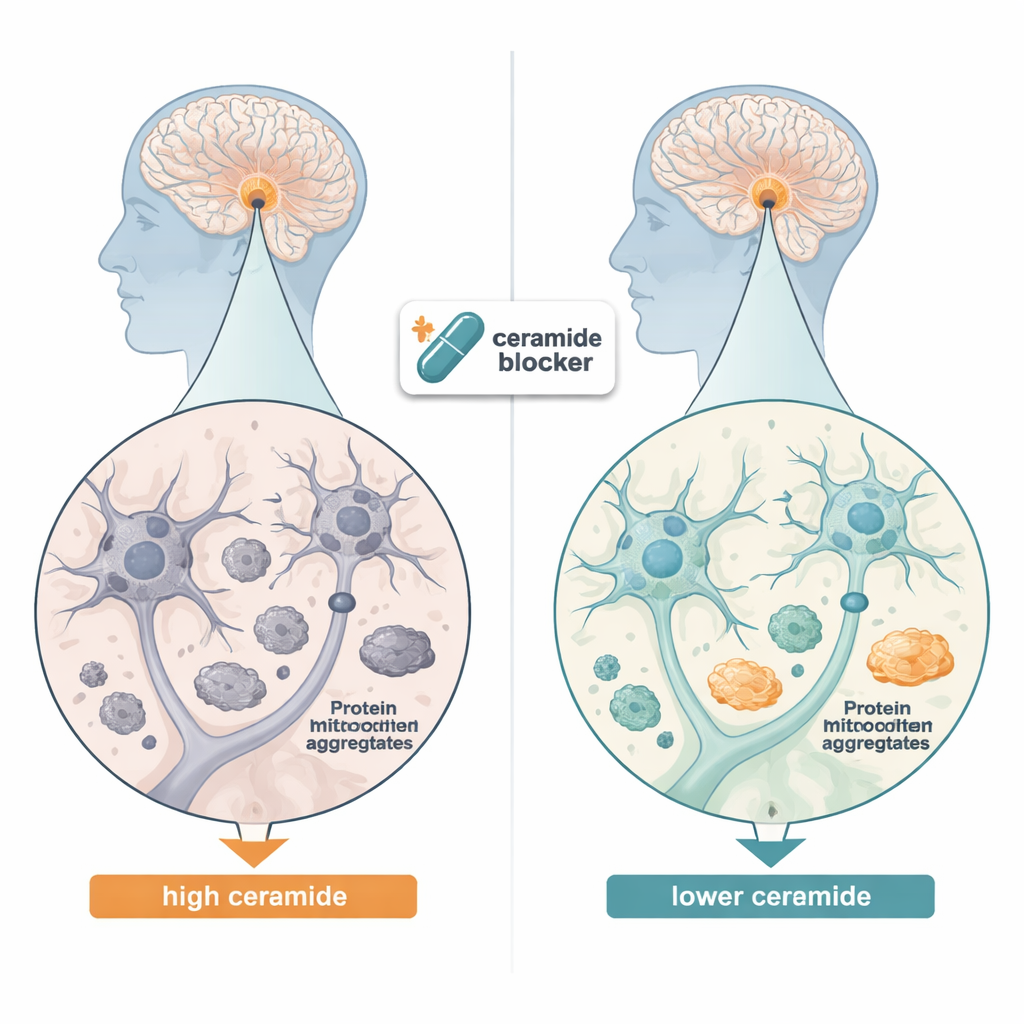
تنظيف كتل البروتين داخل الخلايا
سأل الفريق بعد ذلك ما إذا كان خفض مستويات السيراميد يمكن أن يقلل من تراكم البروتين في خلايا شبيهة بالعصب مزروعة في المختبر. استخدموا خلايا ورم عصبي بشري معدّلة لإنتاج شكل طفري من ألفا‑سينوكلين يميل للتكتل بسهولة. عندما أوقفوا أول خطوة في إنتاج السيراميد—إما بتسكين جين إنزيم رئيسي أو بإضافة دواء يسمى ميريوسين—انخفضت كمية تجمعات ألفا‑سينوكلين غير القابلة للذوبان بشكل حاد. في الوقت نفسه، ارتفعت مؤشرات البتوفاجي الميتوكوندري، النظام المتخصص للخلايا في العثور على الميتوكوندريا التالفة وإعادة تدويرها، وأصبح الجهاز الذي وسم البروتينات غير المرغوب فيها للتخلص منها أكثر نشاطًا. تشير هذه التحولات إلى أن فائض السيراميد عادةً ما يعوق طواقم التنظيف الخلوية، وأن إزالة هذا العبء الدهني تتيح للخلايا تنظيف الميتوكوندريا التالفة وكتل البروتين بكفاءة أكبر.
حماية وظائف الدماغ في الفئران
كان الاختبار الأكثر حسمًا ما إذا كانت هذه الاستراتيجية مفيدة في دماغ حي. عالج الباحثون نموذجًا فأريًا راسخًا ينتج كميات زائدة من ألفا‑سينوكلين البشري الطفري ويتطور تدريجيًا ليعاني من مشاكل حركة وضعف في الذاكرة. ابتداءً من منتصف العمر، تلقى بعض الفئران حقن ميريوسين لعدة أشهر، بينما حصلت الأخرى على محرك خالٍ من التأثير. خفّض ميريوسين بوضوح مستويات السيراميد في دم ونخاع الدماغ المتوسط لدى الحيوانات. أظهرت اختبارات السلوك أن الفئران المعالجة مشت لمسافات أطول وأدت أداءً أفضل في متاهة بسيطة تعتمد على الذاكرة العاملة المكانية. كشفت شرائح الدماغ من هذه الحيوانات أن خلايا منتجة للدوبامين نجت بكثرة في مناطق رئيسية، وأن كمية ألفا‑سينوكلين الفسفوري والمعرض للتكتل قد انخفضت. وأظهر تحليل واسع النطاق للتعبير الجيني في الدماغ المتوسط أن ميريوسين خفّض مسارات الالتهاب بينما أعاد نشاط جينات مرتبطة بالتواصل المشبكي وصيانة الميتوكوندريا الصحية.
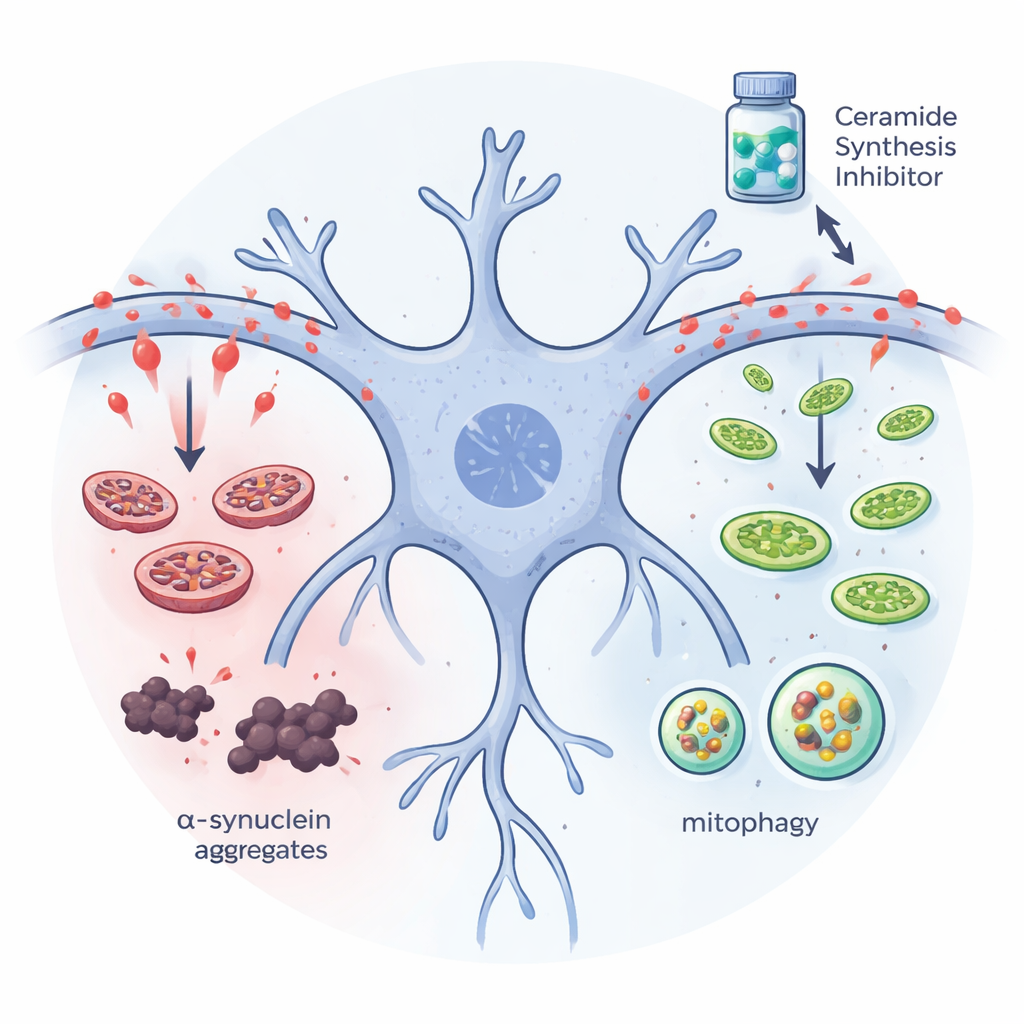
الخلايا العصبية البشرية والـ«أورجانيدات» تتزامن مع النتائج
للاقتراب أكثر من المرضى، استخدم الفريق خلايا عصبية و"أورجانيدات" ثلاثية الأبعاد من دماغ المتوسط مزروعة من خلايا جذعية مستحثة متعددة القدرات مأخوذة من أشخاص مصابين بباركنسون. في الخلايا المريضة الحاملة لمؤشر فلوري للبتوفاجي الميتوكوندري، عزز علاج ميريوسين الإشارة التي تميّز توصيل الميتوكوندريا التالفة لمراكز إعادة التدوير الخلوية وحسّن بنية شبكة الميتوكوندريا. في أورجانيدات دماغ المتوسط، حافظ ميريوسين على الخلايا المنتجة للدوبامين وقلل من تجمعات ألفا‑سينوكلين الضارة. عندما أضاف الباحثون سيراميدات إضافية إلى هذه الأدمغة المصغرة، حدث العكس: تشكلت المزيد من كتل البروتين وفُقدت خلايا الدوبامين، خاصة في الأورجانيدات المأخوذة من متبرعين بباركنسون. تدعم هذه التجارب دورًا ضارًا ومباشرًا لتراكم السيراميد في نسيج بشري ذي صلة بالمرض.
ما الذي قد يعنيه هذا للعلاجات المستقبلية
بالنسبة لغير المتخصصين، الرسالة الأساسية واضحة: في نماذج متعددة لباركنسون، يبدو أن فائض نوع معين من دهون الدماغ يسمم الخلايا عن طريق تعزيز تكتلات البروتين والميتوكوندريا المعطلة والالتهاب المزمن. حجب المسار الرئيسي لصنع هذه الدهون، باستخدام الدواء التجريبي ميريوسين، خفف هذه المشكلات، وحافظ على الخلايا العصبية الضعيفة، وحسّن السلوك في الفئران، بينما أنقذ أيضًا خلايا بشرية في طبق. يؤكد المؤلفون أن السلامة والجرعات طويلة الأمد في البشر غير معروفة، وأن لباركنسون أسبابًا عديدة تتجاوز السيراميدات. ومع ذلك، يفتح العمل خط هجوم جديدًا: بدلاً من مجرد تعزيز إشارة الدوبامين المتضائلة، قد تعمل العلاجات المستقبلية أيضًا على تطبيع أيض الدهون وآليات التنظيف الخلوية، مما يمنح خلايا الدماغ فرصة أفضل لمقاومة التقدم البطيء للضمور العصبي.
الاستشهاد: Lee, E., Park, My., Park, M. et al. Inhibition of de novo ceramide synthesis mitigates alpha-synuclein pathology in a Parkinson’s disease mouse model. npj Parkinsons Dis. 12, 49 (2026). https://doi.org/10.1038/s41531-026-01263-5
الكلمات المفتاحية: مرض باركنسون, سيراميد, ألفا‑سينوكلين, البتوفاجي, الضمور العصبي