Clear Sky Science · ar
متغيرات في MTNAP1 تسبب اضطرابًا عصبيًا تنكسيًا عن طريق إضعاف استقرار الميتوكوندريا
لماذا تهم هذه القصة صحة الدماغ
تواجه عائلات كثيرة ألم مشاهدة طفل يفقد مهارات تطورية تدريجيًا من دون تشخيص واضح. تكشف هذه الدراسة سببًا جينيًا جديدًا لمثل هذه الحالة، متتبعةً السلسلة من جين واحد معطوب إلى «محطات الطاقة» التالفة داخل خلايا الدماغ، وفي النهاية إلى انكماش نسيج المخ. فهم هذا التسلسل لا يوفر إجابات للعائلات المتضررة فحسب، بل يعمق أيضًا فهمنا العام لهشاشة أنظمة الطاقة في الدماغ.
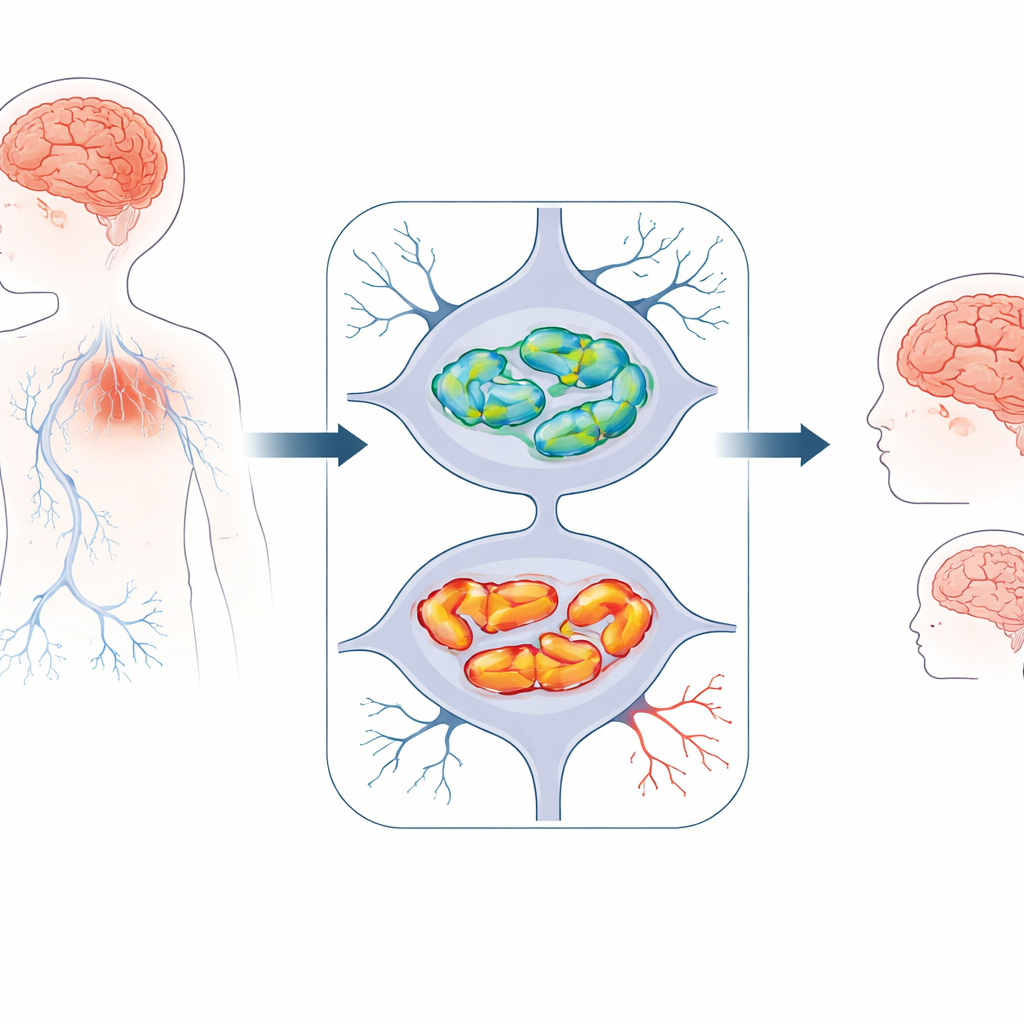
اضطراب دماغي طفولي تم التعرف عليه حديثًا
درس الباحثون ثلاثة أطفال من عائلتين غير مرتبطتين أظهروا جميعًا مشاكل تطورية مبكرة. كانوا أصغر من المتوقع بالنسبة لعمرهم، تأخروا في الجلوس والمشي والكلام ثم فقدوا بعض هذه القدرات تدريجيًا. طوّر الجميع صعوبات حركية مثل مشية غير مستقرة، تيبس العضلات أو انخفاض التوتر العضلي، ونوبات صرع. أظهرت صور الدماغ نمطًا متسقًا: نسيج كل من الدماغ الكبير (المخ) و«الدماغ الصغير» في الخلف (المخيخ) كان يترقق مع مرور الوقت، وجسرًا رئيسيًا من الألياف العصبية، الجسم الثفني، كان نحيفًا بشكل غير معتاد. أشارت هذه السمات إلى فقدان تدريجي للخلايا العصبية بدلاً من إصابة وحيدة عند الولادة.
جين صغير بعواقب كبيرة
للبحث عن سبب وراثي، قام الفريق بتسلسل جميع الجينات المشفرة للبروتين لدى الأطفال المتأثرين ووالديهم. وقع اختيارهم على جين يُدعى MTNAP1، الذي يساعد في تنظيم الحمض النووي داخل الميتوكوندريا، مصانع طاقة الخلية. حمل كل طفل نسختين معطوبتين من MTNAP1، واحدة من كل والد حامل سليم. في اثنين من الأشقاء، أدى تغيير حرف واحد في الجين إلى استبدال وحدة بنائية من البروتين بأخرى، مشوّهًا شكله بشكل طفيف. في الطفل الثالث، أدى إشارة توقف مبكرة في الجين على الأرجح إلى منع تكوين البروتين تمامًا. لم تُرَ هذه التغييرات في قواعد بيانات سكانية كبيرة، مما يعزز احتمال أن تكون طفرات نادرة ومضرة وليست فروقًا حميدة.
محطات الطاقة تحت الضغط
بعد ذلك، فحص العلماء خلايا جلد مأخوذة من الأطفال وقارنوها بخلايا من أفراد أصحاء. تحت المجهر، أظهرت الخلايا الطبيعية ميتوكوندريا طويلة خيطية تشكل شبكة مترابطة، بينما احتوت خلايا الأطفال على ميتوكوندريا قصيرة ومكسورة ومتجمعة. عندما قلّل الباحثون تجريبيًا مستويات MTNAP1 في سلالة خلوية شبيهة بالعصب، لاحظوا نفس تفكك الشبكة الميتوكوندريَّة، ما أكد أن خسارة هذا البروتين وحدها يمكن أن تُخلّ بهيكلها. كشفت قياسات نشاط الميتوكوندريا أن خطوات رئيسية في إنتاج الطاقة أضعفت، وأنتجت الخلايا كمية زائدة من أنواع الأكسجين التفاعلية — نواتج أكسجينية ضارة تعمل مثل الصدأ الجزيئي. توقفت الخلايا المتضررة عن الانقسام بشكل طبيعي، تراكمت في طور سكون، وفعلت علامات الشيخوخة المبكرة.
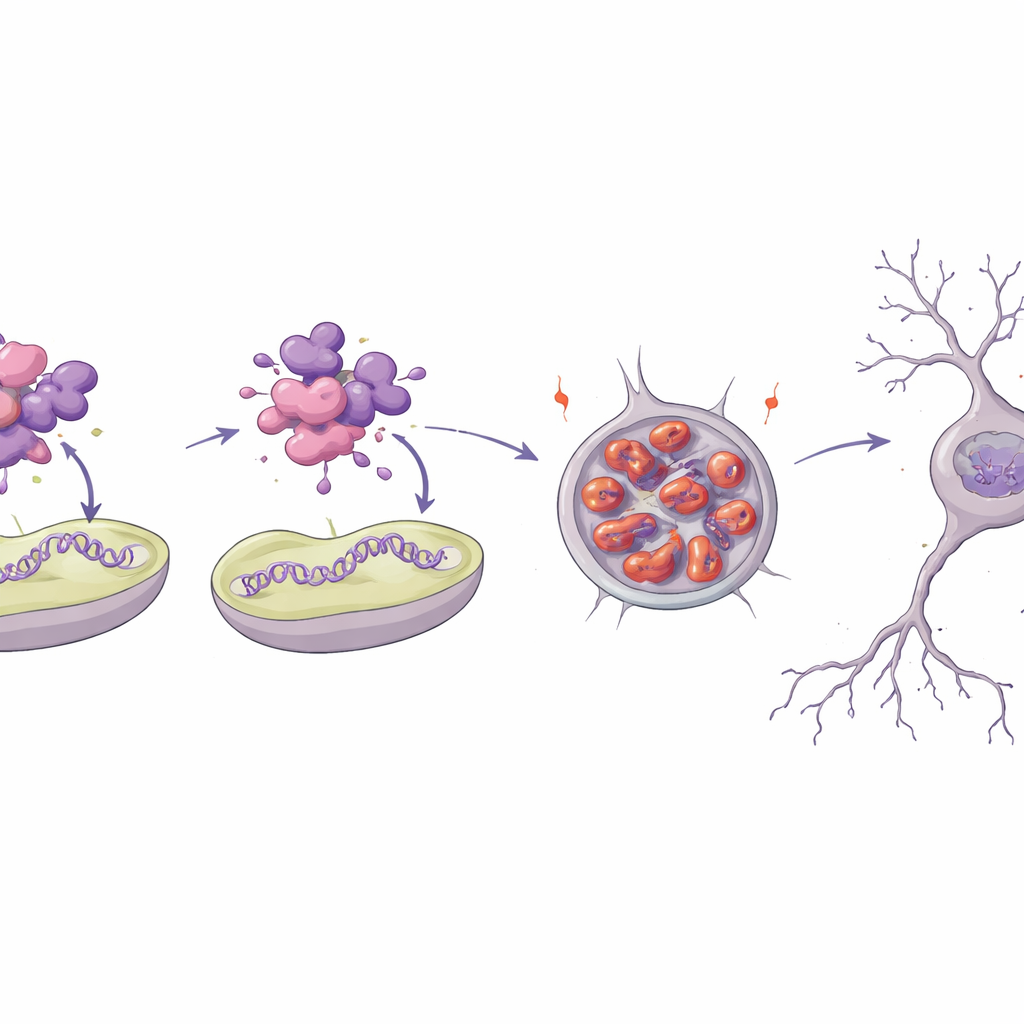
كيف يفك تغيير واحد بنية بروتين حيوي
لفهم سبب تأثير إحدى الطفرات بشدة، نمذج الفريق البنية ثلاثية الأبعاد لبروتين MTNAP1 وأعاد تصنيعه في المختبر. تقع الوحدة البنائية المستبدلة في منطقة حلزونية مضغوطة عادةً تساعد البروتين على التفاعل مع الحمض النووي الميتوكوندري والغشاء الداخلي. أظهرت محاكاة حاسوبية واختبارات فيزيائية حيوية أن البروتين الطافر أقل استقرارًا، يفقد كثيرًا من بنيته المنتظمة، ويتجمع بسهولة في كتل. في تجارب أنبوبية، ارتبط البروتين الطبيعي بقوة بقطع قصيرة من الحمض النووي الميتوكوندري وبأسطح غشائية اصطناعية، بينما تكاد تلامس الطافر هذه المكونات وتجمع بدلًا من ذلك في هياكل تشبه الأميلويد. عند إدخال الطافر إلى خلايا شبيهة بالعصب، تراكم في كتل كبيرة محيطة بالنواة مع مرور الوقت، علامة على إرهاق أنظمة جودة البروتين.
من الميتوكوندريا التالفة إلى دماغ يفشل
بجمع الأدلة، ترسم الدراسة نموذجًا مرحليًا: يضعف MTNAP1 المعطوب القاعدة التي تساعد على تنظيم الحمض النووي الميتوكوندري وربطه بالغشاء الداخلي؛ هذا يزعزع استقرار الميتوكوندريا، مما يؤدي إلى تفتتها وفقدان قدرتها على توليد الطاقة بكفاءة؛ يرفع ذلك الإجهاد التأكسدي وإشارات «الشيخوخة المبكرة» الخلوية التي تجعل الخلايا العصبية عرضة بشكل خاص، لأن احتياجاتها من الطاقة عالية ومستمرة وقدرتها على التجدد محدودة. في الدماغ النامي، يتحول هذا النقص الطاقي البطيء والمستمر إلى توقف في مراحل النمو، فقدان المهارات المكتسبة، وتقلص تدريجي للمناطق الدماغية الرئيسية. بينما هناك حاجة إلى مزيد من المرضى ودراسات الحيوان لرسم متكامل للمتلازمة، تضع هذه العملة MTNAP1 بثبات كحارس حاسم لاستقرار الميتوكوندريا وتبرز تنظيم الحمض النووي الميتوكوندري كركيزة مركزية لتطور دماغ صحي.
الاستشهاد: Kumar, A., Saha, S., Nasir, N. et al. Variants in MTNAP1 underlie a neurodegenerative disorder by impairing mitochondrial stability. npj Genom. Med. 11, 19 (2026). https://doi.org/10.1038/s41525-026-00554-3
الكلمات المفتاحية: الميتوكوندريا, الضمور العصبي, علم الوراثة للأطفال, الحمض النووي الميتوكوندري, طي البروتينات بشكل خاطئ