Clear Sky Science · ar
تحليل النسخيات الجينية لكشف آلية تحسيس الإشعاع في سرطانات الثدي الثلاثية السلبية الإيجابية لمستقبل الأندروجين عبر تثبيط المستقبل
لماذا تهم هذه الدراسة الأشخاص المصابين بسرطان الثدي
العلاج الإشعاعي هو حجر زاوية في علاج العديد من الأشخاص المصابين بأورام ثدي عدوانية، لكن بعض الأورام تكون بطبيعتها أكثر صعوبة في القتل بالإشعاع من غيرها. تطرح هذه الدراسة سؤالاً عملياً له تبعات سريرية حقيقية: هل يمكن لفئة من الأدوية التي تحجب إشارات الهرمونات الذكرية، والمستخدمة بالفعل في سرطان البروستات، أن تجعل شريحة من سرطانات الثدي ثلاثية السلبيات أكثر عُرضة للإشعاع — ولماذا ينجح ذلك في بعض الحالات وليس في أخرى؟
شكل من سرطان الثدي يصعب علاجه
تفتقر سرطانات الثدي ثلاثية السلبيات إلى ثلاثة أهداف جزيئية شائعة — مستقبلات الإستروجين، مستقبلات البروجيسترون، وHER2 — لذا غالباً ما يضطر المرضى للاعتماد على الجراحة، والكيميائي، والإشعاع فقط. مع ذلك، تحمل نسبة من هذه الأورام مستقبل الأندروجين، وهو بروتين يستجيب لهرمونات شبيهة بالتستوستيرون ويمكن أن يدفع نمو الورم. أظهرت أعمال سابقة أن حجب هذا المستقبل يمكن أن يبطئ هذه السرطانات وقد يعزز تأثيرات الإشعاع، لكن تفاصيل كيفية حدوث ذلك، وأي الأدوية والأورام تستفيد أكثر، كانت غير واضحة.
اختبار حاصرات الهرمونات الحديثة مع الإشعاع
درس الباحثون عدة نماذج مخبرية من خلايا سرطان الثدي ثلاثية السلبيات اختلفت أساساً في مقدار مستقبل الأندروجين الذي تحمله. ركزوا على دوائين مضادين للأندروجين أحدث، أبلوتاميد (apalutamide) ودارولوتاميد (darolutamide)، وجمعوا تعرضات قصيرة لهذه الأدوية مع جرعات قياسية من أشعة X. في الخلايا التي تحمل مستويات عالية من مستقبل الأندروجين، زاد أبلوتاميد بوضوح من ضرر الإشعاع، مما ترك عدداً أقل من الخلايا القادرة على تشكيل مستعمرة جديدة. في المقابل، كان لدارولوتاميد تأثير ضئيل أو غير موجود على حساسية الإشعاع في نفس الخلايا، ولم يفد أي من الدوائين في الخلايا التي أعربت عن مستويات منخفضة جداً من مستقبل الأندروجين. تشير هذه النتائج إلى أن ليس كل أدوية حجب الأندروجين تعمل بنفس الطريقة في سرطان الثدي، وأن الأورام يجب أن تعتمد بقوة على هذا المستقبل لكي تنجح هذه المضافة.
مراقبة حركة بروتين رئيسي داخل الخلية
لفهم ما يحدث داخل خلايا السرطان بعد إشارات الهرمونات أو الإشعاع، تتبعت الفريق موقع مستقبل الأندروجين نفسه. عندما تعرضت الخلايا لأندروجين اصطناعي، تحرك المستقبل إلى النواة، مركز التحكم حيث تُشغل وتُوقف الجينات. لم يدفع الإشعاع وحده المستقبل للخروج من النواة؛ بل بقي هناك بعد العلاج، مستعداً للتأثير على نشاط الجينات. ومع ذلك، عندما تلقت الخلايا دواء مضاداً للأندروجين إنزالوتاميد (enzalutamide) قبل الإشعاع، انخفضت مستويات المستقبل في النواة وبقي جزء أكبر منه في سائِل الخلية الخارجي. يدعم هذا فكرة أن حجب دخول المستقبل إلى النواة يعيق قدرته على إطلاق برنامج جيني وقائي بعد الإشعاع.
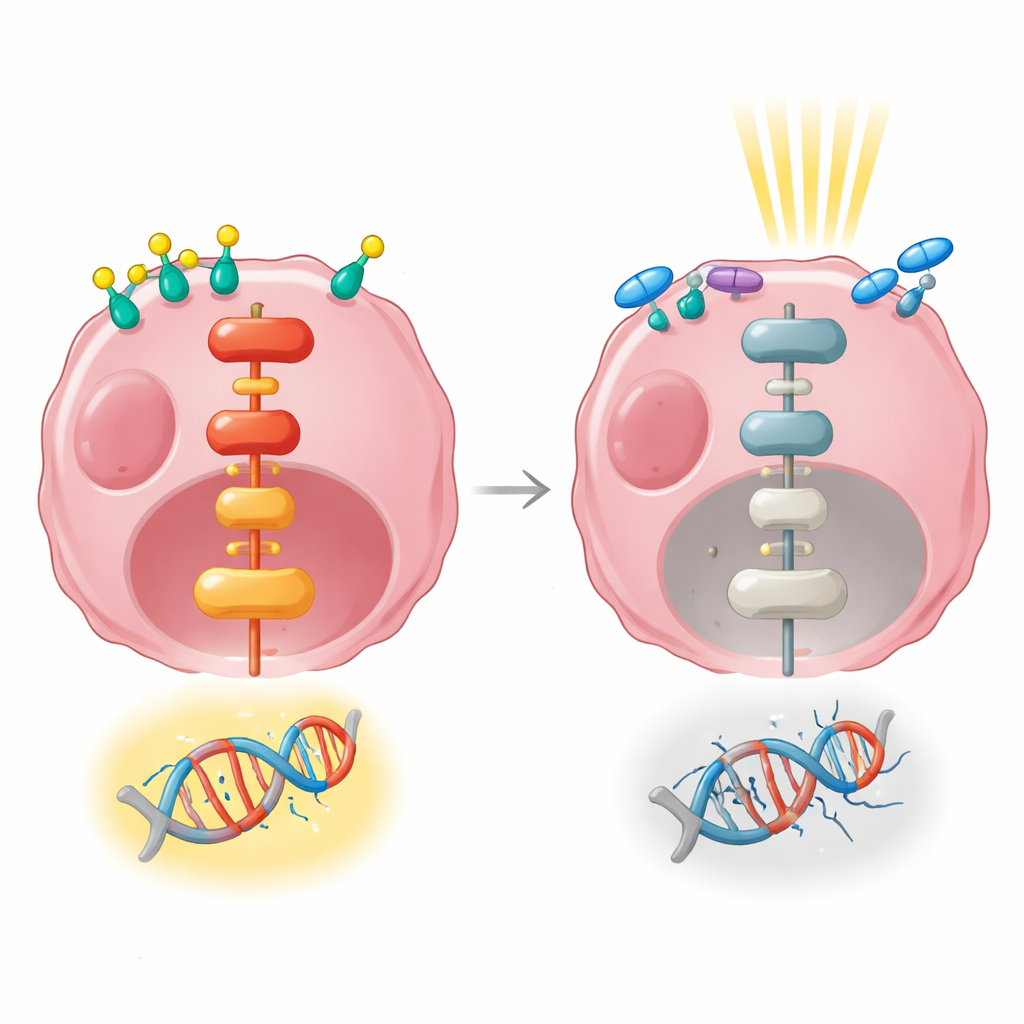
الإشارات الجينية التي تربط الهرمونات بالمقاومة
ثم استخدم الباحثون تسلسل الحمض النووي الريبي (RNA-seq) لأخذ لقطة واسعة للجينات التي ارتفعت أو انخفضت بعد تحفيز الهرمونات، أو الإشعاع، أو كلاهما. غير العلاج الهرموني وحده نشاط مئات الجينات وأثر بقوة على المسارات التي تحكم نمو الخلايا، والتلاصق، والتواصل مع البيئة المحيطة. أما الإشعاع المعطى بمفرده، فعند نقطة زمنية مبكرة، فقد غيّر عدداً أقل بكثير من الجينات. عندما اجتمعت تحفيز الهرمونات والإشعاع، تنشطت العديد من نفس المسارات المتعلقة بالنمو، بما في ذلك مسار إشارية رئيسي معروف باسم MAPK/ERK، الذي ينقل الإشارات من سطح الخلية إلى النواة. ومن المعروف أن هذا المسار يساعد الخلايا على البقاء وإصلاح تلف الحمض النووي.
استكشاف مسار بقاء يحمي الحمض النووي
بما أن إشارة MAPK/ERK ظلت تظهر في تحليلاتهم، اختبر الباحثون ما إذا كان تعزيز هذا المسار يمكن أن يلغي فائدة حجب الأندروجين أثناء الإشعاع. صنَّعوا خلايا سرطانية لإنتاج نسخة دائمة النشاط من ERK، وهو مكوّن رئيسي في المسار، ثم أعادوا تجربة الإشعاع مع أبلوتاميد. في هذا الإعداد، لم يعد أبلوتاميد يجعل الخلايا أكثر حساسية للإشعاع: بدا أن إشارة ERK المتضخمة تحميها. إلى جانب قياسات البروتين، تشير هذه النتائج إلى أن إشارة MAPK/ERK تشكل حلقة وصل حاسمة بين نشاط مستقبل الأندروجين وقدرة الخلية على إصلاح فواصل الحمض النووي الناتجة عن الإشعاع.
ما الذي يعنيه هذا لرعاية سرطان الثدي المستقبلية
بمصطلحات يومية، تقترح هذه الدراسة أن بعض سرطانات الثدي ثلاثية السلبيات تنجو من الإشعاع باستخدام إشارات مرتبطة بالأندروجينات لتشغيل دائرة بقاء داخلية تساعدها على إصلاح الحمض النووي التالف. يمكن لأدوية مثل أبلوتاميد وإنزالوتاميد أن تقطع هذه الدائرة في الأورام التي تعتمد اعتماداً قوياً على مستقبل الأندروجين، مما يجعل الإشعاع أكثر فعالية، بينما قد لا تستفيد الأورام ذات المستويات المنخفضة من المستقبل أو المسارات البديلة للبقاء. من خلال تخطيط مسارات الجينات المتورطة — خصوصاً مسار MAPK/ERK — تضع هذه الدراسة أساساً لتراكيب أدق من حاصرات الهرمونات، ومثبطات المسارات، والإشعاع التي قد تحسن النتائج للمرضى المصابين بهذا الشكل الصعب العلاج من سرطان الثدي.
الاستشهاد: McBean, B., Hauk, B., Michmerhuizen, A.R. et al. Transcriptomic analysis to uncover the mechanism of radiosensitization of AR-positive triple-negative breast cancers with AR inhibition. npj Breast Cancer 12, 50 (2026). https://doi.org/10.1038/s41523-026-00916-1
الكلمات المفتاحية: سرطان الثدي ثلاثي السلبيات, مستقبل الأندروجين, العلاج الإشعاعي, تحسيس للإشعاع, إشارة MAPK ERK