Clear Sky Science · ar
العلاج المناعي الكيميائي الموضعي القابل للبرمجة لسرطان الثدي ثلاثي السلبيات عبر إطلاق مكّون زمني ومكاني محكم لسلاسل CpG من أوليغوديوكسي نيوكليوتيدات والجيمسيتابين والباكليتاكسيل
تحويل سرطان ثدي عنيد إلى هدف محلي
يُعد سرطان الثدي ثلاثي السلبيات أحد أشد أشكال سرطان الثدي صعوبة في المعالجة لأنه يفتقر إلى المفاتيح الجزيئية المعتادة التي تستهدفها العديد من الأدوية الحديثة. غالباً ما يضطر المرضى إلى الاعتماد على علاج كيميائي قوي ينتشر في الجسم بأكمله، ما يسبب آثاراً جانبية خطيرة وغالباً تحقيق نتائج مخيبة على المدى الطويل. تستكشف هذه الدراسة فكرة مختلفة تماماً: بدلاً من إغراق الجسم بالأدوية، هل يمكننا وضع مخزون دوائي صغير قابل للبرمجة بجانب الورم، يطلق العلاجات الكيميائية والمعززة للمناعة بتتابع زمني دقيق في المكان الذي تُحتاج إليه بشدة؟
مخزون صغير بطموحات كبيرة
ابتكر الباحثون ما يسمونه منصة العلاج المناعي الكيميائي الموضعي القابل للبرمجة، أو PLICT. فكر فيها كقطيرة ناعمة قابلة للحقن تجلس بجانب ورم الثدي وتفرّج العلاج ببطء على مدى أسابيع. تجمع القطيرة بين هلام محب للماء يطلق بسرعة محفزاً مناعياً ودواء كيميائياً واحداً، الجيمسيتابين، وبين كرات بلاستيكية مجهرية تطلق تدريجياً دواءً ثانياً، الباكليتاكسيل. المحفز المناعي، وهو مقطع قصير من الحمض النووي يُسمى CpG، مصمّم لإيقاظ الخلايا المناعية المحلية، بينما تهاجم العلاجات الكيميائية المرتبطة الورم مباشرة وتعيد تشكيل بيئته لتسمح بخروج الخلايا المناعية ودخولها للقيام بعملها.
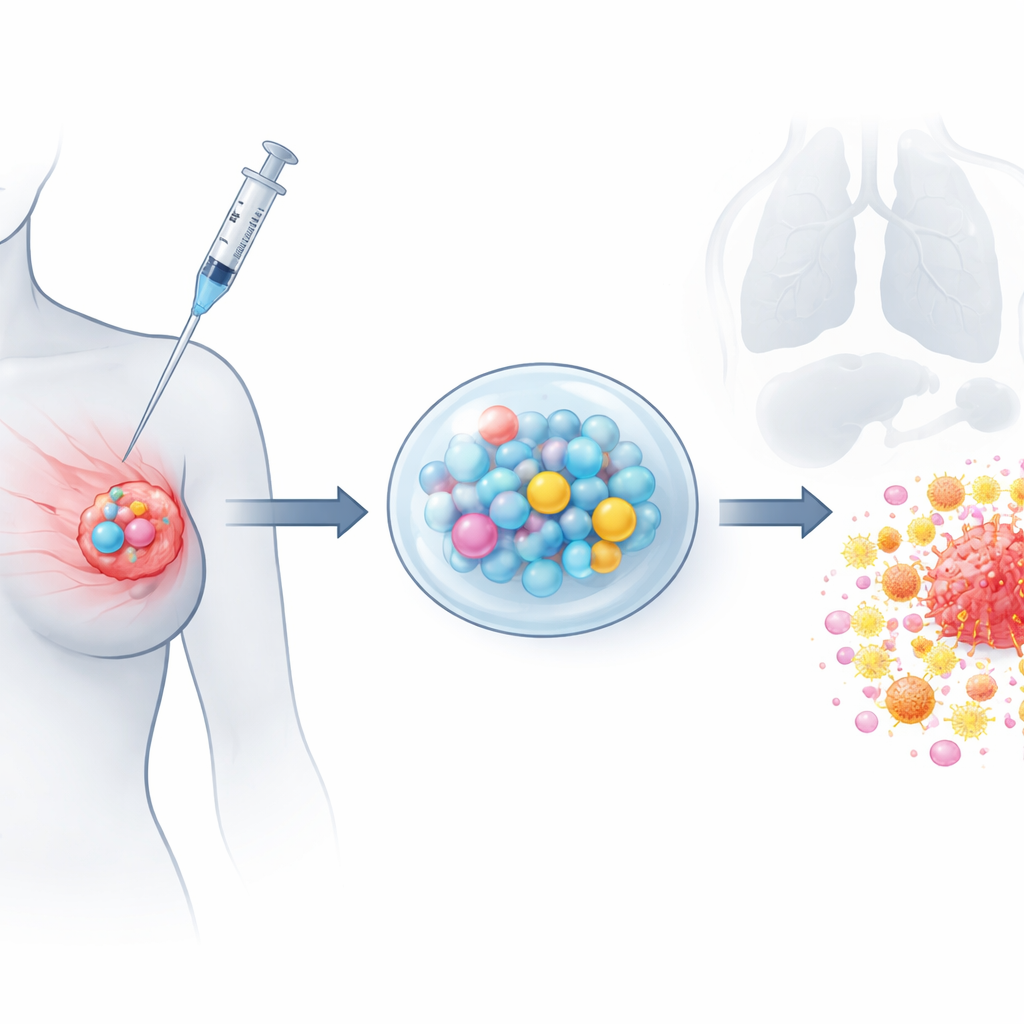
هندسة هجوم سرطاني بإطلاق متزامن
لبناء هذا النظام، استخدم الفريق طريقة «الرش الكهربائي» عالية الجهد لتشكيل جسيمات مجهرية متساوية محملة بالباكليتاكسيل من بوليمر قابل للتحلل الحيوي. أظهرت الصور جزيئات ملساء كروية بحجم حوالي عُشر عرض شعرة الإنسان، وأكدت الاختبارات المخبرية أن الباكليتاكسيل يتسرب بشكل مستمر لمدة لا تقل عن شهر دون اندفاعة مبكرة. بشكل منفصل، دمجوا الجيمسيتابين وCpG داخل هلام حساس لدرجة الحرارة يكون سائلاً عند التبريد ويصبح شبه صلب عند درجة حرارة الجسم. أكدت بصمة التحليل الكيميائي بقاء كلا الدواءين سليمين داخل الحوامل. عند الجمع بينهما، يوفر الهلام جرعة سريعة ومبكرة من الجيمسيتابين وCpG، بينما تقدم الجسيمات المجهرية تدفقاً مطولاً من الباكليتاكسيل، مقلدة فوائد العلاج الكيميائي طويل المدى منخفض الجرعة من تطبيق موضعي واحد.
اختبار الاستراتيجية الموضعية على الفئران
بعد ذلك اختبر الفريق نظام PLICT في نموذج فأري لسرطان الثدي ثلاثي السلبيات. طور الفئران أورام ثدي صغيرة ثم تلقت إما حقنات قياسية من الباكليتاكسيل وحده، أو باكليتاكسيل مع جيمسيتابين، أو زرع موضعي واحد من PLICT بجانب الورم. على مدار أربعة أسابيع نما الورم في مجموعة الضبط بسرعة، ونما ببطء أكبر في من حصلوا على العلاج الكيميائي القياسي، لكن الأورام المعالجة بـ PLICT كانت أصغر بكثير من حيث الحجم والوزن. أظهرت تصويرات الجسم بالكامل والأعضاء المستأصلة أن PLICT قلل أيضاً من انتشار السرطان إلى مواقع بعيدة، وبالأخص الرئتين، بشكل أكثر فعالية من الحقنات التقليدية. وكشفت قياسات مستويات الدواء السبب: كان الباكليتاكسيل مركزاً بشكل كبير داخل الأورام المعالجة بـ PLICT لكنه منخفض في الأنسجة الدهنية البعيدة ومشابه في مجرى الدم، مما يشير إلى احتجاز موضعي قوي مع تعرضات جانبية أقل في أماكن أخرى.
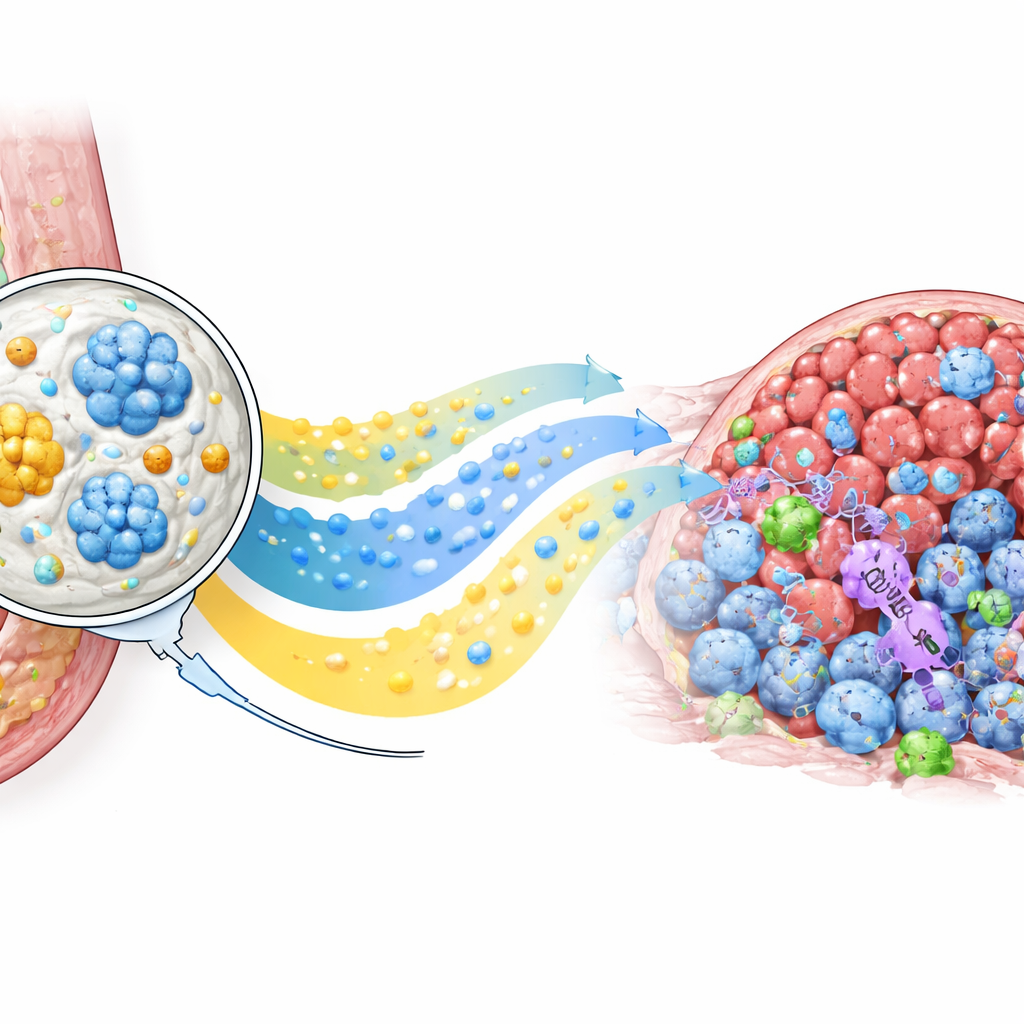
استدعاء مدافعي الجسم الطبيعيين
بخلاف تقليص الأورام، غيّر PLICT المشهد المناعي داخلها. أظهرت تحليلات خلوية مفصلة ارتفاعاً حاداً في خلايا T القاتلة CD8 داخل الأورام المعالجة مقارنة بجميع المجموعات الأخرى، إلى جانب انخفاض في أنواع معينة من الخلايا التنظيمية T التي تخفف عادة من الهجمات المناعية. وأكدت صبغات الأنسجة لمؤشر CD69، وهو علامة للخلايا T المنشَّطة حديثاً، أن كثيراً من هذه الخلايا المتوغلة كانت مفعلة وجاهزة للعمل. في الوقت نفسه، تسبب العلاج الكيميائي القياسي في تلف ملحوظ لأنسجة الكبد، بينما بدت أعضاء الفئران المعالجة بواسطة PLICT شبه طبيعية تحت المجهر. تشير هذه النتائج مجتمعة إلى أن المخزون الموضعي لا يعزز فقط تعرض الدواء المباشر للورم بل يشعل أيضاً استجابة مناعية أكثر ملاءمة وأقل قمعاً دون إضافة ضغط زائد على الأعضاء الحيوية.
ما الذي قد يعنيه هذا لمستقبل علاج السرطان
لغير المتخصصين، الرسالة واضحة: بتحويل العلاج الكيميائي وتحفيز المناعة إلى تدفق بطيء ومصمم بدقة يُقدّم بجانب الورم مباشرة، حققت هذه المقاربة سيطرة أقوى على الورم وآثاراً جانبية أقل على الجسم في التجارب الحيوانية مقارنة بالحقنات الدوائية القياسية. العمل ما يزال في مرحلة ما قبل السريرية، ولا تزال هناك أسئلة حول مدى أداء مثل هذا النظام في البشر أو في إعدادات علاجية مختلفة. لكن مفهوم "مخزون دوائي" قابل للحقن وقابل للبرمجة يطلق متعدد العوامل بتتابع هادئ قد يفتح طرقاً جديدة لعلاج سرطانات عدوانية مثل سرطان الثدي ثلاثي السلبيات—مركّزاً القتال حيث يهم الأمر أكثر مع حماية بقية الجسم.
الاستشهاد: Hsieh, CH., Hsu, MY., Lin, CF. et al. Programmable local immunochemotherapy for triple-negative breast cancer via spatiotemporally controlled release of CpG oligodeoxynucleotides, gemcitabine, and paclitaxel. npj Breast Cancer 12, 45 (2026). https://doi.org/10.1038/s41523-026-00910-7
الكلمات المفتاحية: سرطان الثدي ثلاثي السلبيات, توصيل دوائي موضعي, العلاج المناعي, الإطلاق المُتحكّم به, جسيمات هلامية مجهرية