Clear Sky Science · ar
كشف تعبير جينات الهدف لمستقبل الاستروجين β يكشف عن وظائف كبحية جديدة في سرطان الثدي العدواني
لماذا يهم هذا البحث
يعد سرطان الثدي الالتهابي أحد أكثر أنواع سرطان الثدي عدوانيةً وخطورة، إذ ينتشر بسرعة في كثير من الأحيان ويترك المرضى مع خيارات علاج موجهة قليلة. تستكشف هذه الدراسة جهاز استشعار هرموني أقل شهرة في خلايا الثدي، يُدعى مستقبل الاستروجين بيتا، وتُظهر كيف يمكن أن يعمل ككبح طبيعي لانتشار الورم. قد يفتح فهم كيفية عمل هذا الكبح المدمج الباب أمام أدوية جديدة تُبطئ أو تمنع الانتشار لدى مرضى لديهم حالياً خيارات محدودة للغاية.
وجه مختلف لسرطان الثدي الالتهابي
على عكس العديد من سرطانات الثدي التي تعتمد على مستقبل الاستروجين الكلاسيكي ألفا، عادةً ما يفتقد سرطان الثدي الالتهابي هذا الجزيء وبالتالي لا يستجيب جيدًا للعلاجات الهرمونية القياسية. ركز المؤلفون بدلاً من ذلك على مستقبل الاستروجين الثاني، مستقبل الاستروجين بيتا (ERβ)، الذي ربطوه سابقًا بانخفاض معدلات الانبثاث لدى المرضى ونماذج الفئران. أشارت أعمال سابقة إلى أن ERβ يبطئ آليات الحركة والهيكل الخلوي الداخلي. في هذه الدراسة، سعى الفريق لرسم خريطة على مستوى الجينوم بأكمله لكيفية تغيير ERβ لنشاط الجينات وما هي الجزيئات التالية التي قد تفسر دوره الوقائي المضاد للانبثاث.
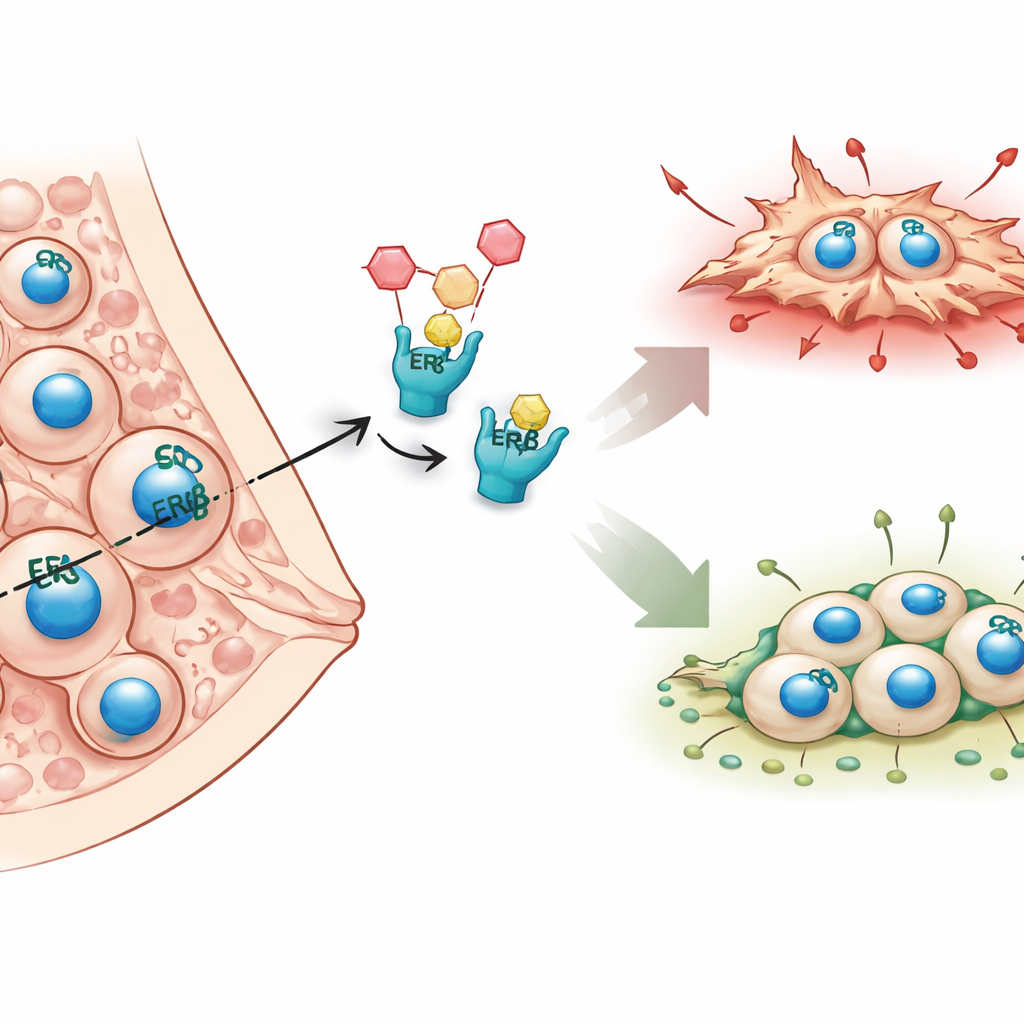
قراءة دليل تعليمات خلية السرطان
لكشف تأثير ERβ، استخدم الباحثون طريقتين قويّتين للتسلسل على خطوط خلايا سرطان الثدي الالتهابي. تُحدد طريقة واحدة، ChIP-seq، الأماكن الدقيقة التي يرتبط فيها ERβ بالحمض النووي، كعلامة على صفحات وأسطر محددة في دليل تعليمات الخلية. تقيس الطريقة الأخرى، RNA-seq، أي الجينات تُرفع أو تُخفض عندما يكون ERβ حاضرًا أو غائبًا أو مفعلاً بواسطة دواء انتقائي. من خلال مقارنة مجموعات البيانات هذه، وجدوا آلاف المواقع على الحمض النووي المرتبطة بـERβ، ومعظمها ليس فقط عند مفاتيح تشغيل وإيقاف الجينات بل داخل الجينات أو بينهما، مما يشير إلى سيطرة واسعة النطاق. واكتشفوا أيضًا أن ERβ غالبًا ما يعمل بالتعاون مع عائلات من عوامل النسخ الأخرى، مكوّنًا مركبات تقرر جماعيًا أي الجينات تُسكَت أو تُفعّل.
إعادة توصيل النمو والحركة والأيض
أظهر التحليل المتكامل أن ERβ يميل إلى تخفيف نشاط الجينات التي تعزز حركة الخلية والتحول الشكلي والغزو، لا سيما تلك المرتبطة بالهياكل الداعمة من الأكتين وإشارات Rho GTPase—مسارات معروفة بدفعها للانبثاث. وفي الوقت نفسه، يدعم ERβ برامج جينية مرتبطة بنمو الأنسجة وتمايز الخلايا، ما يدفع خلايا السرطان نحو حالة أكثر استقرارًا وأقل عدوانية. كشفت الدراسة أيضًا دورًا مفاجئًا لـERβ في تعديل مسارات الأيض، خصوصًا تلك التي تشمل الأحماض الدهنية والفوسفوليبيدات، وهي وقود ولبِنات بناءٍ رئيسية للأورام سريعة النمو. ومن المهم أن هذه التأثيرات لوحظت ليس فقط في خلايا مهندسة لإنتاج ERβ بكميات كبيرة ولكن أيضًا في خلايا ذات مستويات طبيعية من المستقبل، مما يؤكد صلتها بالعالم الواقعي.
المرسلات الصغيرة من الحمض النووي الريبوزي والأثر السريري
بعيدًا عن الجينات المشفرة للبروتين، فحص الفريق الميكروـRNA—جزيئات RNA صغيرة تعمل على ضبط تعبير الجينات بدقة. وجدوا عشرات الميكروـRNA التي تغيرت مستوياتها عند إزالة ERβ أو استعادته، والعديد منها مرتبط بقمع الأورام في سرطان الثدي. من خلال ربط هذه الميكروـRNA بجينات مستهدفاتها، أوضح المؤلفون أن ERβ يتحكم ببعض محفزات السرطان بشكل غير مباشر عبر شبكة تنظيمية متعددة الطبقات. ثم انتقلوا إلى بيانات المرضى، مفحصين أورامًا من أشخاص مصابين بسرطان ثدي التهابي وغير التهابي. كانت عدة جينات خاضعة لسيطرة ERβ مرتبطة بشكل قوي ببقاء المرضى: مستويات عالية لبعضها (مثل SERPINA1 وHSPB8) تنبأت بنتائج أفضل، بينما ارتبطت مستويات عالية لأخرى (مثل PITX1 وHOMER3) ببقاء أسوأ. هذا يضع هذه الجزيئات التالية كعلامات محتملة للتكهن وكأهداف دوائية مستقبلية.
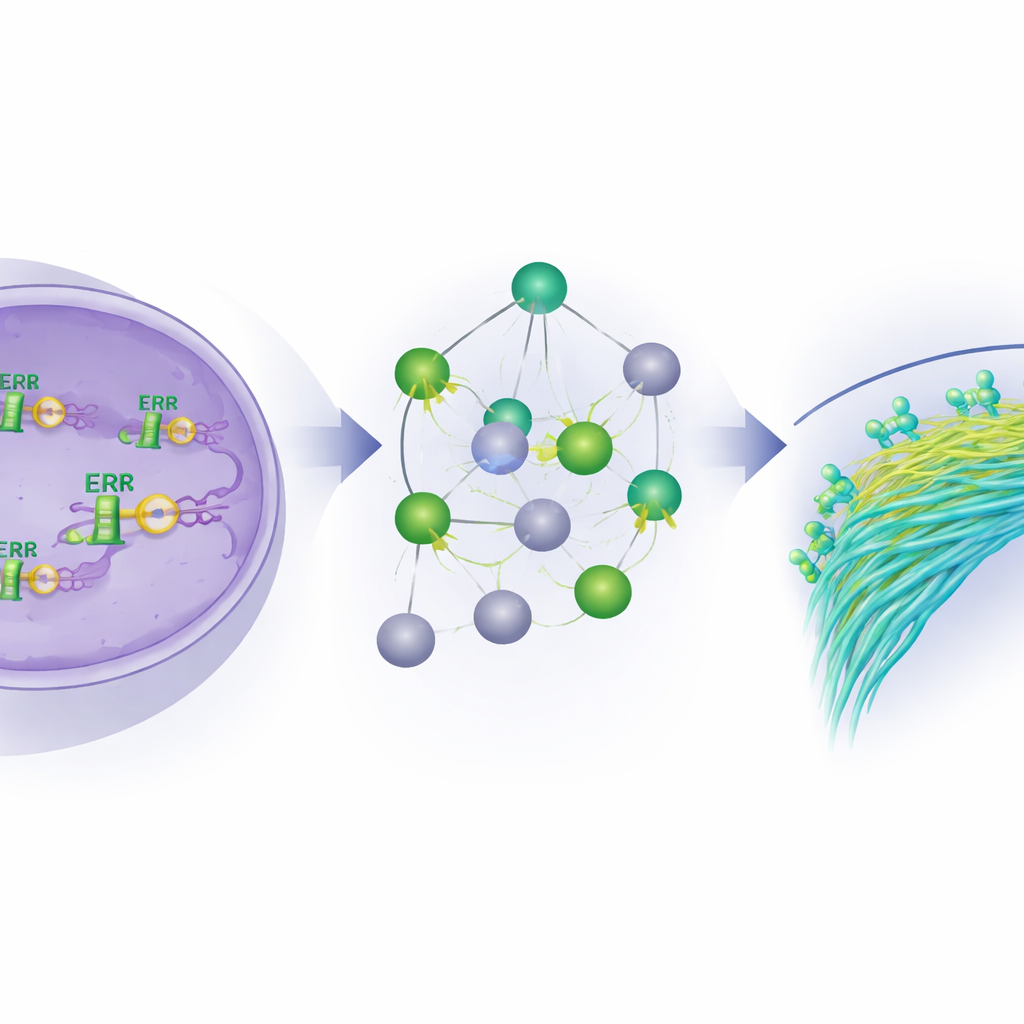
من الكبح الجزيئي إلى العلاجات المستقبلية
إجمالًا، تصور الدراسة ERβ كمكبح مركزي لسلوك الغزو في خلايا سرطان الثدي الالتهابي. من خلال ارتباطه بالحمض النووي، وتعاونه مع منظِّمين آخرين، وتشكيله لشبكات الجينات والميكروـRNA، يخمد ERβ البرامج التي تدفع هجرة الخلايا والانبثاث بينما يعزز حالات أكثر استقرارًا وتمايزًا ويعيد ضبط أيض السرطان. وللمرضى، يوحي ذلك بأن أدوية تفعّل ERβ أو تُثبِط أهدافه التالية الرئيسية—خصوصًا تلك المشاركة في حركة الخلايا واستخدام الأحماض الدهنية—قد تشكل أساس علاجات جديدة أكثر دقة لهذا المرض الصعب المعالجة.
الاستشهاد: Tastsoglou, S., Karagounis, I.V., Miliotis, M. et al. Estrogen receptor β target gene expression reveals novel repressive functions in aggressive breast cancer. npj Breast Cancer 12, 38 (2026). https://doi.org/10.1038/s41523-026-00905-4
الكلمات المفتاحية: سرطان الثدي الالتهابي, مستقبل الاستروجين بيتا, الانبثاث, تنظيم الجينات, أيض السرطان