Clear Sky Science · ar
التوصيل المشترك للكيموكين CXCL9 واللّيغاند المساعد TNFSF9 بواسطة الخلايا الجذعية الميزنشيمية يعيد برمجة البيئة المناعية لسرطان الثدي ثلاثي السلبيات
لماذا تهم هذه المقاربة الجديدة لسرطان الثدي
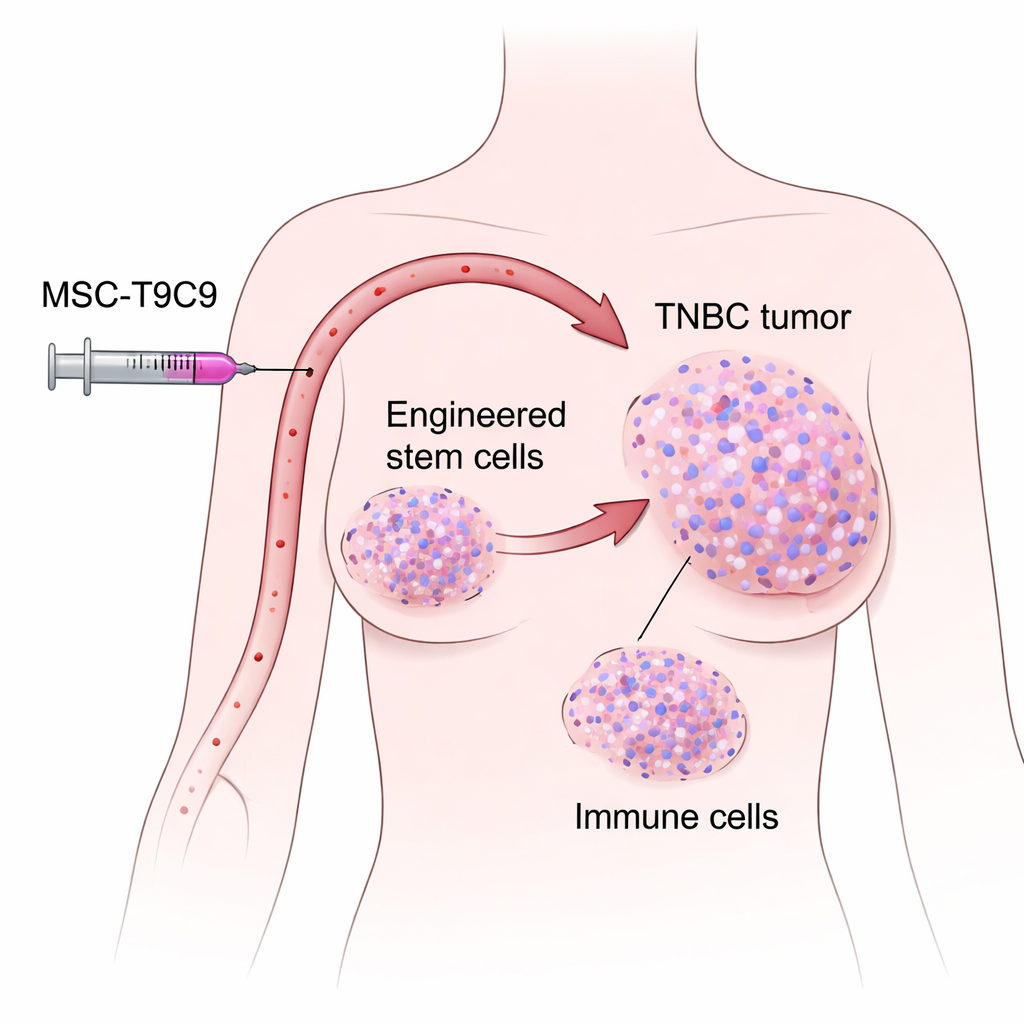
يعد سرطان الثدي ثلاثي السلبيات واحداً من أخطر أشكال سرطان الثدي لأنه ينمو بسرعة، وينتشر مبكراً، ويفتقر إلى الأهداف الهرمونية الشائعة التي تعتمد عليها العديد من الأدوية. أثارت العلاجات المناعية آمالاً كبيرة، لكن في كثير من المرضى لا تدخل خلايا الدفاع في الجسم إلى الورم بأعداد كافية لتحقيق تأثير. تستكشف هذه الدراسة استراتيجية مبتكرة: استخدام خلايا حية ناقلة كـ"شاحنات توصيل" موجهة تجلب إشارات معززة للمناعة مباشرة إلى الأورام التي يصعب علاجها، مما قد يجعل عدد أكبر من المرضى مؤهلين للعلاجات المناعية الفعالة.
سرطان عنيد مع مساعدة مناعية قليلة
العلاجات القياسية لسرطان الثدي ثلاثي السلبيات—الجراحة، والعلاج الكيميائي، والإشعاع—غالباً لا تمنع الانتكاس، ولا يزال متوسط البقاء للمرض المتقدّم أقل من عامين. أحد الأسباب الرئيسية هو أن العديد من هذه الأورام "باردة"، أي أنها تحتوي على قليل من خلايا المناعة المقاتلة للسرطان. أظهرت قواعد بيانات مرضى كبيرة أن الأشخاص الذين تصنع أورامهم طبيعياً كميات أعلى من جزيئين متعلقين بالمناعة، CXCL9 وTNFSF9، يميلون إلى العيش لفترة أطول ويملكون خلايا T وخلايا القاتلة الطبيعية (NK) أكثر داخل أورامهم. CXCL9 هو إشارة كيميائية تستدعي خلايا المناعة إلى الأنسجة، بينما يعمل TNFSF9 كمفتاح "تشغيل" إضافي يساعد تلك الخلايا على الهجوم بقوة أكبر. الاقتراح كان أن رفع كلا الإشارتين مباشرة داخل الأورام قد يغير المعادلة لصالح النظام المناعي.
تحويل الخلايا الجذعية إلى شاحنات توصيل ذكية
ركز الباحثون على الخلايا الجذعية الميزنشيمية المأخوذة من أشرطة الحبل السري البشرية المتبرع بها. لهذه الخلايا خاصية مفيدة: عندما تُحقن في مجرى الدم لالفئران الحاملة لأورام ثدي، تتوجه طبيعياً نحو مواقع الأورام وتبقى هناك لأيام، مع تجنب الأعضاء الطبيعية إلى حد كبير. قام الفريق بتعديل هذه الخلايا وراثياً لإطلاق CXCL9 وعرض TNFSF9 على سطحها، مكوين نظام علاج خلوي ذا غرضين أطلقوا عليه MSC‑T9C9. أظهرت الاختبارات المخبرية أن الخلايا المعدلة أفرزت مستويات عالية من CXCL9 ونشّطت بشدة خلايا T وخلايا NK لدى الفئران، دون تغيير سلوك نموها أو إحداث أورام بمفردها. هذا جعلها مرشحة واعدة كمقويات مناعية موجهة.
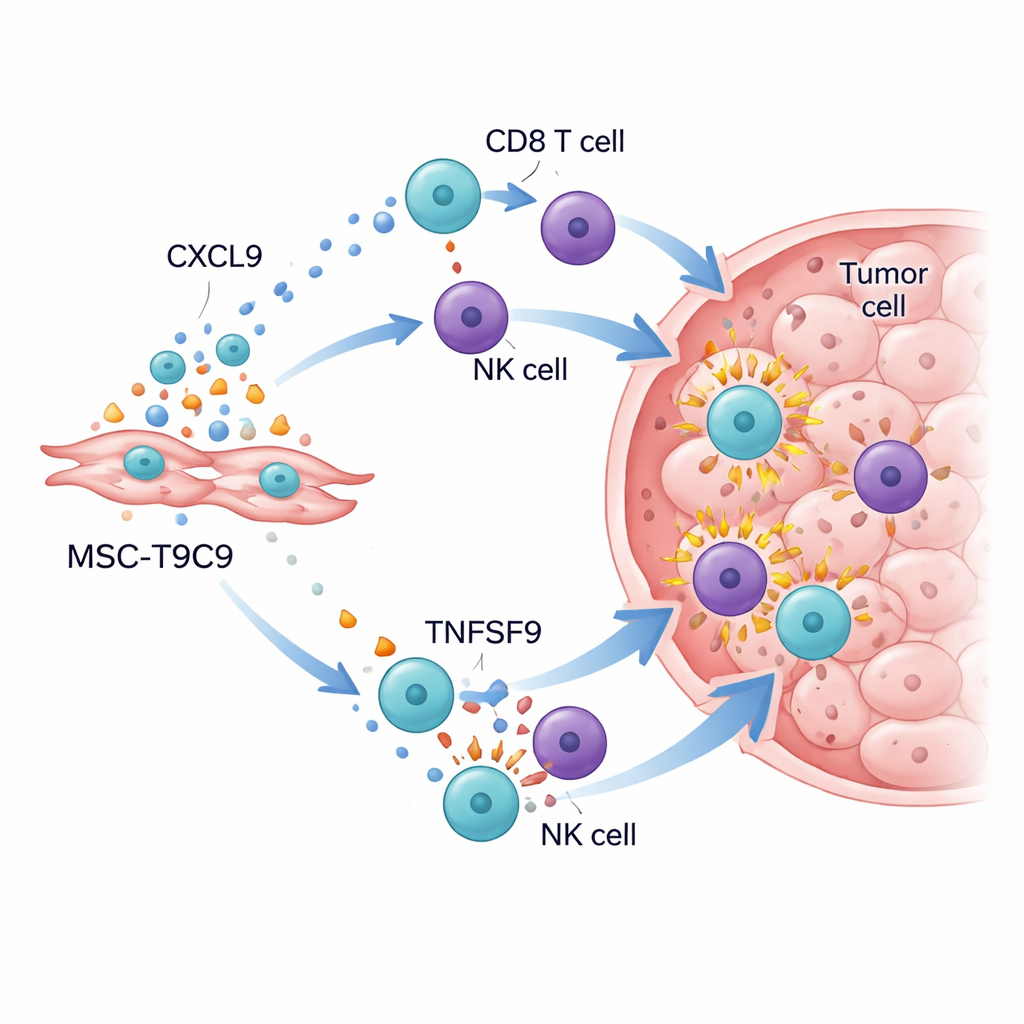
إيقاظ ساحة المعركة المناعية داخل الورم
عندما عُطيت الخلايا المهندسة لفئران تحمل أورام ثدي ثلاثية السلبيات، كانت النتائج ملفتة. في الفئران ذات الجهاز المناعي السليم، أدت الحقن المتكررة بـMSC‑T9C9 إلى تباطؤ كبير في نمو الأورام وزيادة موت الخلايا السرطانية، بينما كانت للخلايا الجذعية الضابطة تأثير ضئيل. أظهر التحليل التفصيلي للأورام ارتفاعاً دراماتيكياً في عدد خلايا CD8 القاتلة وخلايا NK، إلى جانب مستويات أعلى من جزيئات الهجوم القوية مثل جرانزيم B، والإنترفيرون‑γ، وعامل نخر الورم‑α، والإنترلوكين‑2. وفي الوقت نفسه، تغيرت بيئة الورم بعيداً عن الحالة الكابحة: زاد عدد البلاعم الالتهابية المفيدة، وعلى الرغم من استمرار وجود الخلايا التائية التنظيمية، فقد طغت عليها الموجة الجديدة من الخلايا المقاتلة. في الفئران المناعية الناقصة، حيث تفتقد خلايا T وNK، لم يبطئ MSC‑T9C9 نمو الورم، مما يؤكد أن فائدته تعتمد على حشد دفاعات الجسم الذاتية.
تهيئة الأورام لعلاج نقاط التفتيش المناعية
تُطلق أدوية المناعة الحديثة مثل الأجسام المضادة المضادة لـPD‑1 "الفرامل" الجزيئية عن خلايا T، لكنها تعمل أفضل عندما تكون هناك خلايا T كافية بالفعل داخل الورم. وجدت الدراسة أن MSC‑T9C9 لم يجذب المزيد من خلايا CD8 إلى الأورام فحسب، بل دفعها أيضاً إلى حالة نشطة للغاية ومع ذلك حساسة للفرامل، تتميز بمستقبل PD‑1. في نموذج فأري، أدى الجمع بين MSC‑T9C9 ودواء مضاد لـPD‑1 إلى أقوى تقلص في الورم وأطول مدة بقاء مقارنة بأي علاج وحده. دعمت تحليلات مجموعات بيانات مرضى البشر هذه الفكرة: كان المرضى الذين لديهم مستويات مشتركة أعلى من TNFSF9 وCXCL9 أكثر عرضة للاستفادة من علاجات حجب نقاط التفتيش، مما يوحي بأن نفس البيولوجيا قد تنطبق على البشر.
السلامة والآفاق المستقبلية
أي علاج يعزز المناعة يثير قلقاً بشأن آثار جانبية خطيرة مثل الالتهاب الواسع أو تلف الأعضاء. بشكل مشجع، حافظت الفئران التي تلقت MSC‑T9C9 على وزن وسلوك طبيعيين، ولم تظهر إصابات واضحة في الأعضاء الرئيسية، وكانت نتائج اختبارات الدم والكبد والكلى طبيعية. والأهم أن الزيادة في النشاط المناعي كانت محصورة إلى حد كبير داخل الورم نفسه، ولم ترتفع إشارات الالتهاب في مجرى الدم. بينما هناك حاجة إلى مزيد من العمل قبل البدء بالتجارب البشرية—بما في ذلك اختبارات في نماذج أكثر واقعية وتحديد جرعات دقيقة—تشير هذه الدراسة إلى أن توجيه خلايا جذعية مهندسة إلى الأورام لاستدعاء وتفعيل خلايا المناعة قد يوفر وسيلة موجهة وأكثر أماناً لتحويل سرطانات الثدي ثلاثية السلبيات "الباردة" إلى أورام "حارة" تستجيب بشكل أفضل للعلاج المناعي.
الاستشهاد: Ye, P., Wen, Y., Liu, R. et al. Co-delivery of chemokine CXCL9 and costimulatory ligand TNFSF9 by mesenchymal stem cells reprograms the immune microenvironment for triple-negative breast cancer. npj Breast Cancer 12, 30 (2026). https://doi.org/10.1038/s41523-026-00893-5
الكلمات المفتاحية: سرطان الثدي ثلاثي السلبيات, العلاج المناعي, الخلايا الجذعية الميزنشيمية, البيئة الميكروية للورم, حجب نقاط التفتيش المناعية