Clear Sky Science · ar
إنترلوكين-1α المشتق من المضيف يقود قمع المناعة الورمية عبر إعادة برمجة الخلايا النخاعية المرتبطة بالورم
لماذا يهم هذا البحث مرضى السرطان
غيّرت العلاجات المناعية مسار علاج بعض السرطانات، لكن العديد من أورام الثدي لا تزال تتملص من جهاز المناعة. يستكشف هذا البحث سبباً أقل شهرة: جزيء إشارة يُدعى إنترلوكين‑1α (IL‑1α) يُنتَج ليس من قِبل الخلايا السرطانية نفسها بل من خلايا طبيعية في الجسم. يبيّن المؤلفون أن IL‑1α المشتق من المضيف يمكنه بهدوء تحويل خلايا المناعة إلى حلفاءٍ للورم، وأن حجب هذا الإشارة في الفئران يؤدي أحياناً إلى تقلص الأورام الثديية أو زوالها. قد يساعد فهم هذا التحول الأطباء على تصميم علاجات تجعل المناعة المضادة للسرطان أكثر فعالية لسرطان الثدي.
مؤثر خفي في حَيّ الورم
لا تنمو السرطانات بمفردها؛ بل تعيش في «حي» مزدحم من خلايا مناعية وأوعية دموية ونسيج رابط يُعرف بالبيئة الدقيقة للورم. من بين أهم السكان هناك خلايا النخاع، خاصة البلعميات، التي يمكن أن تهاجم الورم أو تحميه. تُقسِم الكتب المدرسية الكلاسيكية البلعميات إلى M1 (مقاتلة للورم) وM2 (مساندة للورم)، لكن الأورام الحقيقية تحتوي على درجات عديدة بين هذين القطبين. ركز المؤلفون على IL‑1α، جزيء عادة ما تنتجه الأنسجة غير السرطانية، لطرح سؤال مفاده هل توجّه هذه الإشارة الصادرة من المضيف الخلايا النخاعية الواردة إلى أدوار مفيدة أم ضارة داخل أورام الثدي.
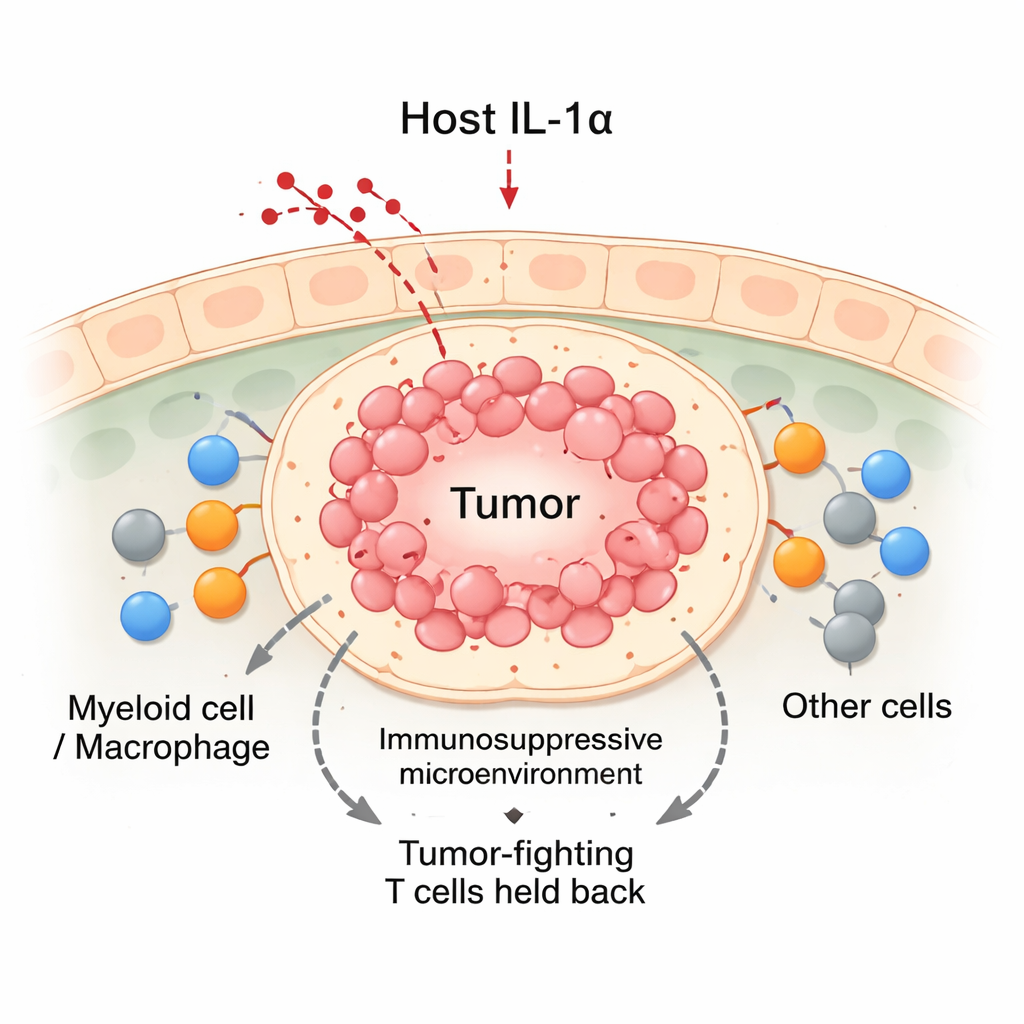
إيقاف IL‑1α يحوّل الميزان ضد الأورام
باستخدام نماذج فأرية لسرطان الثدي، قارن الفريق الحيوانات الطبيعية مع أخرى مُهندَسة وراثياً لالتقاط IL‑1α. عند زرع خلايا سرطان الثدي في الغدد الثديية، نمت الأورام في الفئران العادية باستمرار. بالمقابل، نمت الأورام في الفئران الخالية من IL‑1α مبدئياً لمدة نحو أسبوعين ثم تراجعت كثيراً. احتوت هذه الأورام المتراجعة على عدد أكبر إجمالاً من الخلايا المناعية، بما في ذلك ازدياد لخلايا CD8 «القاتلة» وخلايا النخاع. رغم أن الفئران الخالية من IL‑1α كان لديها عدد أقل من كريات الدم البيضاء في الدوران، فإنها جمعت عدداً أكبر من الخلايا المناعية داخل موقع الورم. أظهرت التحليلات التفصيلية أن خلايا CD8 المتسللة في أورام الفئران الخالية من IL‑1α كانت أكثر نشاطاً، منتجةً مستويات أعلى من الجزيئات القاتلة للورم وتُظهر علامات أقل للاستنفاد.
كيف يعيد IL‑1α تشكيل الخلايا النخاعية المرتبطة بالورم
لفهم ما يفعله IL‑1α على المستوى الخلوي، استخدم الباحثون تسلسل RNA لخلايا فردية لفحص آلاف الخلايا من الأورام. اكتشفوا أن مجموعة صغيرة فقط من البلعميات المرتبطة بالورم—المميزة بمستقبل يُدعى CX3CR1—كانت تنتج IL‑1α. في الفئران العادية، ناضت العديد من الوحيدات الواردة لتصبح هذه البلعميات الموجبة لـCX3CR1، والتي ارتبطت بسلوك مثبط للمناعة. في الفئران الخالية من IL‑1α، تعطّل هذا الطريق الناضج. وبدلاً من ذلك، كانت الخلايا النخاعية أكثر ميلاً لأن تصبح بَلْعَمات التهابية موجبة لـiNOS، ملف مرتبط بنشاط مضاد للورم. وظيفياً، كانت خلايا النخاع من أورام الفئران الخالية من IL‑1α أقل قدرة على استحثاث مكابح مثل PD‑1 وCTLA‑4 على الخلايا التائية، وأظهرت قدرة أضعف على كبح تكاثر الخلايا التائية.
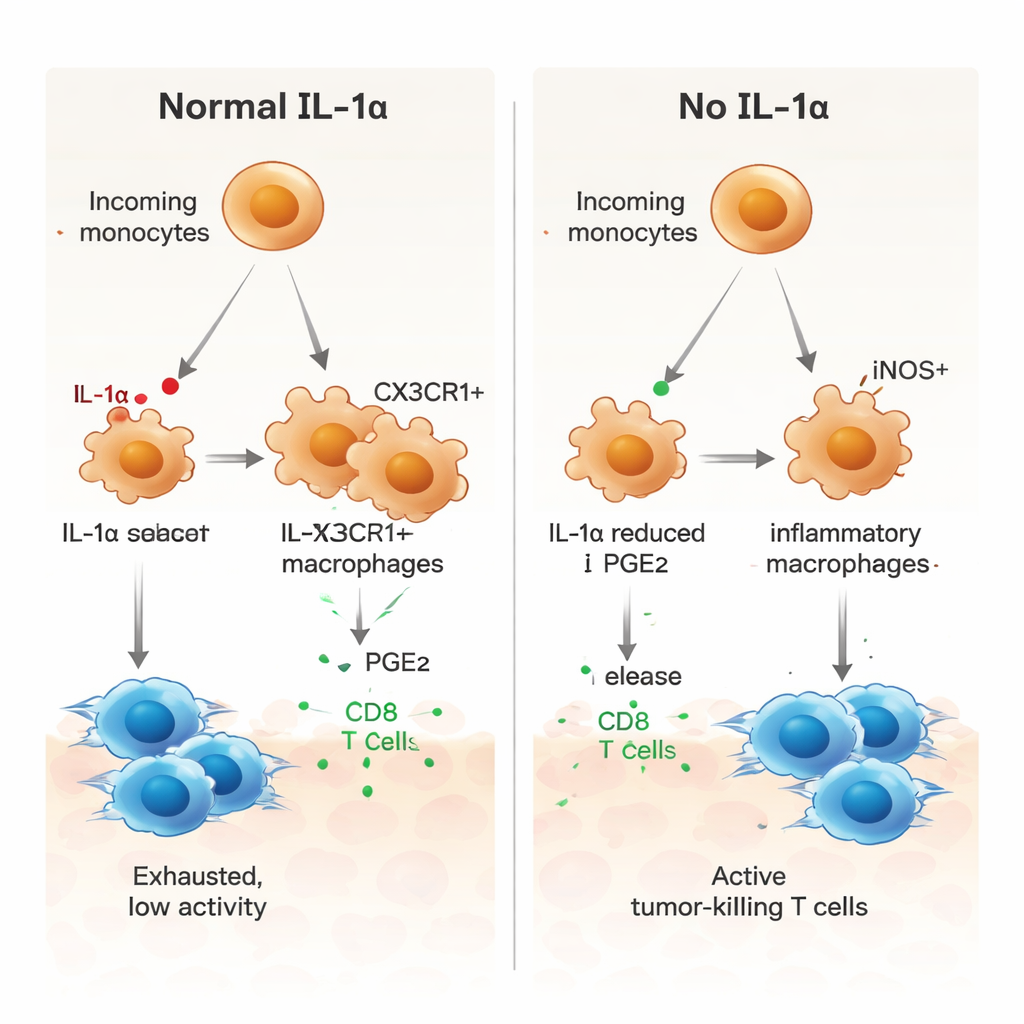
دور محوري لرسول دهني، PGE2
سأل المؤلفون بعد ذلك كيف يدفع IL‑1α الخلايا النخاعية نحو حالة داعمة للورم. أشارت تحليلات التواصل في بيانات الخلايا المفردة إلى عدة مسارات إشارية، منها مسار يتضمن بروستاجلاندين E2 (PGE2)، وهو رسول دهني معروف بتعزيز كبت المناعة. في الأورام الخالية من IL‑1α، عبّرت البلعميات عن مستويات أقل من مستقبلات عامل نمو البلعميات (M‑CSF) ومستقبلات TGF‑β ومستقبل لـPGE2، وأنتجت الخلايا الداعمة المجاورة كميات أقل من الإنزيمات المنتجة لـPGE2. في مزروعات مخبرية، أظهرت البلعميات المشتقة من نخاع العظم لدى الفئران الخالية من IL‑1α نمطاً أكثر التهابية، مع iNOS أعلى وCX3CR1 أقل. أعاد إضافة PGE2 هذا التحول واستعدت نمطاً أكثر قمعية، بينما دفعت معاوقة PGE2 البلعميات الطبيعية نحو حالة مؤيدة للالتهاب. كما حفزت البلعميات الخالية من IL‑1α تكاثر خلايا CD8 التائية المحددة للورم بشكل أقوى، وهو تأثير خفّته إعادة إضافة PGE2.
جسر النتائج الفأرية إلى المناعة البشرية
ليروا ما إذا كانت بياناتهم في الفأر تنعكس في البيولوجيا البشرية، قارن الفريق طرق التعبير الجيني لمجموعات البلعميات الفأرية المختلفة بمجموعة كبيرة من الخلايا النخاعية البشرية المُدعاة نحو حالات متنوعة في المختبر. شَبَهت مجموعات البلعميات من أورام الفئران العادية خلايا بشرية دُفِعت نحو حالات شبيهة بـM2 ومُثبِطة للمناعة بواسطة جزيئات مثل IL‑10 وIL‑4 والغلوكوكورتيكويدات. بالمقابل، تطابقت نفس المجموعات من أورام الفئران الخالية من IL‑1α مع خلايا بشرية في حالات أكثر التهابية وأقل قمعاً. ولاحظ الباحثون أن أنماط الجينات المرتبطة بإشارات PGE2 كانت مُثرَّية في البلعميات المعتمدة على IL‑1α لكنها غائبة عند فقدان IL‑1α، مما يعزز فكرة أن IL‑1α وPGE2 يعملان معاً لبناء موضع قمعي للمناعة.
ماذا قد يعني هذا لعلاج سرطان الثدي في المستقبل
بعبارة بسيطة، تشير هذه الدراسة إلى أن جزيئاً مصدره المضيف، IL‑1α، يمكنه أن يُمرِر إشارات لبعض البلعميات لتَحمِي الورم وتكبُت خلايا CD8 القاتلة، جزئياً عبر إشارات PGE2. عند إزالة IL‑1α في الفئران، تتحول البلعميات إلى حالة أكثر التهابية ومهاجمة للورم، وتصبح خلايا CD8 أكثر نشاطاً، وغالباً ما تُرفض أورام الثدي المزروعة. وبما أن العلاجات المناعية الحالية تهدف بالفعل إلى إعادة تنشيط الخلايا التائية المستنفدة، فإن الجمع بينها وبين مقاربات تحجب IL‑1α أو مسار PGE2 التالي قد يزجّ بالبيئة الدقيقة للورم لصالح جهاز مناعة المريض. ورغم الحاجة لمزيد من العمل لاختبار الأمان والفعالية لدى البشر، تبرز هذه النتائج IL‑1α كهدف واعد لجعل سرطان الثدي أكثر عُرضة للهجوم المناعي.
الاستشهاد: Keerthi Raja, M.R., Gupta, G., Atkinson, G. et al. Host-derived interleukin-1α drives tumor immunosuppression by reprogramming tumor-associated myeloid cells. npj Breast Cancer 12, 26 (2026). https://doi.org/10.1038/s41523-026-00890-8
الكلمات المفتاحية: مناعـة سـرطان الثدي, البيئة الدقيقة للورم, البلعميات, إنترلوكين-1 ألفا, بروستاجلاندين E2