Clear Sky Science · ar
تنظيم الميكروبات لجزيئات الإشارات المرتبطة بالإجهاد ودورها في الصحة والمرض
كيف يشكّل سكان الأمعاء الصغار استجابتنا للإجهاد
غالبًا ما نفكر في الإجهاد كأمر يحدث في أدمغتنا، لكن هذه المقالة تبيّن أن بعض أهم اللاعبين في استجابة الإجهاد يعيشون في أمعائنا. الميكروبات التي تؤوي أمعاؤنا تفعل أكثر بكثير من مجرد مساعدة الهضم: فهي تستطيع صنع هذه الهرمونات وتحليلها وإعادة تشكيلها — الهرمونات نفسها التي تتحكم في كيفية استجابة أجسامنا للضغط والخوف والألم. قد يفتح فهم هذه الشراكة الخفية سبلًا جديدة لتخفيف حالات مثل داء الأمعاء الالتهابي والاكتئاب وغيره من الأمراض المرتبطة بالإجهاد.
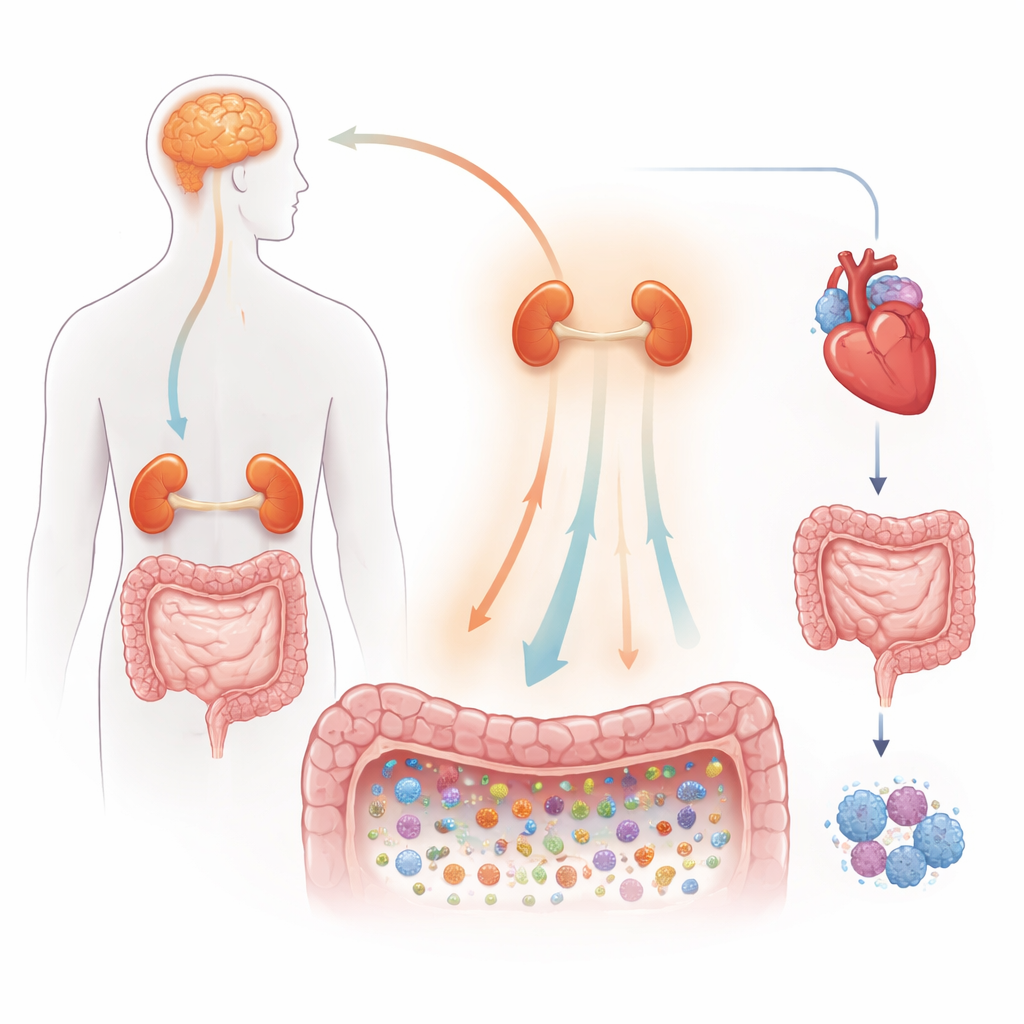
جهاز الإنذار المدمج في الجسم
يبدأ المؤلفون بتوضيح كيفية عمل استجابة الإجهاد عادةً. عندما نواجه تحديًا، ينشط الدماغ سلسلة قيادة تمتد عبر الغدة النخامية والغدد الكظرية، لتفيض الجسم برسائل كيميائية مثل الكاتيكولامينات الشبيهة بالأدرينالين والستيرويدات المسماة الجلوكوكورتيكويدات. ترفع هذه الإشارات معدل ضربات القلب، وتحوّل تدفق الدم، وتغير حركة الأمعاء، وتعدّل الجهاز المناعي لحالة "القتال أو الهرب". الأعصاب التي تتصل مباشرة بالجهاز الهضمي توفر مسارًا سريعًا للإشارات إلى الأمعاء، فتشد أو ترخّي الحاجز المعوي وتغيّر البيئة المحلية التي تعيش فيها الميكروبات. هذا يجعل الأمعاء مفترق طرق أساسيًا حيث تلتقي بيولوجيا الإجهاد والميكروبيوم باستمرار.
الميكروبات تستمع وتتواصل مع إشارات الإجهاد
تكشف الأبحاث على مدى عدة عقود أن العديد من البكتيريا يمكنها استشعار واستخدام موادنا الكيميائية المرتبطة بالإجهاد. أوضحت تجارب مبكرة أن بعض بكتيريا الأمعاء والبكتيريا الممرِضة تنمو أسرع وتصبح أكثر عدوانية عند تعرضها لكاتيكولامينات مثل النورإبينفرين والإبينفرين. وأظهرت أعمال أخرى أن البكتيريا قادرة على امتصاص هذه الجزيئات، وتحويلها إلى أشكال جديدة، أو حتى إنتاج مركبات مماثلة بنفسها من أحماض أمينية مثل التيروزين. في الوقت نفسه، كثيرًا ما تقوم إنزيمات المضيف "بإطفاء" الكاتيكولامينات عن طريق إلحاق مجموعات كيميائية صغيرة بها؛ والبكتيريا المعوية المزوّدة بالأدوات المناسبة يمكنها قص هذه المجموعات مجددًا، فتستعيد الشكل النشط. في الفئران الخالية من الميكروبات، تكون معظم رسائل الإجهاد في الأمعاء محبوسة في شكل غير نشط، لكن إدخال بكتيريا محددة يعيد مجموعة الشكل النشط، مما يُظهر أن الميكروبات تتحكم مباشرة في مقدار توافر هذه الإشارات.
إعادة تشكيل الستيرويدات المرتبطة بالإجهاد من الداخل
ينتقل الاستعراض بعد ذلك إلى الجلوكوكورتيكويدات، وهي الهرمونات الستيرويدية المعروفة بتهدئة الالتهاب ومساعدة الجسم على التعامل مع الإجهاد المستمر. تدخل كميات صغيرة من هذه الهرمونات الأمعاء عبر مجرى الدم أو تُصنع محليًا في بطانة الأمعاء، حيث تلتقي بمجتمعات بكتيرية كثيفة. تحمل العديد من ميكروبات الأمعاء إنزيمات متخصصة يمكنها تقليم أو إعادة ترتيب أو اختزال هذه الجزيئات الستيرويدية. بعضها يقطع سلاسل جانبية ليحوّلها إلى أندروجينات، التي تعمل أكثر كهرمونات جنسية ويمكن أن تؤثر على ضغط الدم وحتى على السرطانات الحساسة للهرمونات. والبعض الآخر يزيل مجموعات كيميائية معينة، مما يضعف قدرة الهرمون على الارتباط بمستقبله، أو يقلّص بنية الجزيء بحيث لا يمكن إعادة تدويره إلى أشكال قوية. وهناك من يعكس خطوات "إلغاء النشاط" التي يقوم بها الجسم عن طريق إزالة مجموعات الكبريتات أو مجموعات شبيهة بالسكر المرتبطة بالجزيء، محوّلًا الستيرويدات مجددًا إلى شكل نشط ينتقل في الدورة الدموية. معًا، تجعل هذه الأعمال الميكروبيوم زر تحكم متحركًا في قوة وتوازن الستيرويدات.
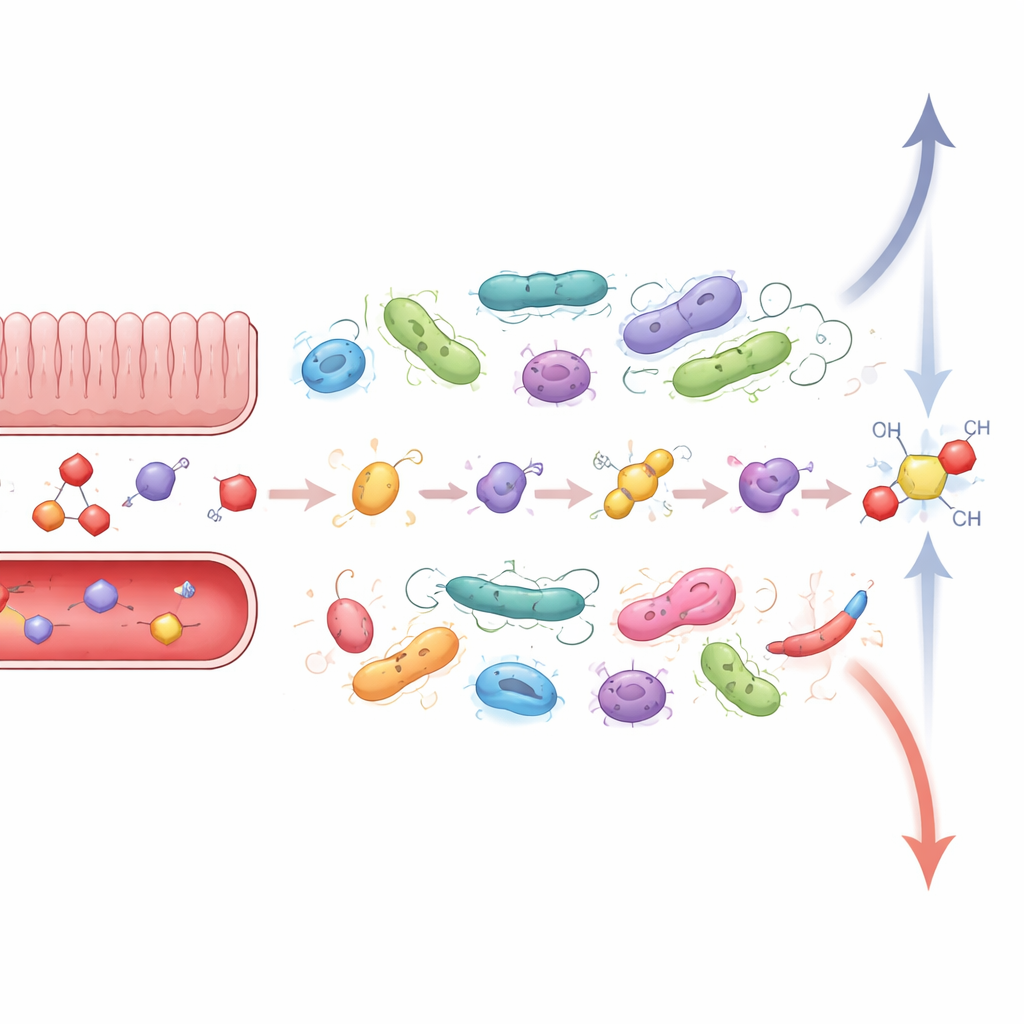
عندما يتغذى الإجهاد والالتهاب والميكروبات على بعضهم البعض
تزداد أهمية هذه التبادلات الكيميائية الحميمة في الأمراض التي يكون فيها كل من الإجهاد وميكروبات الأمعاء مضطربين بالفعل. داء الأمعاء الالتهابي مثال بارز: يظهر لدى المرضى التهاب معوي مزمن، وتغيّر في التجمعات الميكروبية، وحساسية متزايدة لإجهادات الحياة. يمكن لهرمونات الإجهاد أن تضعف الحاجز المعوي، مما يسمح بمزيد من الميكروبات ومنتجاتها بالتسرب والتحفيز المفرط للجهاز المناعي. في الوقت نفسه، يرتبط داء الأمعاء الالتهابي بازدهار أنواع قادرة على إعادة تشكيل الكورتيزول والستيرويدات ذات الصلة، فضلًا عن فقدان بكتيريا تصنع الأحماض الدهنية القصيرة السلسلة، وهي نواتج تخمير صغيرة تساعد عادة على إحكام الحاجز وتهدئة الالتهاب. تشير دراسات حيوانية إلى أن هذه التحولات الميكروبية يمكن أن تضخم اختلالات الهرمونات والنشاط المناعي، مما يقفل المرضى في حلقة مفرغة حيث يزيد الإجهاد من شدة المرض المعوي ويضاعف المرض المعوي من حدة الإجهاد.
سبل جديدة لتهدئة حلقة الأمعاء–الإجهاد
بما أن الميكروبات تجلس عند مفترق إشارات الإجهاد والالتهاب، فهي أهداف جذابة لعلاجات جديدة. تسلط المقالة الضوء على أعمال تُظهر أن الأنظمة الغذائية الغنية بالألياف مثل الإينولين يمكن أن تعزز نواتج التخمر المفيدة، وتخفف الالتهاب المعوي، وتحدّ من بعض أضرار الإجهاد في نماذج داء الأمعاء الالتهابي. وُجد أن سلالات بروبيوتيك من جنس لاكتوباسيلس تقوّي الحاجز المعوي، وتقلل من ارتفاعات هرمونات الإجهاد الناتجة عن الإجهاد، وتخفض حساسية الألم في الحيوانات. يمكن أن يقلّل التوصيل المباشر للأحماض الدهنية قصيرة السلسلة إلى القولون من السلوكيات المشابهة للقلق في الفئران ويخفّض استجابات الكورتيزول للإجهاد الاجتماعي لدى البشر. تشير هذه النجاحات المبكرة إلى أن بروبيوتيكات ومُعدّات مسبقة وحَوامض ميكروبية مصممة بعناية قد تساعد في إعادة ضبط استجابة الإجهاد من خلال إعادة تشكيل تعامل الأمعاء مع الهرمونات.
ماذا يعني هذا للصحة اليومية
ختمًا، يجادل المؤلفون بأن ينبغي اعتبار ميكروبات الأمعاء شركاء فاعلين في بيولوجيا الإجهاد لدينا، لا مجرد متفرجين سلبيين. من خلال صنع وتعديل وإعادة تدوير جزيئات الإشارات المرتبطة بالإجهاد، يمكن للميكروبيوم أن يؤثر في قوة استجابتنا للتحديات، وسرعة تعافينا، ومدى احتمال أن يدفعنا الإجهاد إلى مرض مزمن. هذا لا يعني أن هناك ميكروبًا واحدًا "ساحرًا" سيعالج الإجهاد، لكنه يوحي بأن حماية ورعاية نظام أمعاء صحي قد تكون واحدة من أقوى الأدوات المتاحة لبناء القدرة على التحمل. ومع رسم الباحثين لهذه التفاعلات بين الميكروبات والهرمونات بمزيد من التفصيل واختبارها لدى البشر، قد تصبح الاستراتيجيات اليومية الداعمة لصحة الأمعاء جزءًا أساسيًا من إدارة الإجهاد والمزاج والحالات الالتهابية.
الاستشهاد: Sie, C., Tropini, C. Microbial regulation of stress-associated signaling molecules and its role in health and disease. npj Biofilms Microbiomes 12, 65 (2026). https://doi.org/10.1038/s41522-026-00932-w
الكلمات المفتاحية: ميكروبيوم الأمعاء, هرمونات الإجهاد, محور الميكروبيوتا-المعِدة-الدماغ, داء الأمعاء الالتهابي, علم الغدد الصغرى الميكروبي