Clear Sky Science · ar
بكتيريا لاكتوباسيلس الناقلة للنانوبديز تحسن إنتاجية دجاج التسمين في وجود التهاب معوي نخرِي تحت السريري مع تغيُّرات مرافقة في الميكروبيوم والترانسكريبتوم
لماذا تهم صحة أمعاء الدجاج على طبق عشاءك
تُواجه مزارع الدجاج الحديثة توازناً دقيقاً: عليها تربية مليارات الطيور بكفاءة مع تقليل استخدام المضادات الحيوية التي قد تُسهِم في ظهور عدوى مقاومة للأدوية لدى البشر. أحد أكبر التهديدات المخفية لدجاج التسمين هو مرض معوي يُسمى الالتهاب المعوي النخري تحت السريري. تبدو الطيور المصابة بهذا المرض سليمة في المظهر غالباً لكنها تنمو ببطء وتستهلك علفاً أكثر لتصل إلى نفس الوزن، مما يزيد بهدوء من تكلفة وبصمة إنتاج لحم الدجاج على البيئة. تستكشف هذه الدراسة نهجاً بروبيوتيكياً مستهدَفاً جديداً يزوِّد البكتيريا المفيدة بشظايا صغيرة من الأجسام المضادة لتحييد السموم المسببة للمرض مباشرة داخل الأمعاء.
مرض معوي مكلف وغالباً غير ظاهر
ينجم الالتهاب المعوي النخري عن البكتيريا الشائعة في الأمعاء Clostridium perfringens عندما تتكاثر بشكل مفرط وتفرز سموماً قوية. في صورته الشديدة، يقتل المرض الطيور ويسبب تلفاً واضحاً في الأمعاء. لكن الشكل الأكثر شيوعاً هو الشكل تحت السريري، حيث تُؤذي السموم مثل NetB وalpha toxin بطانة الأمعاء بشكل طفيف. تهضم الطيور العلف بكفاءة أقل، وتكسب وزناً أقل، ومع ذلك تظهر عليها علامات مرض قليلة من الخارج. تقدر الخسائر العالمية الناجمة عن هذا النقص الصامت في الإنتاجية بأكثر من ملياري دولار أمريكي سنوياً لمربي الدواجن. تاريخياً كانت المزارع تتحكم في المشكلة باستخدام مضادات حيوية في العلف، لكن تزايد القلق بشأن مقاومة الميكروبات للمضادات الحيوية وطلب المستهلكين على الدجاج «المربى دون مضادات حيوية» جعل هذه الأدوية أقل قبولاً، مما خلق حاجة ملحّة لبدائل دقيقة وخالية من الأدوية.
تحويل البروبيوتيك إلى مانعات سموم مُستهدَفة
بنى الباحثون على أعمال سابقة مهندسين فيها سلالتين من البكتيريا البروبيوتيكية Limosilactobacillus reuteri لتفرزا «نانوبديز» — شظايا صغيرة جداً من الأجسام المضادة — تلتصق بسم NetB أو alpha toxin وتُعطِّلها. في الدراسة الجديدة اختبروا ما إذا كانت هذه البروبيوتيك المصممة يمكن أن تُحسّن أداء دجاج التسمين المعرض لشكل خفيف وواقعي تجارياً من المرض. على مدار تجربة استغرقت 43 يوماً، وُزِّع أكثر من 2000 طائر إلى أربع مجموعات: مجموعة تحكم مُصابَة؛ مجموعة تلقت مضاداً وقائياً شائعاً (باسترياسين ميثيلين دي ساليسيلات، BMD)؛ مجموعة أعطيت السلالات المهندَسة المنتجة للنانوبديز (المُسَمّات NE01 وNE06)؛ ومجموعة أعطيت السلالات الأصلية غير المهندَسة من البروبيوتيك. جميع الطيور تلقت تطعيماً ضد الكوكسيديوز ثم تعرّضت لـC. perfringens لتحفيز المرض تحت السريري.
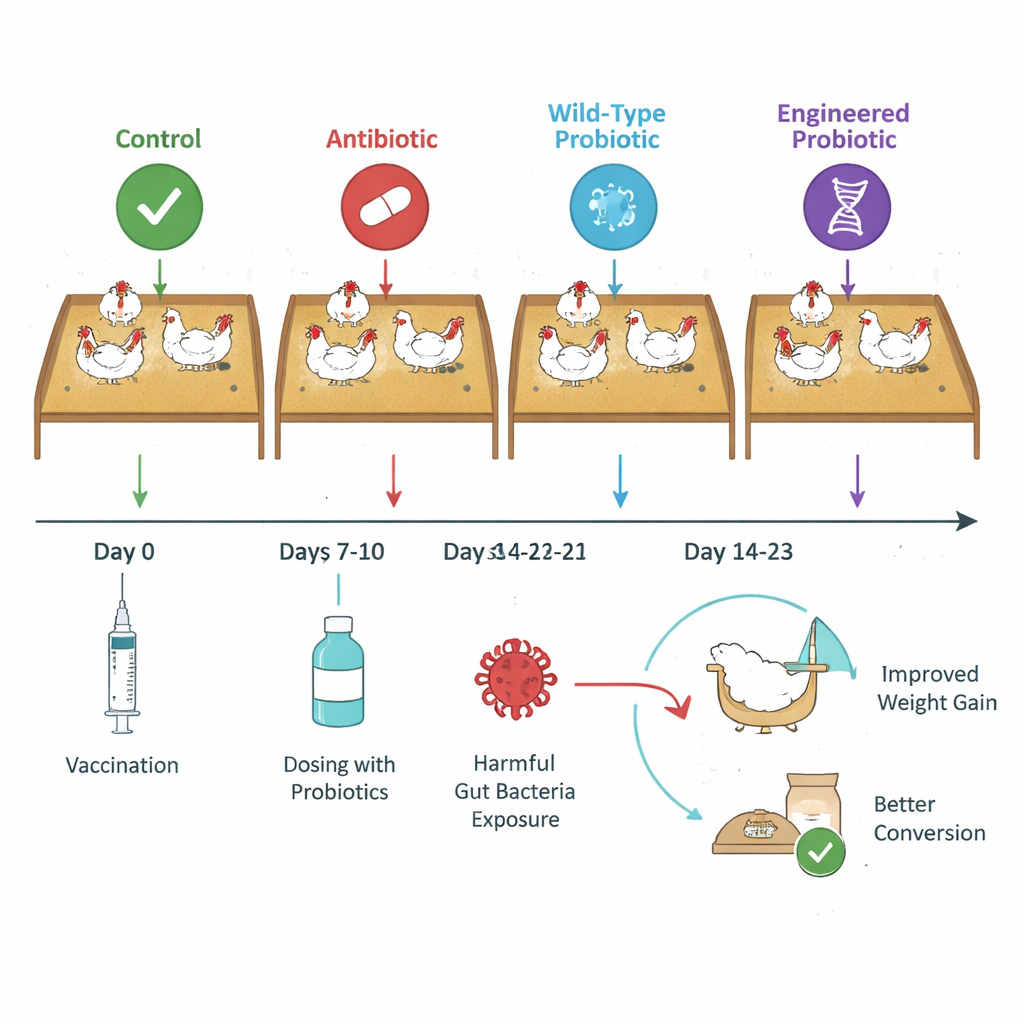
نمو أفضل مع تكاليف خفية أقل
الطيور التي تلقت السلالات المنتجة للنانوبديز حوّلت العلف إلى وزن جسم بكفاءة أكبر باستمرار مقارنة بالمجموعات الأخرى. تحسّن نسبة تحويل العلف المعدَّلة بالوفيات لديهم بمقدار 4–7 «نقاط» (0.04–0.07 وحدة) نسبياً إلى الطيور غير المعالجة في مراحل زمنية مختلفة، وكانوا أثقل بمقدار 34–81 غراماً في نهاية الدراسة مقارنةً بمجموعة التحدي أو مجموعة المضاد الحيوي أو الطيور التي أعطيت بروبيوتيك عادي. من المثير للاهتمام أن مقاييس المرض التقليدية — مثل الآفات المعويّة المرئية وعدد C. perfringens في البراز ومحتويات الأعور — أظهرت فروقاً طفيفة فقط بين المعالجات. هذا يعني أن الطيور كانت كلها تواجه مستوى مشابهاً من التحدي الخفيف، لكن مجموعة النانوبديز كانت تتعامل معه بكفاءة أكبر، محولة نفس العلف إلى لحم أكثر.
ميكروبيومات أكثر هدوءاً وأجهزة مناعية أقل ضوضاءً
لفهم سبب تحسّن الأداء، نظرت المجموعة البحثية إلى ما وراء الأمراض الظاهرة وفحصت الميكروبيوم ونشاط الجينات في الأمعاء والكبد. أظهر التحليل الميتاترنسكربتومي لمحتويات الـ jejunum (الأمعاء الدقيقة) أن الطيور التي تلقت السلالات المهندَسة كان لديها مزيد من نسخات L. reuteri وتعبيراً قابلاً للكشف عن جينات النانوبديز، مؤكداً أن البروبيوتيك نجح في البقاء داخل الأمعاء وإنتاج جزيئاته المانعة للسموم. تغيَّرت التشكيلة الميكروبية العامة أساساً مع تقدم عمر الطيور أكثر من اعتمادها على المعالجة، لكن مجموعة النانوبديز أظهرت تبايناً أقل عينةً بعينة، مما يوحي بمجتمع أمعاء أكثر استقراراً ومرونة. من الناحية الوظيفية عبّرت ميكروبات الأمعاء في هذه المجموعة عن مزيد من الجينات المرتبطة بالتخمير وتركيب البروتين وأقل من الجينات المرتبطة بالتنفس واستخدام النترات — أنماط مرتبطة ببيئة أقل التهاباً. كما لاحظ الباحثون زيادة في تعبير إنزيمات توليد مركب يسمى 2,3-بوتانديول، الذي أظهر تأثيرات مضادة للالتهاب في النماذج الحيوانية.
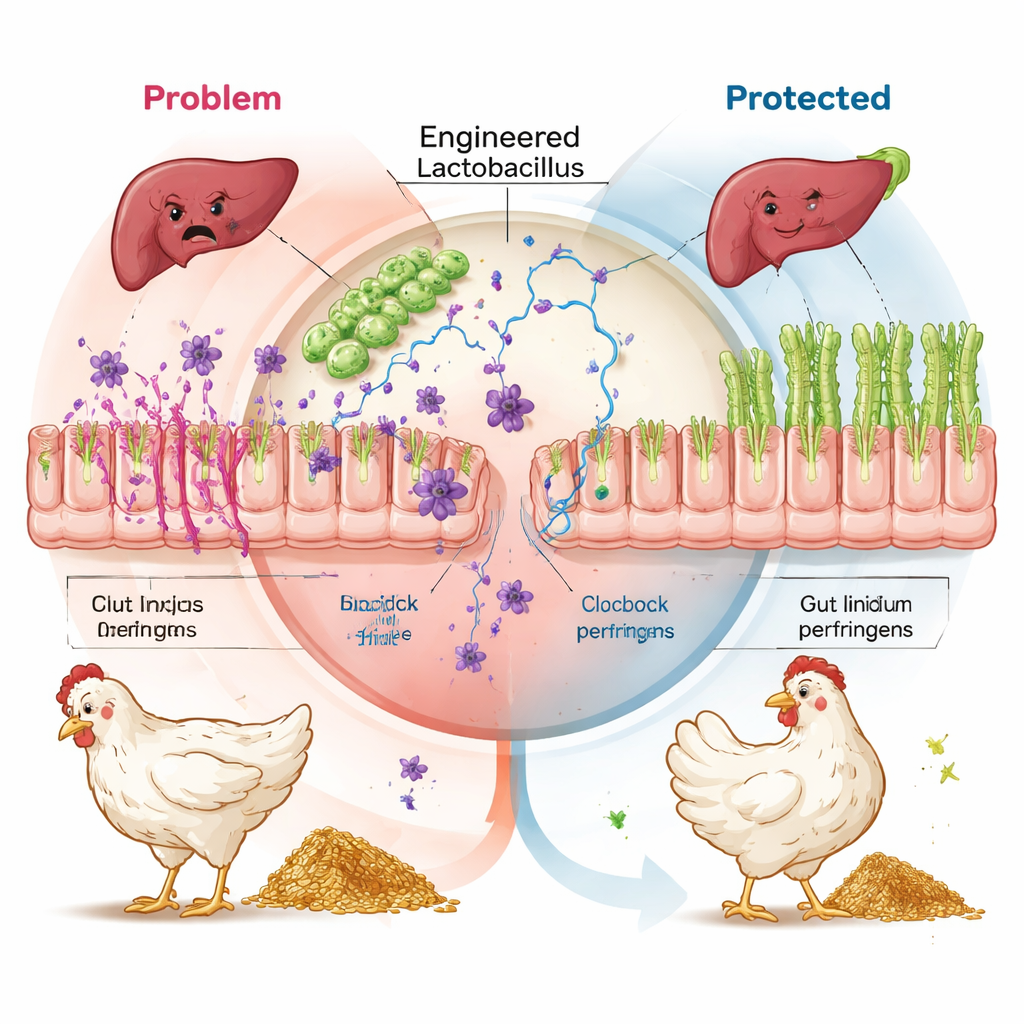
حماية أعضاء بعيدة وزيادة الكفاءة
امتد التأثير إلى ما هو أبعد من الأمعاء. كشف تعبير الجينات في الـ jejunum والكبد أن الطيور التي أعطيت البروبيوتيك المهندَس أظهرت تنشيطاً أقل بكثير لمسارات المناعة والإجهاد التأكسدي مقارنةً بمجموعات التحكم المُصابة، وفي كثير من الحالات مقارنةً بمجموعة المضاد الحيوي والبروبيوتيك العادي. في الكبد — العضو الذي يتعرّض لأضرار جانبية من سموم البكتيريا — أظهرت مجموعة النانوبديز انخفاضاً في الإشارات عبر مسارات الأنسولين وmTOR المعروفة بتصاعدها أثناء الإصابة الناجمة عن السموم، مع تعزيز لمسارات مضادة للأكسدة وتوليد الطاقة. مجتمعة، تشير هذه النتائج إلى أن تحييد NetB وalpha toxin عند سطح الأمعاء يمنع سلسلة من الالتهاب وتلف الأنسجة، مما يوفّر على الطائر التكاليف الأيضية الكبيرة لمواجهة عدوى خفية بشكل مستمر.
ماذا يعني هذا لصحة الدجاج والبشر في المستقبل
للقارئ العام، الرسالة الأساسية هي أن ليست كل «البروبيوتيك» متشابهة. من خلال تزويد البكتيريا النافعة بنانوبديز مستهدفة بدقة، ابتكر الباحثون علاجاً حياً يحمي الدجاج من مرض معوي شائع إلى حد كبير وخفي دون الاعتماد على المضادات الحيوية التقليدية — وقد تفوّق على كل من نظام المضاد الحيوي والبروبيوتيك الاعتيادي. أكلت الطيور علفاً أقل للوصول إلى وزن السوق، مع علامات أقل للضغط الداخلي. إذا أمكن توسيع استراتيجيات مماثلة إلى مواشٍ أخرى، وفي نهاية المطاف إلى البشر، فقد تقدم البروبيوتيك المُهندَسة وسيلة قوية لتعطيل السموم الضارة في الأمعاء مع الحفاظ على الميكروبات المفيدة وإبطاء انتشار مقاومة المضادات الحيوية.
الاستشهاد: Hall, A.N., Manuja, S., Payling, L.M. et al. Lactobacillus-vectored nanobodies improve broiler productivity under sub-clinical necrotic enteritis with associated microbiome and transcriptome changes. npj Biofilms Microbiomes 12, 52 (2026). https://doi.org/10.1038/s41522-026-00916-w
الكلمات المفتاحية: بروبيوتيك مُهندَس, التهاب معوي نخرِي, صحة أمعاء الدواجن, نانوبديز, بدائل للمضادات الحيوية