Clear Sky Science · ar
التفاعل بين التَأسُّل المعتمد على SLC33A1 والمستقل عنه لتأسُّل حمض السياليك بالأو-أسيتيل في تَحفيز CASD1
كيف يمكن لتعديلات سكرية صغيرة أن تشكّل الصحة والمرض
تُغطّى خلايانا بسلاسل سكّرية معقّدة تعمل كبطاقات تعريف جزيئية، توجه الاستجابة المناعية والتطوّر وحتى كيفية ارتباط الفيروسات بها. تستكشف هذه الدراسة تعديلًا دقيقًا لكنه قويًا لتلك السكّرات — إضافة «أغطية» كيميائية صغيرة تسمى مجموعات الأسيتيل إلى سكر طرفي يُدعى حمض السياليك — وتكشف عن جهاز جزيئي مكوَّن من جزئين مفاجئين يتحكّم في هذه العملية داخل جهاز غولجي في الخلية. يساعد فهم هذا النظام المخفي في تفسير بعض الاضطرابات العصبية الشديدة ويقدّم دلائل عن كيفية ضبط الخلايا لأسطحها بدقة في الصحة والمرض. 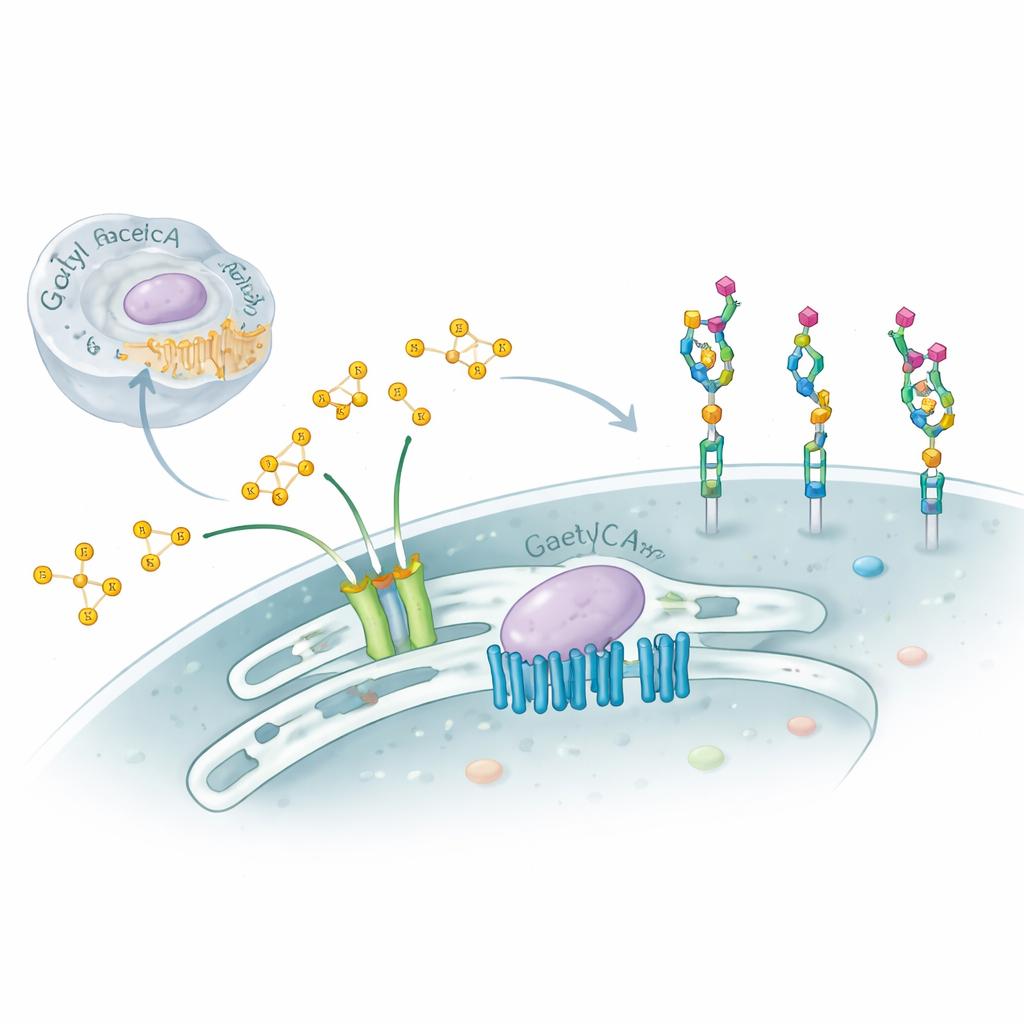
السكّرات الخاصة على سطح الخلية
تقع أحماض السياليك في أطراف العديد من السكّرات السطحية على البروتينات والدهون، وبشكل خاص على جزيئات تُدعى غانغليوسيدات في الدماغ. من خلال تعديل حمض السياليك قليلًا — مثل إضافة مجموعة أو مجموعتين أسيتيليتين في مواقع محددة — تستطيع الخلايا إخفاء مواقع تعرف موجودة أو خلق مواقع جديدة. الفيروسات مثل إنفلونزا C وبعض فيروسات كورونا تبحث تحديدًا عن هذه السكّرات المعدّلة، ويمكن أن تؤثر الغانغليوسيدات الأسيتيلية على مصير خلايا الأعصاب (البقاء أو الموت) وكذلك على نمو السرطانات. ومع ذلك، وعلى الرغم من أهميتها، بقيت الآليات الداخلية للماكينة الخلوية التي تضع هذه مجموعات الأسيتيل في الغولجي غير مفهومة جيدًا.
ناقل وإنزيم يعمَلان معًا
ركّز الباحثون على بروتينين يقيمان في الغولجي أو حوله: SLC33A1، ناقل ينقل الأسيتيل‑CoA (المتبرع الرئيسي بالأسيتيل في الخلية) عبر الأغشية، وCASD1، إنزيم معروف بنقل مجموعات الأسيتيل إلى حمض السياليك. باستخدام تحرير الجينات في خلايا بشرية وهامستر، أزالوا SLC33A1 وراقبوا ما يحدث لغانغليوسيدات محددة. استطاعت الخلايا الخالية من SLC33A1 تكوين الغانغليوسيدات الأساسية GD3 وGD2، لكنها فقدت تمامًا أشكالها المؤكسدة بـ9‑O‑أسيتيل، وهو تعديل مميّز مرتبط بالسرطان والوظيفة العصبية. إعادة إدخال SLC33A1 البشري أعادت هذه الغانغليوسيدات الأسيتيلية، مما يبيّن أن SLC33A1 هو مورد حاسم لأسيتيل‑CoA لهذا المسار. 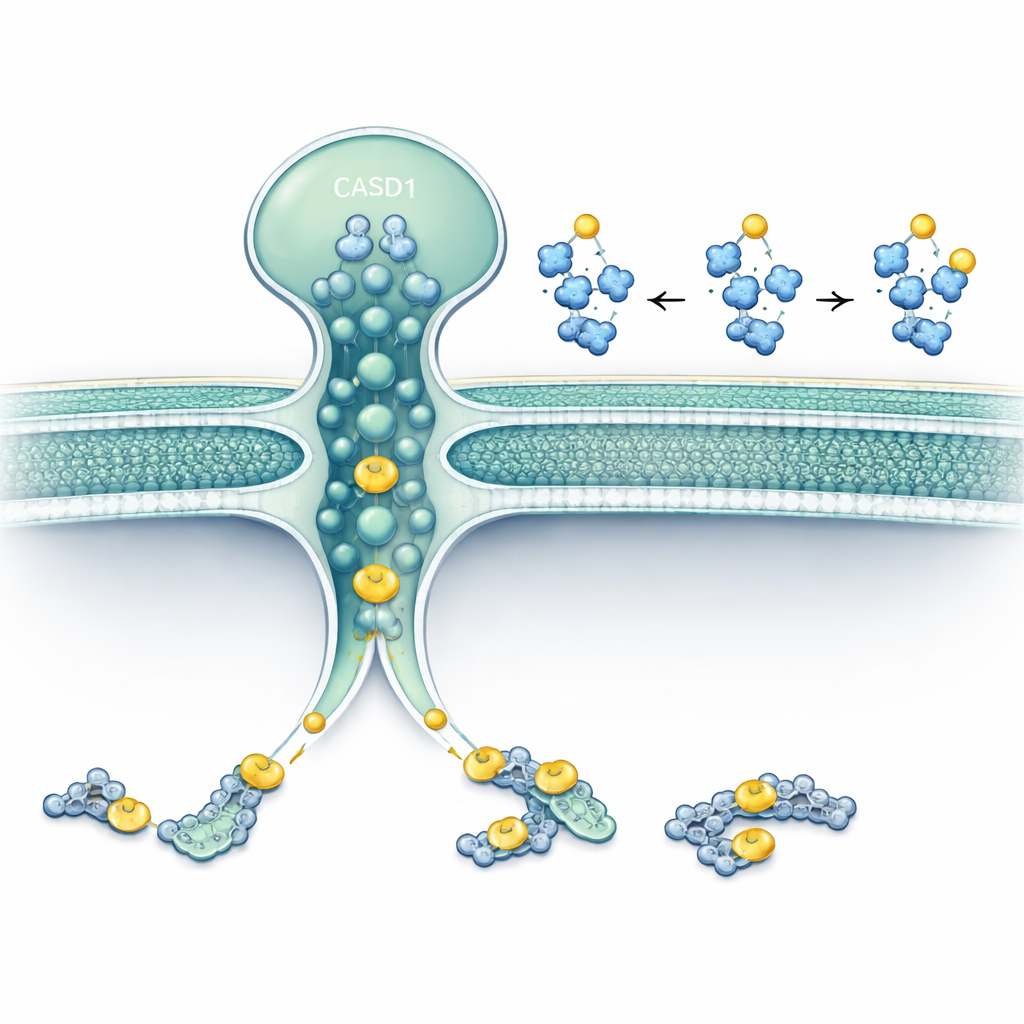
طفرات المرضى تكشف صلة طبية
ارتبط SLC33A1 بعدّة حالات عصبية نادرة، بما في ذلك اضطراب طفولي شديد (متلازمة هوبّك–بريندل)، وشكل من الشلل الرخو الوراثي، والترنّح المخيخي المتأخر الظهور. أعاد الفريق إنشاء أربع متغيرات مشتقة من مرضى في خلايا تفتقد الناقل الطبيعي واختبروا ما إذا كانت هذه النسخ المتغيّرة قادرة على استعادة أسيتلة الغانغليوسيدات. أظهرت جميعها وظيفة منخفضة، وكانت الطفرات الأكثر شدة المسببة للمرض الطفولي بالكاد تعيد أي أسيتلة. مسترشدين ببنية ثلاثية الأبعاد حديثًا لحزمة SLC33A1، رسم المؤلفون هذه الطفرات على البروتين وبيّنوا كيف أنها من المحتمل أن تعطل معمارته أو قدرته على ربط الأسيتيل‑CoA. هذا يشير بقوة إلى أن ضعف أسيتلة الغانغليوسيدات يساهم في الأعراض العصبية التي يُشاهَد عليها المرضى.
موقع نشط ثانٍ خفي في CASD1
كشفت العمل أيضًا عن منعطف غير متوقع: يبدو أن CASD1 نفسه إنزيم ذو غرض مزدوج. الجزء المعروف منه في حجرة الغولجي يستخدم الأسيتيل‑CoA الذي يوصّله SLC33A1. لكن عندما أُزيل SLC33A1، استطاعت الخلايا مع ذلك إضافة مجموعة أسيتيل واحدة إلى أحماض سياليك معينة في ظلّ ظروف معينة، رغم أنها فشلت في إضافة المجموعة الثانية اللازمة لأنماط أكثر تعقيدًا. باستخدام تنبؤ بنيوي متقدّم ومحاكاة جزيئية، أظهر المؤلفون أن الجزء العابر للغشاء من CASD1 يشبه بشدّة ناقل أسيتيل‑ترانسفيراز عابر للغشاء معروفًا من الليزوزومات. حدّدوا أحماض أمينية رئيسية في هذه المنطقة تُقيّد الأسيتيل‑CoA على الجانب السيتوسولي وتنقل مجموعته الأسيتيلية عبر الغشاء مباشرةً إلى حمض السياليك. عندما طُفّرت هذه البقايا، فقد CASD1 هذه النشاطية الثانية في تجارب الأنابيب الحاضنة وفي الخلايا الحية.
مساران، شفرة سكرية واحدة مضبوطة بدقّة
تدعم البيانات مجتمعة نموذج «موقعي‑التحفيز» مزدوج. أحد المسارين يعتمد على SLC33A1 في جلب الأسيتيل‑CoA إلى تجويف الغولجي، حيث تضيف المجال الجوفي لـCASD1 مجموعة أسيتيل إلى حمض السياليك، مما يمكّن من الأنماط الأسيتيلية البسيطة والمزدوجة. المسار الآخر مدمج في لبّ CASD1 العابر للغشاء، والذي يصل مباشرة إلى الأسيتيل‑CoA السيتوسولي ويمكنه أن ينفّذ مستوى أساسيًا من الأسيتلة حتى عند غياب SLC33A1. للمستمع العام، هذا يعني أن إنزيمًا واحدًا، تغذّيه من مصدرين مختلفين للأسيتيل، يضع «علامات ترقيم» دقيقة على سكّرات سطح الخلية. عندما يكون الناقل أو أي جزء من الإنزيم معطلاً، تُختلّ هذه العلامات أو تفقد، الأمر الذي قد يفسّر بعض الأمراض النمائية والعصبية التنكسية ويبرز طبقة جديدة من التنظيم في كيفية تشكيل خلايانا لهويتها السطحية.
الاستشهاد: Albers, M., Bosse, L., Schröter, L. et al. Interplay of SLC33A1-dependent and -independent Golgi sialic acid O-acetylation in CASD1 catalysis. Nat Commun 17, 3156 (2026). https://doi.org/10.1038/s41467-026-71333-y
الكلمات المفتاحية: حمض السياليك, أسيتلة الغولجي, غانغليوسيدات, SLC33A1, CASD1