Clear Sky Science · ar
الديناميكا التركيبية للـ midnolin-بروتيازوم أثناء تدوير العوامل دون اعتماد على يوبكويتين
كيف تتخلص الخلايا من القمامة بسرعة
داخل كل خلية تُصنع البروتينات وتُهدم باستمرار. يُعلَّق كثير منها بجزيئات صغيرة تُسمى اليوبيكويتين قبل أن تُغذى إلى آلة إعادة التدوير الرئيسية في الخلية، البروتيازوم. لكن بعض البروتينات النووية يجب إزالتها بسرعة بالغة لدرجة أنه لا يتوفر وقت لوضع علامات عليها. تكشف هذه الدراسة كيف يندمج بروتين مساعد غير معروف جيدًا، ميدنولين، مباشرة في البروتيازوم لإزالة هذه الأهداف العاجلة، مما يقدم دلائل عن كيفية حفاظ الخلايا على ضبط نشاط الجينات بسرعة ودقة.
اختصار إلى المفرمة الخلوية
البروتيازوم 26S مركب على شكل أسطوانة يقوم بتفكيك البروتينات إلى قطع صغيرة. تقليديًا، يتعرف على الأهداف بقراءة سلاسل اليوبيكويتين المرفقة بها. كشفت أبحاث حديثة عن طريق بديلة: مسار «اختصاري» يرافق فيه ميدنولين بعض البروتينات النووية—وخاصة منتجات جينات البدء الفوري التي تُشغّل وتُطفأ الجينات بسرعة—مباشرة إلى البروتيازوم دون علامات يوبكويتين. هذه البروتينات، مثل عوامل النسخ المشاركة في استجابات الإجهاد والالتهاب، يجب أن تظهر وتختفي خلال دقائق. يجمع البحث الجديد بين المجهر الإلكتروني بالانجماد عالي الدقة وتجارِب بيوكيميائية لرسم خريطة، تقريبًا إطارًا بإطار، لكيفية ترسخ ميدنولين في البروتيازوم ووضع حمولته للتحلل.
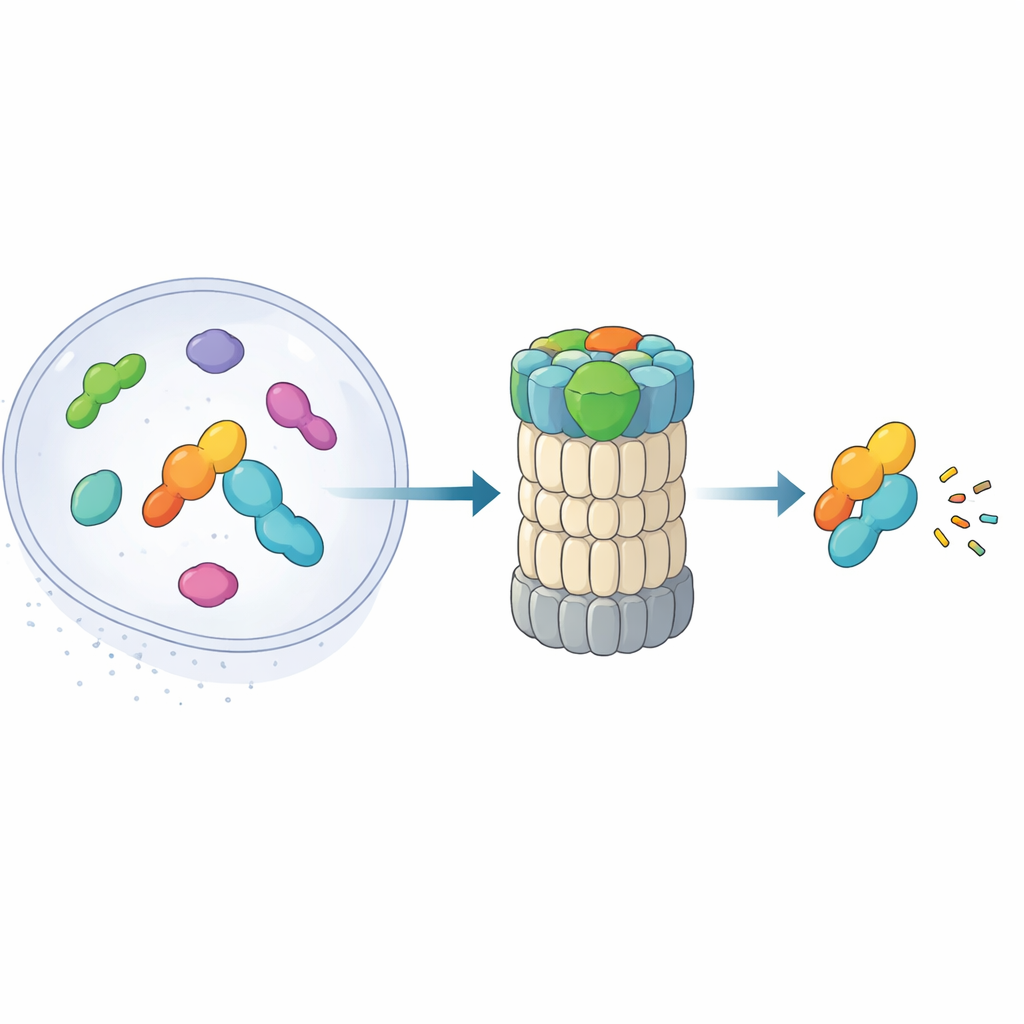
المساعد الثلاثي الأجزاء الذي يمسك بالأهداف ويوجهها
يعمل ميدنولين كأداة متعددة الوظائف بثلاث وحدات رئيسية. أحد الطرفين، حلزون C-طرفي، يركن في موقع رسو على مكوّن من البروتيازوم يُدعى RPN1، مثبتًا ميدنولين على آلة إعادة التدوير. منطقة وسطى تسمى «الصيد» تتعرف وتقبض سمة شبيهة بالخيط (degron) في بروتينات الهدف. في الطرف المقابل توجد منطقة شبيهة باليوبيكويتين. والمفاجأة أن هذه المنطقة ليست مخصصة بالأساس لربط البروتيازوم، كما تفعل مناطق مماثلة في بروتينات الناقل الأخرى. بل تُظهر النتائج أنها تستقر ضد RPN11، إنزيم يقص عادة اليوبيكويتين من الركائز. هنا، يعمل RPN11 أكثر كحامل: من خلال احتضان الجزء الشبيه باليوبيكويتين في ميدنولين، يساعد في تثبيت منطقة الصيد وحمولتها مباشرة فوق فتحة الإدخال الضيقة إلى البروتيازوم.
توجيه البروتين إلى النواة الطاحنة
بعد رسو ميدنولين، يتولى محرك البروتيازوم الجائع للطاقة—حلقة AAA+ ATPase—المهمة. تقع هذه الحلقة تحت فتحة الإدخال مباشرة وتسحب سلاسل البروتين المطوية إلى الداخل خطوة بخطوة. تكشف لقطات الـ cryo-EM عن سلسلة من مواقع «الدرج الحلزوني» التي تتخذها الوحدات الست للمحرك أثناء قبضها وتسليمها للركيزة عبر القناة المركزية. التقط المؤلفون أربع مراحل متتالية من هذه الدورة، وكلها بمادة مرتبطة بميدنولين مخطوطة عبر الفتحة، وحتى شاهدوا كيف يتزامن إفراج أيون المغنيسيوم في إحدى الوحدات مع هبوط حلقة بأكملها. وهذا يشير إلى أن استخدام ATP المنسق وإطلاق المغنيسيوم يساعدان على دفع البروتين إلى عمق الحجرة حيث توجد مواقع القص.
لماذا يهم التموضع والتعبير المشترك
اختبر الفريق كيف تساهم كل وحدة في ميدنولين في الكفاءة. يمكن للحلزون المثبت وحده أن يرتبط بـ RPN1 لكنه لا يعزز نشاط البروتيازوم بشكل ملحوظ. يؤدي إزالة منطقة الصيد إلى إبقاء العديد من البروتيازومات في حالة خمول خالية من الركائز، على الرغم من أن ميدنولين لا يزال قادرًا على الارتباط؛ واستبدال الصيد بركيزة مُلصقة بشكل دائم يفشل أيضًا في استعادة النشاط الكامل. تشير هذه النتائج إلى أن الصيد يفعل أكثر من مجرد الإمساك بالهدف—بل يجب أن يوجه البروتين بدقة عند مدخل الفتحة. تُظهر البيانات البيوكيميائية ونصوص الأورام أيضًا أن ميدنولين يميل إلى أن يُنتج مع ركائزه. عند التعبير المشترك، يطوى ميدنولين بشكل أفضل ويشكل مركبات مستقرة، مكوّنًا حزمة «اهدموني» جاهزة يمكن تسليمها بسرعة إلى البروتيازوم عندما تحتاج الخلية إلى إعادة ضبط التعبير الجيني.
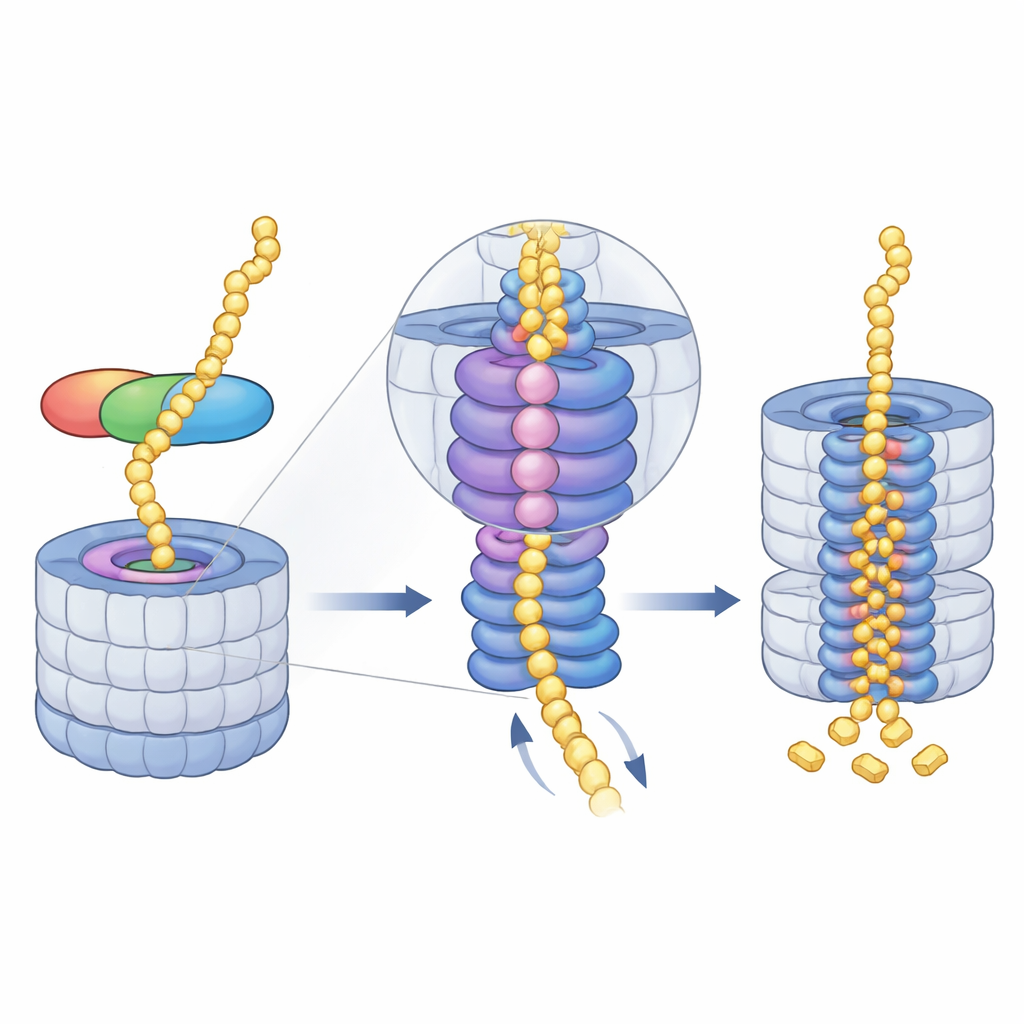
التنظيف الذاتي وإمكانات طبية مستقبلية
بعد أن يُسحب البروتين الهدف ويُقطع، لا ينجو ميدنولين نفسه. يمكن أن تُدفع مناطقه غير المهيكلة داخل المحرك وتُغذى في نفس غرفة التدمير، مما يضمن ألا يتراكم المساعد بلا حاجة. من خلال إضاءة هذا المسار الخالي من اليوبيكويتين إلى البروتيازوم، توسع الدراسة فهمنا لكيفية إدارة الخلايا لأعمار البروتينات على جداول زمنية ضيقة للغاية. كما تلمّح إلى استراتيجيات علاجية جديدة: عبر هندسة جزيئات مبنية على ميدنولين تحزم البروتينات النووية المسببة للأمراض مباشرة إلى البروتيازوم، قد يتمكن الباحثون يومًا ما من القضاء على أهداف «غير قابلة للعلاج» بما في ذلك بعض محفزات السرطان بسرعة وبانتقائية أكبر.
الاستشهاد: Zhu, C., Qin, L., Dai, Z. et al. Structural dynamics of the midnolin-proteasome during ubiquitin-independent substrate turnover. Nat Commun 17, 2800 (2026). https://doi.org/10.1038/s41467-026-71002-0
الكلمات المفتاحية: البروتيازوم, ميدنولين, تحلل البروتين, المسار غير المعتمد على اليوبيكويتين, جينات البدء الفوري