Clear Sky Science · ar
الكفاءة النسخية تحدد قدرة وحدات MSR المعزولة على تكوين النيوكليوتيدات المظلمة
مفاتيح مخفية في حمضنا النووي
تُعبّأ جينوماتنا داخل نواة الخلية بحالتين رئيسيتين: مناطق نشطة تستضيف الجينات، ومقاطع مكثفة عميقًا كانت تُعتبر طويلاً «مادة مظلمة» جينية. يطرح هذا البحث سؤالاً يبدو بسيطًا: ما الذي يجعل بقعة من الحمض النووي تتحول إلى مادة مضغوطة وكاتمة للجينات — المعروفة بالهيتروكروماتين — في المقام الأول؟ من خلال تحليل فئة محددة من الحمض النووي المكرر في الفئران، يكشف المؤلفون أن ليس كل التكرارات متساوية: فقط تلك القادرة على دعم نوع خاص من النسخ يمكنها قلب المفتاح الذي يبني ويحافظ على هذه الأحياء الصامتة من الحمض النووي.
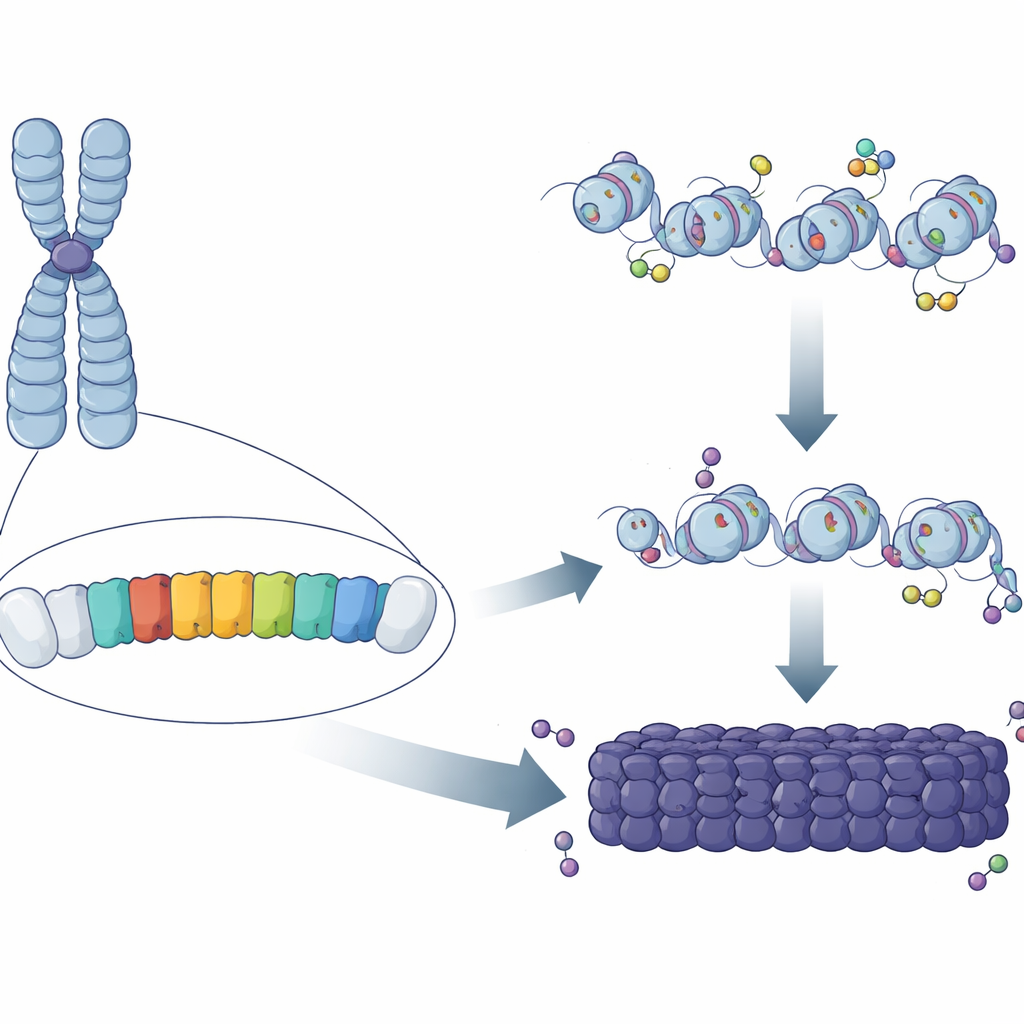
أنماط متكررة في الجينوم
ما يقرب من نصف حمض نووي الثدييات يتكون من تسلسلات مكررة، تتركز العديد منها في مناطق حول مركز الكروموسوم. في الفئران، أحد المكونات الرئيسية لهذه المناطق هو «التكرار القمني الرئيسي» (MSR)، وهو تسلسل قصير غني بالـA/T يُنسخ مئات الآلاف من المرات. أظهرت أعمال كلاسيكية أن هذه المناطق مغطاة بعلامات كيميائية وبروتينات تقفل الحمض النووي في حالة مضغوطة وحامية. لكن ظل غامضًا لماذا تصبح بعض نسخ MSR مُكوَّنة تمامًا كهيتروكروماتين بينما لا تفعل نسخ أخرى متناثرة في أنحاء الجينوم. افترض المؤلفون أن فروقًا صغيرة في التسلسل أو سلوك وحدات MSR الفردية قد تحدد ما إذا كانت قادرة على زراعة، أو «نواة»، رقعة من الهيتروكروماتين.
بناء موقع اختبار داخل الجينوم
لاختبار هذه الفكرة بوضوح، مهندَس الفريق خلايا جذعية جنينية للفأر لتحتوي على منصة إنزال اصطناعية في مقطع هادئ من الكروموسوم 2 — منطقة بلا جينات أو تكرارات قريبة ولا تظهر نشاطًا قابلًا للكشف. في هذا الموقع المحايد أدخلوا شظايا حمض نووي مختلفة: وحدات MSR سليمة، متغيرات MSR مشوشة بشدة، وعناصر ضابطة مثل محفزات فيروسية أو مقاطع من عناصر متحركة. سمح لهم ذلك بسؤال، وحدة بوحدة، أي التسلسلات قادرة على جذب ميزات الهيتروكروماتين المميزة: وسم كيميائي محدد على بروتينات الهيستون (H3K9me3)، ارتباط بروتينات HP1، ودمج هيستون الرابط H1، وكلها معًا تكثف وتثبت الكروماتين المحلي.
فقط التكرارات الجاهزة للنسخ تُزرع الكروماتين الصامت
كانت النتائج انتقائية بشكل لافت. لم تكن وحدة MSR سليمة واحدة مدخلة في موقع الاختبار كافية لتغيير الكروماتين. مع ذلك، فإن ثلاث أو أكثر من النسخ المتتالية من تسلسل MSR السليم حوَّل المنطقة المحيطة إلى «جزيرة» هيتروكروماتين، مع إشارة قوية لـ H3K9me3 وHP1 والهيستون H1. بالمقابل، فشلت مقاطع بنفس الطول من تسلسل MSR المشوش، أو من نوع تكرار آخر (منطقة LINE-1 غير المترجمة 5') في فعل ذلك، رغم أنها كانت قادرة على دفع نسخ قوي. الفرق الرئيسي هو أن وحدات MSR متعددة النسخ السليمة دعمت نسخًا ثنائي الاتجاه معتدلاً أنتج جزيئات RNA قصيرة وغير قياسية مرتبطة بإحكام بالكروماتين. هذا النمط، وليس النسخ العالي الشبيه بالجينات، ارتبط بقدرة زراعة الهيتروكروماتين.
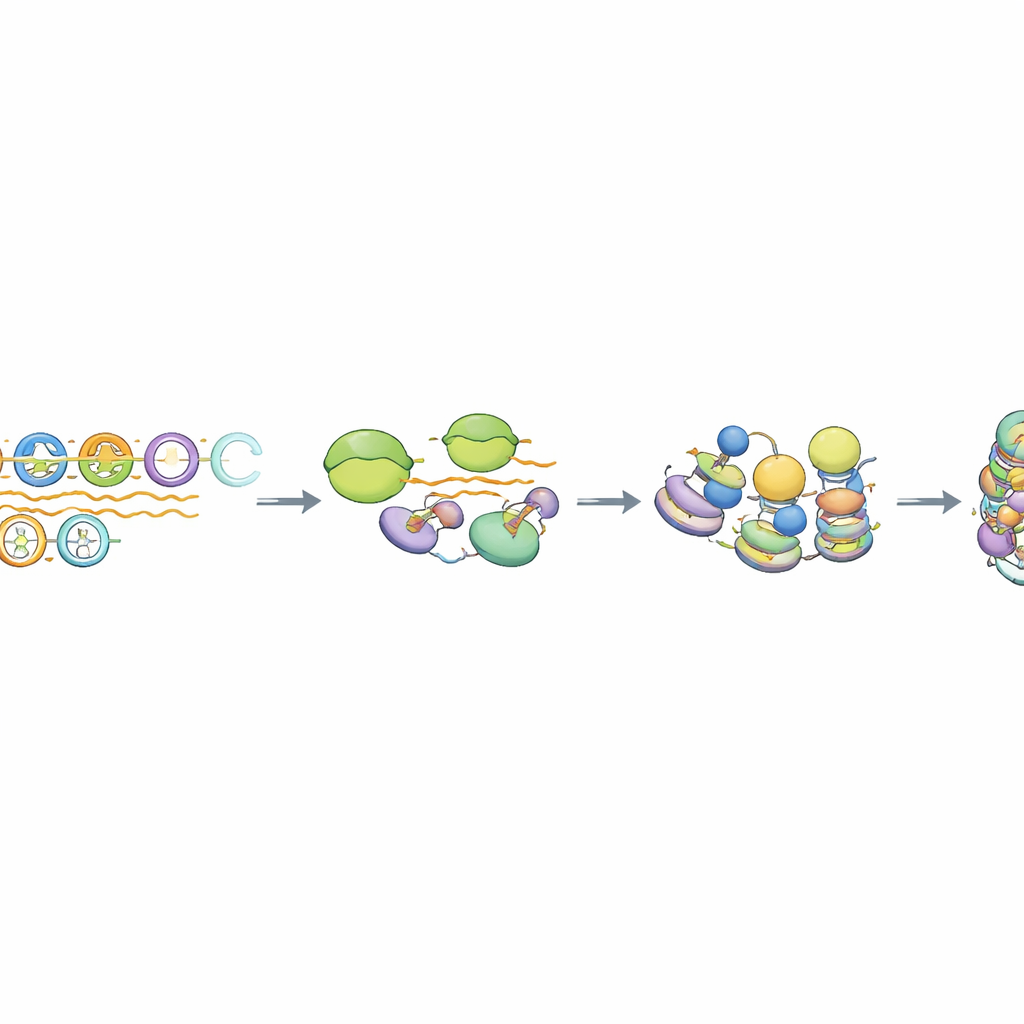
نوع خاص من النسخ ومعالجة الـRNA
بتعمق أكثر، وجد المؤلفون أن بوليميراز RNA II، الإنزيم الذي يصنع عادةً الرنا الرسول، يتفاعل لفترة وجيزة مع مصفوفات MSR لكنه لا يتقدم بكفاءة إلى نصوص طويلة. النتائج كانت RNAs تفتقر إلى سمات الرنا الرسول النموذجية مثل غطاء 5' الحامي والذيول الطويلة من البولي‑A، وتظل قريبة من الحمض النووي الذي أنتجها. كان مجمع بروتيني يُدعى مركب الإنتيغريتر، المعروف بقصّه وإنهائه لبعض الرناوات غير المشفرة، مكثفًا بشكل خاص عند وحدات MSR السليمة. عندما قُلِّلت فعالية القص لمركب الإنتيغريتر، ارتفعت مستويات RNA المشتق من MSR بشكل كبير، لكن وسم الهستون القابض ظل قائمًا بينما تغير ارتباط HP1 بشكل طفيف. أظهر التحليل على مستوى الجينوم أن نحو 10–15% الأكثر سلامة من نسخ MSR فقط تتصرف بهذه الطريقة، مما يبرز مجموعة من التكرارات «الكوّادة» المهيأة لهذا المسار المقرون بالنسخ لكتم الصوت.
الحمض النووي المفكوك كقالب محفز
استكشف الفريق أيضًا كيف يشجع حمض MSR نفسه هذا النسخ غير المألوف. أظهرت مصفوفات MSR متعددة النسخ، لكن ليس النسخ المفردة أو المزدوجة، علامات واضحة على حمض نووي محلي مفكوك وهجائن RNA:DNA، وهي خصائص تركيبية تُرى غالبًا قرب المحفزات النشطة وعند مواقع التوقف. تعززت هذه التراكيب عندما حُبطت إنزيمات التوبويزوميراز، وتزامنت مع ازدياد نسخ MSR وميزات هيتروكروماتين أقوى. يقترح المؤلفون أن ثلاث وحدات MSR متتالية أو أكثر تخلق طوبولوجيا حمض نووي فيزيائية تُحاكي المحفز، داعيةً البوليميراز وعوامل النسخ للتفاعل بما يكفي لتوليد RNAs قصيرة تعمل، مع بروتينات محددة، على تعزيز بنية كروماتين مضغوطة.
لماذا يهم هذا لصحة الجينوم
للمشاهد العادي، يُظهر هذا العمل أن أجزاء من «الحمض النووي القمري» تعمل كمفاتيح مضبوطة بعناية، مستخدمة مزيجًا من شكل الحمض النووي والنسخ منخفض المستوى ومعالجة الرنا لبناء الغلاف الواقي للجينوم. فقط وحدات MSR القادرة على دعم هذا النسخ المسيطر غير الرسول يمكنها إشعال هيتروكروماتين جديد، بينما لا تستطيع العناصر المشوشة أو المفرطة النشاط فعل ذلك. تساعد هذه المنطقية القائمة على الحمض النووي/الحمض النووي الريبي في تفسير كيف تميّز الخلايا بين المناطق التي يجب إبقاؤها صامتة وتلك المسموح باحتضان الجينات، ولماذا يرتبط عدم تنظيم رناوات القمرية بالسرطان ومشاكل التطور. باختصار، تُظهر الدراسة أن «خلفية» التكرارات في الجينوم ليست حشوًا خاملاً بل مهندس نشط لهندسة واستقرار النواة.
الاستشهاد: Lo, YH., Shukeir, N., Erikson, G. et al. Transcriptional competence defines the heterochromatin nucleating potential of isolated MSR units. Nat Commun 17, 2653 (2026). https://doi.org/10.1038/s41467-026-70991-2
الكلمات المفتاحية: الهيتروكروماتين, حمض نووي قمري, حمض نووي ريبوزي غير مشفر, بنية الكروماتين, استقرار الجينوم