Clear Sky Science · ar
تيموسابونين AIII يعزز فعالية خلايا CAR-T ويمنع الانتكاس عبر إضعاف خلايا CAR-T المنظمة
خفض مكابح المناعة لتعزيز علاج السرطان
بالنسبة للأشخاص المصابين بسرطانات دموية عدوانية، يمكن أن يكون علاج خلايا CAR-T مغيرًا للحياة: إذ تُعاد برمجة خلايا المريض المناعية لتتتبع الخلايا الورمية. ومع ذلك، لا يزال العديد من المرضى ينتكسون عندما تفقد هذه الخلايا الهندسية فعاليتها. تبحث هذه الدراسة في جزيء نباتي منشأ، تيموسابونين AIII، يساعد خلايا CAR-T على البقاء نشطة لفترة أطول من خلال تعطيل فرعي محدد داخل جهاز المناعة، مما قد يجعل هذه العلاجات أكثر ديمومة وفعالية.
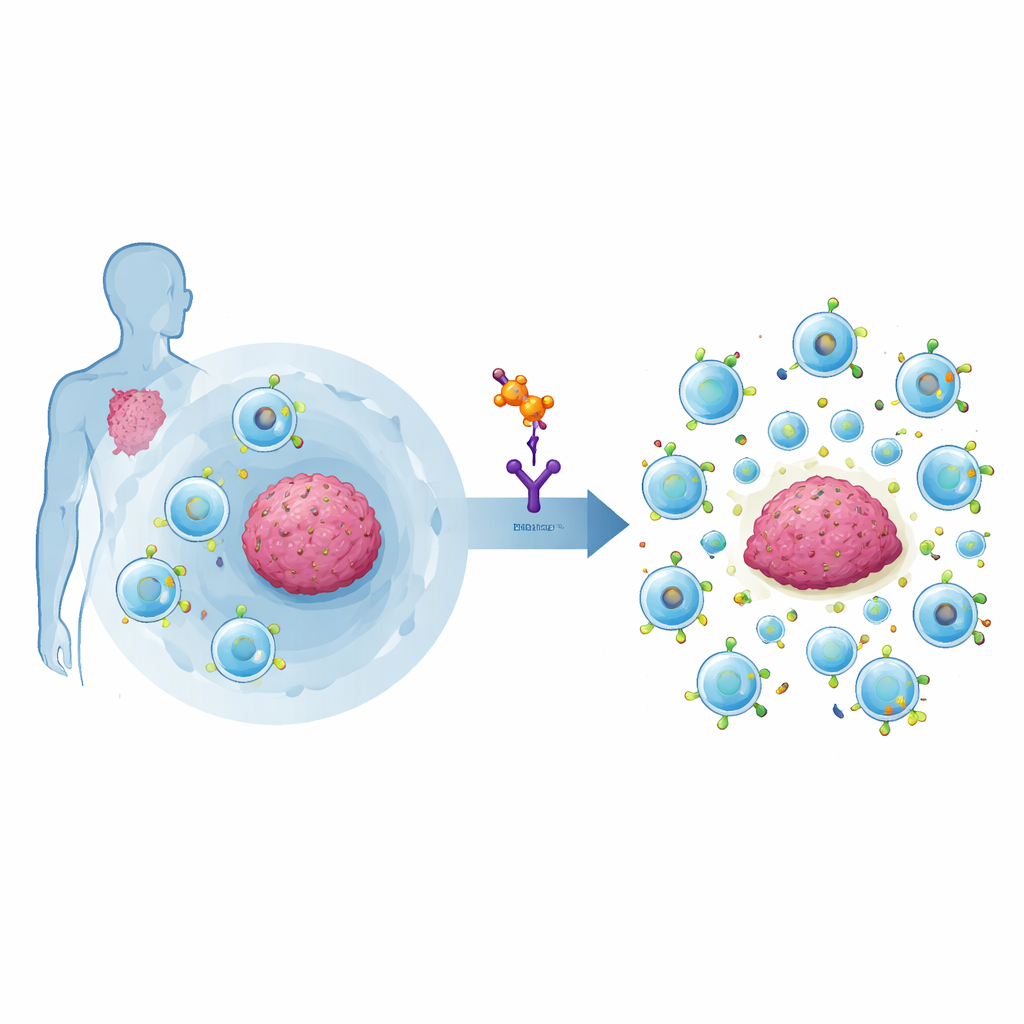
لماذا تتعثر مقاتلات السرطان القوية أحيانًا
خلايا CAR-T هي خلايا مناعية مصممة خصيصًا تحمل مستقبلًا اصطناعيًا للتعرف على أهداف سرطانية مثل CD19 على الخلايا البائية الخبيثة. في المرضى الفعليين، مع ذلك، يستمتع نحو نصف المرضى فقط بهدوء انتكاس طويل الأمد. أحد الأسباب الرئيسية هو مجموعة خاصة من الخلايا المناعية تُسمى الخلايا التائية المنظمة أو Tregs. هذه الخلايا تمنع عادة جهاز المناعة من مهاجمة الأنسجة السليمة، لكن في السرطان يمكنها قمع الاستجابات المضادة للأورام، بما في ذلك استجابات خلايا CAR-T. أظهرت دراسات سريرية حديثة أنه عندما تحتوي منتجات CAR-T على عدد كبير جدًا من Tregs، يكون احتمال مقاومة العلاج أو الانتكاس أعلى بكثير. وللأسف، فإن الأدوية الحالية التي تقلل Tregs غالبًا ما تكون أدوات خشنة، تضر بالخلايا المناعية المفيدة إلى جانب الضارة.
العثور على مساعد لطيف في نبتة طبية
بنى الباحثون نظام فحص يبلّغ عندما ينطفئ مفتاح تحكم مركزي في Treg، البروتين FoxP3، الذي يوقف تنشيط المناعة. اختبروا أكثر من 3000 مركب طبيعي ومعتمد وحددوا تلك التي يمكنها تخفيف قبضة FoxP3 دون قتل الخلايا. برز مرشح واحد: تيموسابونين AIII (TAIII)، جزيء شبيه بالستيرويد من العشبة الصينية التقليدية Anemarrhena asphodeloides، والتي توجد تجارب سريرية عليه بالفعل كعلاج موضعي مضاد للالتهابات الجلدية. في الخلايا التائية البشرية المزروعة في ظروف عادة ما تحولها إلى Tregs، قلّص TAIII بشكل حاد تشكل ونشاط هذه الخلايا القمعية، بينما ترك أنواعًا أخرى من الخلايا التائية إلى حد كبير سليمة. وهذا يوحي بأن TAIII قد يدفع جهاز المناعة بعيدًا عن الكبت ونحو الهجوم.
كيف يحرر جزيء صغير خلايا CAR-T
غطس الفريق في الآلية مستخدمًا مسبارات كيميائية، واختبارات ارتباط البروتين، والنمذجة الحاسوبية لاكتشاف أن TAIII يلتصق بمستقبل الأدينوسين A2A (A2AR)، وهو "مفتاح إيقاف" مناعي معروف يستجيب لمستويات مرتفعة من الأدينوسين في الأورام. بدلاً من حظر موقع الربط الرئيسي، يندفع TAIII إلى منطقة حساسة للكوليسترول في مستقبل الغشاء الخلوي، ويعمل كمثبط تعامل جميعوسي. من خلال إزاحة الليبيدات المشابهة للكوليسترول وتخفيف سلسلة إشارية تنتهي في البروتين CREB، يخفض TAIII إنتاج FoxP3 ويقوض برنامج Treg. عندما أُزيل A2AR من الخلايا التائية أو خلايا CAR-T، فقد TAIII تأثيره، ما يؤكد أن هذا المستقبل هو هدفه الحاسم.
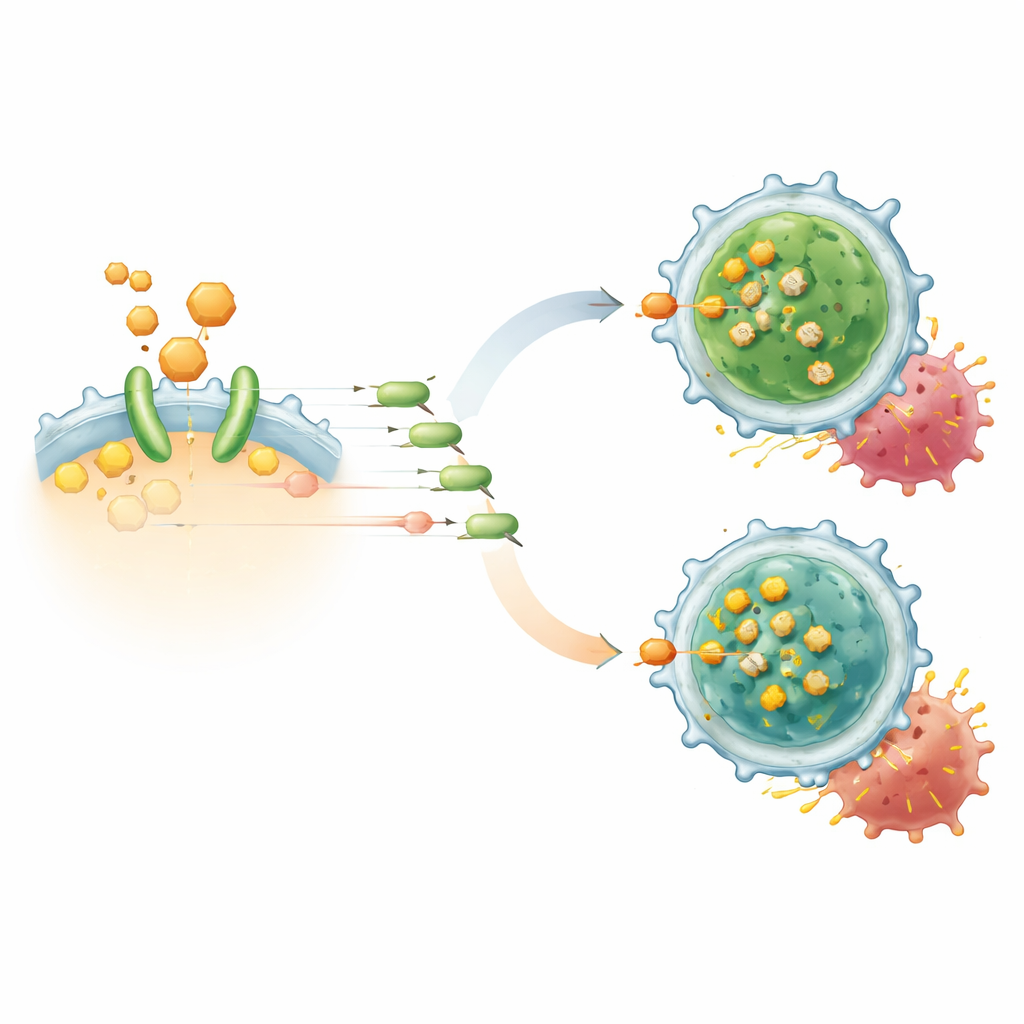
استجابات CAR-T أقوى وأطول أمدًا في النماذج
في تجارب التعايش المخبرية، أدى إضافة TAIII إلى خلايا CAR-T البشرية المستهدفة CD19 إلى زيادة قدرتها على قتل خلايا اللمفوما وزيادة إفراز جزيئات الهجوم مثل الإنترفيرون-غاما وIL-2. وفي الوقت نفسه، قلّلت نسبة خلايا CAR-T الحاملة لصفات شبيهة بـTreg وعزّزت الخلايا التائية الذاكرة المركزية، وهي فئة مرتبطة بالحماية المستمرة. كشفت تسلسلات RNA على مستوى الخلية الواحدة أن تجمعات CAR-T المعالجة بـTAIII احتوت على خلايا تنظيمية منخفضة التعبير عن FoxP3 ومزيدًا من الخلايا القاتلة النشيطة. في نماذج فئران متعددة لأورام دموية وصلبة، أدى الجمع بين TAIII وعلاج CAR-T إلى إبطاء نمو الورم، وتعميق الاستجابات، وتقليل الانتكاسات المتأخرة بشكل كبير. عندما جُردت منتجات CAR-T تجريبيًا من Tregs، لم يعد TAIII يضيف فائدة، ما يؤكد أن دوره الرئيسي هو تفكيك هذه الفئة القمعية بدلاً من التحفيز المفرط لجميع الخلايا التائية.
ما وراء CAR-T: إعادة توصيل حيّ مناعة الورم
لم تقتصر آثار TAIII على الخلايا المهندسة. في فئران ذات مناعة سليمة تحمل أورامًا صلبة، أدت الجرعات اليومية من TAIII إلى تقليل عدد Tregs داخل الأورام، وزيادة تسلل خلايا CD8 "القاتلة"، ورفع مستويات السيتوكينات المضادة للورم، وكل ذلك دون سمية واضحة أو فقدان وزن. عند الجمع مع علاج نقاط التفتيش المضاد لـPD-1—شكل آخر واسع الاستخدام من العلاجات المناعية—عزز TAIII السيطرة على الورم ووسع الخلايا شبيهة بالذاكرة المفيدة. من المهم أن يظهر TAIII تأثيرًا ضئيلاً في فئران شديدة النقص المناعي تفتقر إلى خلايا تائية وظيفية، مما يشير إلى أن نشاطه المضاد للسرطان يعتمد على إعادة تشكيل الاستجابة المناعية بدلاً من تسميم الخلايا السرطانية مباشرة.
ماذا قد يعني هذا لرعاية السرطان في المستقبل
لغير المختصين، الرسالة هي أن الباحثين وجدوا طريقة لتخفيف أحد مكابح جهاز المناعة الانتقائية دون قطع خط الوقود أو الضغط على دواسة الوقود حتى النهاية. من خلال تعديل الخلايا التائية المنظمة عبر تفاعل دقيق مع مستقبل A2A، يساعد تيموسابونين AIII خلايا CAR-T على البقاء نشطة، وتكوين مجموعات ذاكرة أطول عمرًا، وتجنب الصمت بفعل بيئة الورم. في الدراسات ما قبل السريرية والاختبارات مع خلايا CAR-T المأخوذة من مرضى، تجسّد ذلك في قتل أقوى للأورام وانتكاسات أقل. بينما ستحتاج التجارب السريرية إلى تأكيد السلامة والفعالية في البشر، يبرز TAIII كملحق واعد مشتق من النبات قد يجعل العلاجات المناعية المتطورة أكثر ديمومة ونجاحًا على نطاق أوسع.
الاستشهاد: Hou, M., Zhang, W., Qi, Z. et al. Timosaponin AIII enhances CAR-T cell potency and prevents relapse through impairing CAR-Tregs. Nat Commun 17, 3045 (2026). https://doi.org/10.1038/s41467-026-70867-5
الكلمات المفتاحية: علاج خلايا CAR-T, الخلايا التائية المنظمة, مستقبل الأدينوسين A2A, تيموسابونين AIII, المناعة المضادة للسرطان