Clear Sky Science · ar
التغاير المكاني للخلايا المسببة للكبت المناعي (MDSCs) بوساطة إشارة ANXA1-FPRs يقود كبت المناعة في تطور سرطان الخلايا الحرشفية للفم
لماذا تكافح دفاعات الجسم بعض سرطانات الفم
سرطان الخلايا الحرشفية الفموي، وهو شكل شائع من سرطان الفم، غالبًا ما يقاوم أكثر علاجات السرطان الواعدة اليوم: العلاجات المناعية التي تطلق دفاعات الجسم الذاتية. تطرح هذه الدراسة سؤالًا أساسيًا لكنه حاسم: لماذا تفشل الخلايا المناعية القوية، التي يُفترض أن تتعرف على السرطان وتدمره، في هذه الأورام في كثير من الأحيان؟ من خلال رسم خريطة أماكن تواجد الخلايا المختلفة داخل الورم وكيفية تواصلها مع بعضها، يكشف الباحثون عن لعبة متغيرة من «القط والفأر» بين الخلايا السرطانية، والخلايا القمعية المناعية، والخلايا التائية القاتلة التي تشرح فشل العلاج — وتقترح طريقة لإصلاح ذلك. 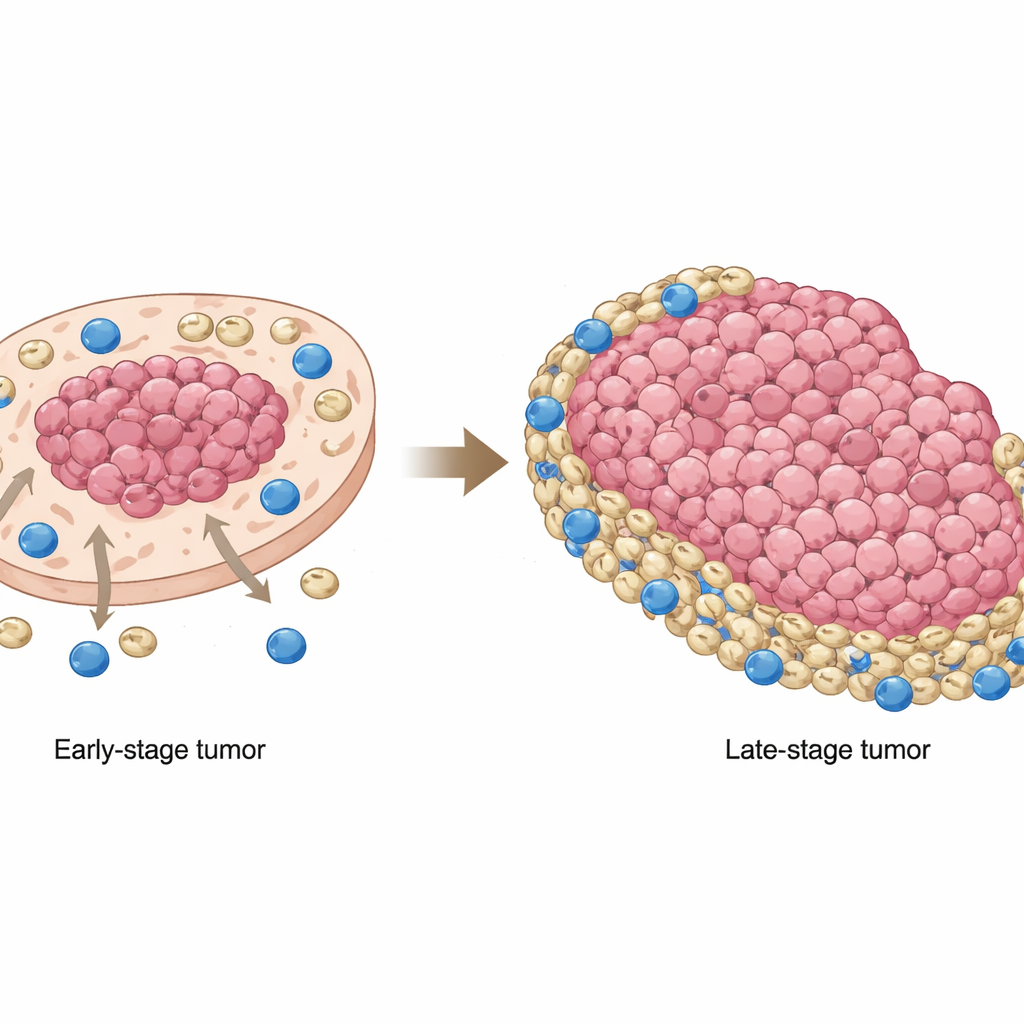
المشهد الخفي داخل الورم
جمع المؤلفون بين طريقتين متقدمتين: تسلسل الحمض النووي الريبي للخلايا المفردة، الذي يقرأ نشاط كل خلية على حدة، والترانسكريبتوميكس المكانية، الذي يحدد مواقع تلك الخلايا داخل شرائح نسيجية حقيقية للورم. من خلال تحليل أورام من مرضى بمراحل مبكرة ومتأخرة من سرطان الفم، حدَّدوا اللاعبين الخلويين الرئيسيين: الخلايا الظهارية السرطانية، الخلايا التائية CD8 «القاتلة»، خلايا تائية وB أخرى، الخلايا الليفية التي تشكل الدعامة البنيوية، وخلايا مناعية متخصصة تسمى الخلايا القمعية المشتقة من النخاع (MDSCs). بينما احتوت الأورام المبكرة على المزيد من خلايا CD8 النشطة، أظهرت الأورام المتأخرة إشارة تائية أضعف وإشارات مهيِّجة لكبح المناعة أقوى من الخلايا النخاعية، مما يشير إلى بيئة تصبح تدريجيًا أكثر عدائية ضد المناعة المضادة للسرطان.
الخلايا القمعية تتحرك
كانت إحدى النتائج الأكثر لفتًا للانتباه هي كيفية تغير موقع خلايا MDSCs مع تقدم الأورام. في السرطانات المبكرة، كانت هذه الخلايا القمعية تميل إلى التجمع داخل مناطق غنية بالخلايا السرطانية، قريبة من قلب الورم. في المراحل المتأخرة، انتقلت إلى الخارج، متراكمة في مناطق فقيرة بالخلايا السرطانية وعلى الحواف، حيث كانت خلايا CD8 أكثر شيوعًا. هذا يعني أنه في الأورام المتقدمة، دفعت الخلايا التائية القاتلة إلى الحواف وباتت تلتقي بحزام من خلايا MDSCs التي خففت قدرتها على مهاجمة الخلايا السرطانية. أكدت عينات المرضى ونماذج الفئران أن هذا التوزيع لم يكن مجرد ظاهرة فضولية: عندما تداخلت MDSCs أقل مع الخلايا السرطانية وركنت بدلًا من ذلك إلى مناطق غير ورمية، كان لدى المرضى بقاء إجمالي أسوأ. 
مفتاح إشاري يتبدل بين الخلايا السرطانية والخلايا القمعية
ركزت الدراسة على «محاورة» جزيئية بين الخلايا السرطانية وMDSCs تشمل بروتينًا يسمى أنكزين A1 (ANXA1) على خلايا الورم وعائلة مستقبلات تُدعى FPRs على الخلايا النخاعية. في المرض المبكر، كان ANXA1 على الخلايا السرطانية يتفاعل بقوة مع FPR1 وFPR3، خصوصًا على MDSCs والبلعمات المرتبطة بالورم، مساعدًا في تجنيد هذه الخلايا القمعية والمحافظة عليها في قلب الورم. مع تقدم السرطان، انخفضت مستويات ANXA1 على خلايا الورم، مضعفة هذه الروابط الأصلية. في الوقت نفسه، بدأت المزيد من MDSCs في التعبير عن مستقبل آخر، FPR2، وبرزت إشارة ANXA1–FPR2 كطريق تعويضي للحفاظ على ارتباط MDSCs. بدا أن شريحة محددة من الخلايا السرطانية ذات مستويات عالية من ANXA1، والتي أظهرت أيضًا خصائص شبيهة بالجذعية، تعمل كـ«طعم»، تجذب MDSCs في المراحل المبكرة؛ عندما انخفض ANXA1، لم تعد MDSCs مُرسَّخة في القلب وتحركت بدلًا من ذلك نحو مناطق غنية بخلايا CD8.
إيقاف الدرع لمساعدة العلاج المناعي
لاختبار ما إذا كان قطع هذا التواصل قد يحسن العلاج، استخدم الباحثون نموذج فأر لسرطان الفم وحجبوا FPR2 بمثبط جزيء صغير يُدعى WRW4. بمفرده، أدى تثبيط FPR2 إلى تقليل وجود MDSCs وزيادة خلايا CD8 في بيئة الورم لكنه لم يبطئ نمو الورم بما يكفي. بالمثل، أظهر العلاج بمضاد لموقع التفتيش المناعي PD-1 بمفرده فوائد متواضعة، لأن MDSCs ما زالت تشكل حاجزًا قمعيًا. عندما جُمعت الدواؤان معًا، مع ذلك، تضاءل نمو الورم بشدة وعاشت الفئران لفترة أطول. في هذه الحيوانات، انخفضت تسلل MDSCs بشكل حاد بينما تسللت خلايا CD8 أعمق إلى مناطق غنية بالخلايا السرطانية، ما يشير إلى أن حجب FPR2 يزيل درعًا رئيسيًا يحمي الخلايا السرطانية عادة من الهجوم المناعي.
ما الذي يعنيه هذا لرعاية السرطان المستقبلية
تُظهر هذه النتائج مجتمعة أن ليس فقط أنواع الخلايا ولكن أيضًا ترتيبها المكاني وشراكاتها الإشارية هي التي تحدد ما إذا كان العلاج المناعي سينجح في سرطان الفم. مع تقدم الأورام، تهاجر MDSCs من المركز إلى الحواف حيث تعترض الخلايا التائية القاتلة، وتساعد إشارات ANXA1–FPR2 في الحفاظ على هذا الترتيب القمعي. عن طريق تعطيل هذا المسار—وخاصة بالاشتراك مع أدوية نقاط التفتيش الحالية—قد يتمكن الأطباء من إعادة تشكيل بيئة الورم حتى تتمكن خلايا الجسم المناعية من التعرف على السرطان وتدميره مرة أخرى. هذا يشير إلى استراتيجية ملموسة: أن الجمع بين حاصرات FPR2 والعلاج المناعي قد يحسن النتائج للمرضى الذين تقاوم أورام فمهم أفضل العلاجات المتاحة حاليًا.
الاستشهاد: Li, F., Han, Y., Ou, F. et al. Spatial heterogeneity of MDSCs mediated by ANXA1-FPRs signaling drives immune suppression in OSCC progression. Nat Commun 17, 2535 (2026). https://doi.org/10.1038/s41467-026-70861-x
الكلمات المفتاحية: سرطان الخلايا الحرشفية الفموي, البيئة الدقيقة للورم, الخلايا القمعية المشتقة من النخاع (MDSCs), الترانسكريبتوميكس المكانية, العلاج المناعي للسرطان