Clear Sky Science · ar
مستشعرات الميكانيك الريبوزومية التركيبية تمكّن استشعار القوى المخصص للخلايا والتحكم الزمني عبر دوائر DNA
الاستماع إلى الخلايا عبر سحبات لطيفة
أجسامنا مليئة بالخلايا التي تدفع وتسحب محيطها باستمرار، مستخدمة قوى دقيقة لتقرير متى تنمو أو تتحرك أو تتغير. تصف هذه الدراسة طريقة جديدة للتطفّف على تلك القوى باستخدام أجهزة قائمة على DNA يمكن ضبطها لتتفاعل مع أنواع خلايا معينة وتفعيلها وإيقافها بمرور الزمن. قد تساعد هذه التقنية يومًا ما المهندسين على توجيه نمو الأنسجة، أو فهم سلوك الأورام، أو تصميم مواد ذكية تتفاعل مع الخلايا الحية في الوقت الحقيقي.
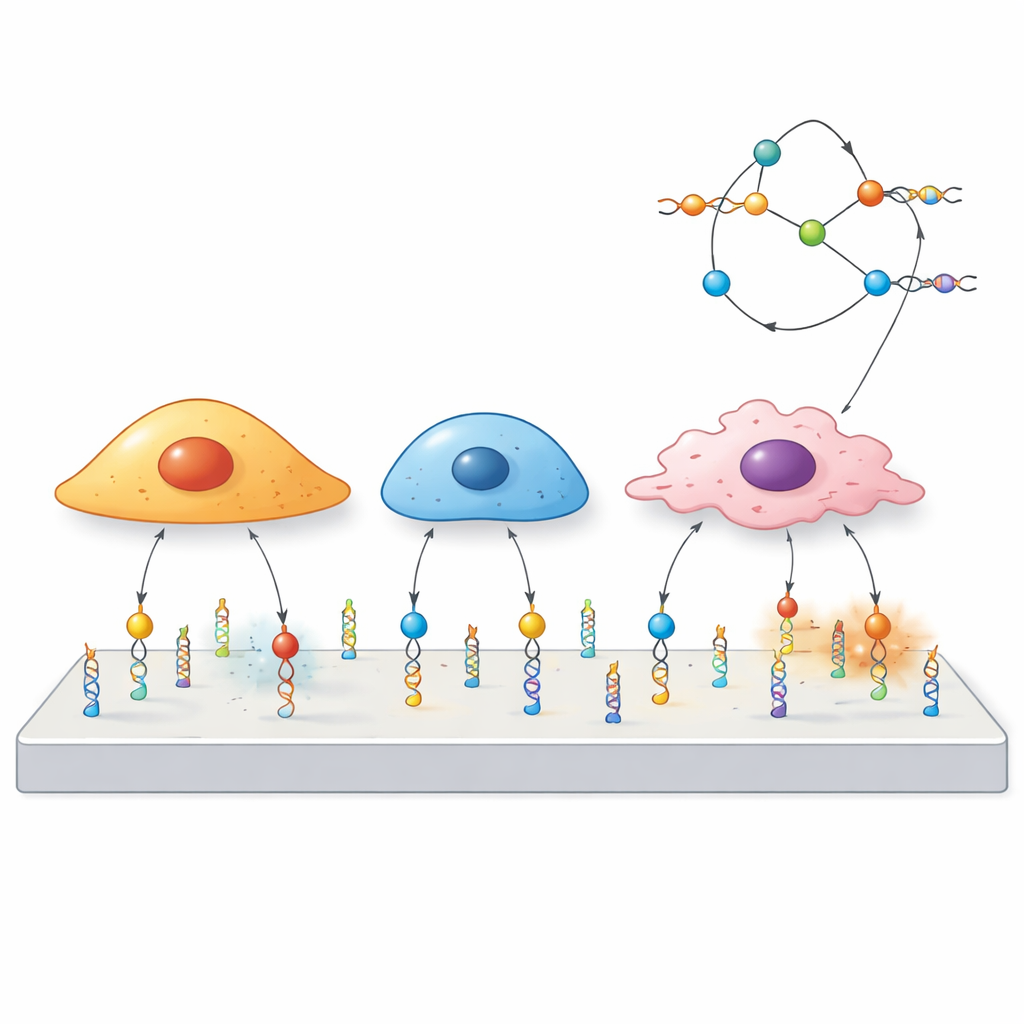
استخدام الـDNA كمفتاح ميكانيكي صغير
بنَى الباحثون «مسبارات ميكانيكية» من الـDNA، نفس الجزيء الذي يحمل المعلومات الوراثية. لكل مسبار ثلاثة أجزاء: تسلسل DNA قصير يُسمى أبتامير يلتصق ببروتين مختار على سطح الخلية، ومقطع مزدوج من الـDNA يعمل كزنبرك مُعدّ للانفصال عند قوة معينة، وصبغة فلورية تضيء عندما ينكسر ذلك الزنبرك. عندما تسحب الخلية المستقبل المرتبط بالأبتامير بقوة كافية، ينفتح المزدوج وتشتغل الإشارة. وبما أن أبتاميرات مختلفة ترتبط بمستقبلات مختلفة، يمكن للفريق أن يحدد مقدمًا أي الخلايا أو البروتينات ستكون قادرة على تفعيل المسبار.
اكتشاف مسارات قوى مخفية على أسطح الخلايا
تركز معظم مستشعرات القوة الحالية على الإنتغرينات، البروتينات المعروفة التي تساعد الخلايا على الإمساك بمحيطها لكنها توجد في أنواع خلايا كثيرة، مما يحد من الانتقائية. هنا استهدفت الفريق بدلًا من ذلك مستقبلات «غير تقليدية» لا يُنظر إليها عادة كمكوّنات ميكانيكية. أظهروا أن أبتاميرًا يسمى AS1411، الذي يربط بروتينًا يُدعى نوكلولين الموجود بكثرة على الخلايا السرطانية، لم يُنتج إشارة إلا عندما تعرّف هدفه بشكل محدد. عبر تصميم مسابر تتطلب قوى أضعف أو أقوى للانفتاح، اكتشفوا أن النوكلولين ينقل قوى معتدلة مقارنةً بالإنتغرينات ولا يساعد بمفرده على انتشار الخلايا على سطح. بالمقابل، أبتامير آخر، Sgc8، الذي يتعرف على المستقبل PTK7، استطاع الإبلاغ عن قوى حتى عندما كانت التصاق الخلايا بالكاد موجودًا، مكونًا أنماطًا حلقية أشارت إلى مصدر حركة مختلف.
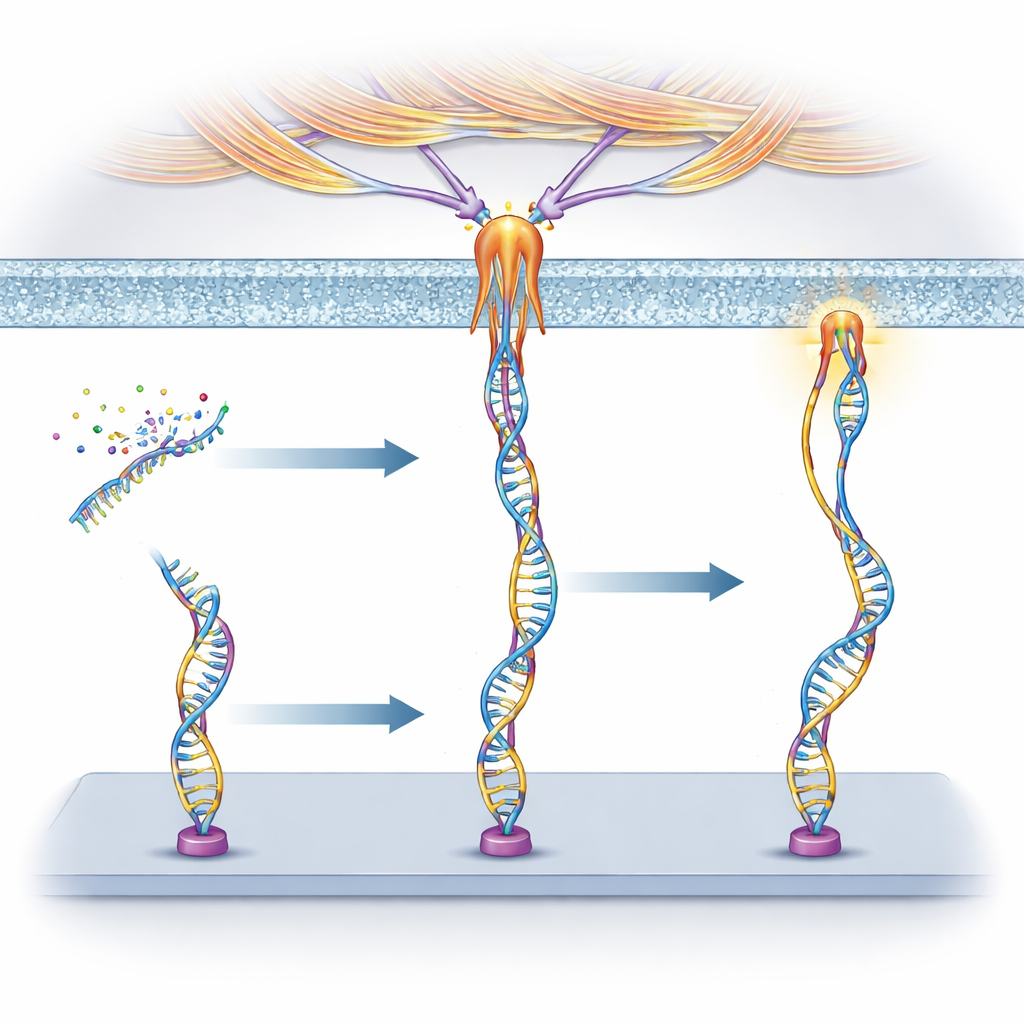
تتبع مصدر تلك القوى
لفهم ما كان يسحب تلك الأجهزة المصنوعة من الـDNA، استخدم الباحثون أدوية تحجب انتقائيًا عمليات خلوية مختلفة. بالنسبة للنوكلولين، وجدوا أن قوته اعتمدت بشدة على الميوزين، نفس بروتين المحرك الذي يساعد العضلات على الانقباض، وظهرت في مواقع تُشكّل فيها الخلية التصاقات بؤرية—نقاط تلامس خاصة تُستخدم للإمساك واستشعار الصلابة. وهذا يوحي أن النوكلولين مرتبط بشكل غير مباشر بآلية الأكتين–ميوزين الداخلية للخلية ويمكنه مشاركة قواها الانقباضية. أما بالنسبة لـPTK7، فكان حجب عملية تُدعى البلعمة الكبيرة (macropinocytosis)—حيث تُجعد الخلايا أغشيتها وتبتلع السائل—قد خفّض الإشارات كثيرًا. نشأت القوى أساسًا من تموجات مبكرة في الغشاء مدفوعة بنمو الأكتين، وليس من خطوات لاحقة في سد الحويصلات، كاشفًا عن مسار ميكانيكي مغاير.
ضبط انتقائية الخلايا بدقة جزيئية
لأن كل أبتامير يتعرف على مستقبل سطحي معيّن، يمكن إعادة برمجة نفس السقالة الـDNA ببساطة عن طريق استبدال أبتامير بآخر. برهن الفريق ذلك باستخدام مسابر تستهدف ثلاثة أهداف مختلفة—PTK7 وmucin-1 وEpCAM—عبر لوحة من خطوط خلايا سرطانية ذات مستويات مرتفعة أو منخفضة من كل بروتين. أنتجت الخلايا الغنية بمستقبل معين إشارات قوية، بينما بالكاد استجابت تلك التي تحتوي على القليل من المستقبل، حتى عندما خُلطت معًا في نفس الطبق. من اللافت أن خلايا تشترك في نفس المستقبل قد تُظهر مع ذلك أنماطًا مكانية مختلفة للقوة، مما يؤكد أن تدفق القوة عبر مستقبل يعتمد ليس فقط على وجوده بل أيضًا على التوصيلات الداخلية لكل نوع خلية.
برمجة متى يُسمح للخلايا بالسحب
مستفيدين من أن الأبتاميرات مكوّنة من DNA، ربط الباحثون مسابيرهم بشبكات تفاعلات DNA تتحكم فيما إذا كان بإمكان الأبتامير أن يرتبط على الإطلاق. يمكن لسلاسل "حاجبة" مكملة أن تخفي الأبتامير مؤقتًا، ويمكن لسلاسل "مفعّلة" لاحقًا أن تزيل الحواجز عبر تفاعل تبادل سلاسل، مستعادةً حساسية القوة. كما صمموا حاجبًا قائمًا على RNA يمكن أن يقصّه إنزيم يُدعى RNase H، وأبطأوا هذا القص باستخدام جزيئات طُعم تتنافس على الإنزيم. بهذه الطريقة، حوّلوا الاستشعار الميكانيكي إلى برنامج زمني: لم تستطع الخلايا توليد إشارات إلا بعد تأخير مدمج أو داخل نوافذ زمنية مختارة.
لماذا يهم هذا للمواد الحية المستقبلية
بعبارات يومية، يحول هذا العمل الـDNA إلى قفل ميكانيكي ذكي يفتح فقط لأنواع خلايا معينة، وتحت قوى محددة، وفي أوقات مختارة. عبر الكشف أن مستقبلات أقل وضوحًا مثل النوكلولين وPTK7 يمكنها نقل معلومات ميكانيكية عبر مسارات داخل الخلية مختلفة تمامًا، يوسع ذلك صورتنا حول كيفية "إحساس" الخلايا ببيئتها. وبما أن النظام كله مبني من الأحماض النووية، فيمكن توصيله مباشرة إلى صندوق أدوات دوائر ونانوأجهزة الـDNA سريع النمو. يخلق ذلك أساسًا لمواد وأنسجة مهندسة لا تكتفي باستشعار متى تدفع أو تسحب الخلايا، بل تستجيب أيضًا بإجراءات بيوكيميائية ذات توقيت محسوب، مما قد يوجّه الشفاء أو النمو أو علاج السرطان بطريقة قابلة للبرمجة بدرجة عالية.
الاستشهاد: Xu, T., Sethi, S., Drees, C. et al. Synthetic aptamer mechanoreceptors enable cell-specific force sensing and temporal control via DNA circuits. Nat Commun 17, 2492 (2026). https://doi.org/10.1038/s41467-026-70765-w
الكلمات المفتاحية: التحويل الميكانيكي الحيوي, أبتاميرات DNA, ميكانيكا الخلايا, علم الأحياء التركيبي, شبكات تفاعلات DNA